Clear Sky Science · ru
Квантование динамики фаг‑хозяин с помощью микрофлюидики капель
Почему крошечные вирусы и капли важны для нас
Вирусы, убивающие бактерии, называемые бактериофагами, вновь рассматриваются как возможные союзники в борьбе с лекарственно‑устойчивыми инфекциями. Но чтобы превратить их в надёжные лекарства, учёным нужно измерять, насколько эффективно отдельные вирусы инфицируют и уничтожают бактерии — то, с чем классические лабораторные методы справляются с трудом. В этой работе представлен подход на основе капель, который одновременно наблюдает тысячи миниатюрных схваток между отдельными вирусами и бактериями, раскрывая, как быстро и как часто инфекции оказываются успешными. Такие точные сведения могут помочь в разработке более эффективных фаговых терапий и углубить наше понимание скрытого мира вирусов, формирующих микробную жизнь на Земле.
Ограничения традиционных тестов на чашках Петри
Десятилетиями исследователи полагались на плакообразные анализы: смешивают вирусы с пластом бактерий в мягком агаре, ждут ночь и затем считают прозрачные пятна, где бактерии были уничтожены. Эти пятна дают оценку числа инфекционных вирусов. Несмотря на надёжность, метод медленный, негибкий и предоставляет лишь конечный снимок процесса. Он не позволяет отслеживать развитие инфекции во времени и объединяет в одном результате многочисленные циклы инфекции и реинфекции. Другие подходы, такие как массовая флуоресценция или тесты на основе ДНК, по‑прежнему усредняют по огромным популяциям, что затрудняет наблюдение единичных событий инфицирования или точную настройку условий, например числа вирусов на одну бактерию.
Превращая каждую инфекцию в крошечную пробирку
Авторы создали высокопроизводительную платформу, которая упаковывает бактерии и фаги в микроскопические капли воды, взвешенные в масле. Два отдельных потока жидкости — один с бактериями, другой с вирусами — встречаются только на узком участке образования капель, так что время экспозиции начинается точно при инкапсуляции. Каждая капля становится изолированной реакционной камерой с точно определённым объёмом и контролируемым соотношением фагов к бактериям. Команда добавляет специальный флуоресцентный краситель, который ярко светится, когда бактериальная ДНК высвобождается после лизиса клетки, служа прямым сигналом успешного разрушения клетки, а не просто наличия вирусного генетического материала.
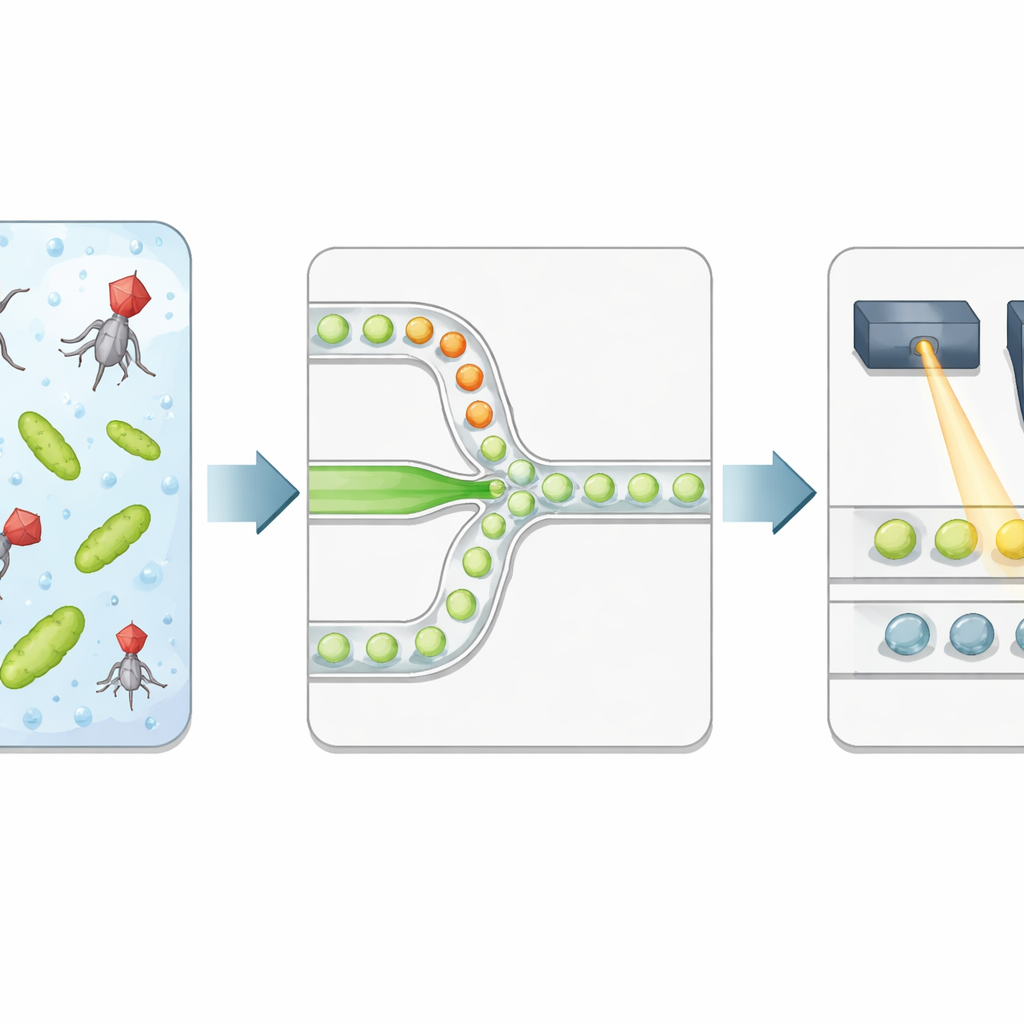
Чтение результатов капель светом
После контролируемой инкубации эмульсию пропускают через второй микрофлюидный чип, который выстраивает капли по одной под фокусированным лазером. Быстрый детектор регистрирует зелёную флуоресценцию от красителя ДНК и красный сигнал от опорного красителя, добавленного при производстве капель. Красный сигнал сообщает о размере капли и о том, сколько вирусного раствора попало в каждую каплю, в то время как зелёный сигнал указывает, произошёл ли лизис. Автоматизированный статистический метод отделяет тусклые капли (без лизиса) от ярких (по крайней мере одна инфицированная и лизированная бактерия), преобразуя эксперимент в строку цифровых 0 и 1. Соотнося долю ярких капель с ожидаемыми числами вирусов и бактерий на каплю, исследователи восстанавливают концентрацию вирусов и сравнивают её с классическими подсчётами по бляшкам.
Настройка условий и изучение скрытой кинетики
Платформа предлагает больше, чем простое счётное определение. Целенаправленно меняя соотношение смешения вирусного и бактериального растворов, команда генерирует субпопуляции капель с разными отношениями вирус:хозяин, всё в рамках одного эксперимента. Это эффективно расширяет диапазон концентраций, в котором анализ даёт точные результаты, и даже выявляет, что не все клетки, видимые в массовых оптических измерениях, действительно подлежат инфицированию. Авторы также варьируют размер капель и время инкубации, чтобы наблюдать, как доля лизированных капель растёт во времени. Их модель адсорбции вирусов на бактериях внутри капель показывает, что время и успех лизиса зависят от истинного числа клеток, способных к инфицированию, и от того, как часто вирусные частицы сталкиваются с ними, но слабо зависят от самого объёма капли.
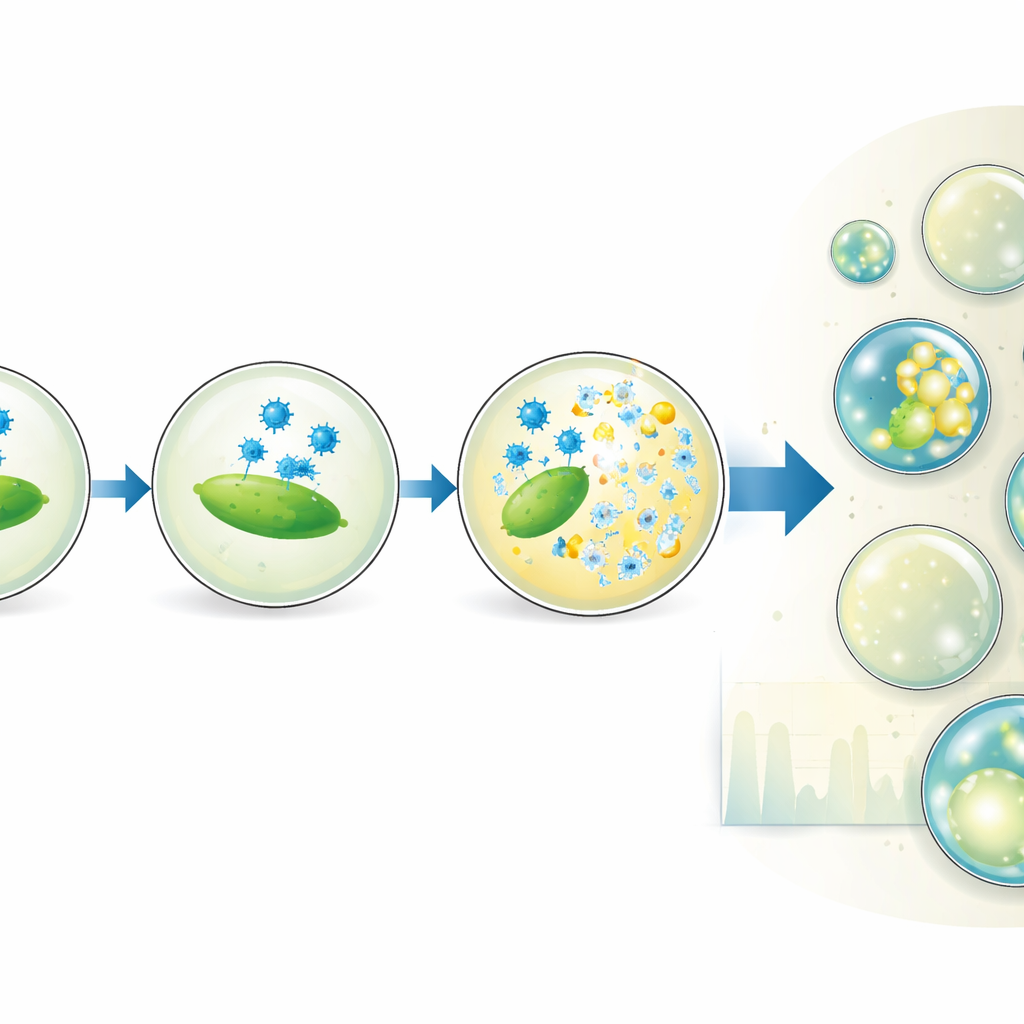
От лабораторного инструмента к будущим терапиям
Изолируя и оцифровывая отдельные события инфицирования, этот капельный метод даёт точные оценки числа вирусов, которые хорошо согласуются с традиционными плаковыми анализами, при этом добавляя информацию с временным разрешением и тонкий контроль над экспериментальными условиями. Метод применим ко многим различным парам лизогенных фаг–бактерия и может масштабироваться до миллионов капель, открывая путь к высокопроизводительному скринингу фаговых вариантов, сред или температур. Практически, работа предоставляет мощный новый способ охарактеризовать, насколько эффективно терапевтические фаги инфицируют свои мишени — важный шаг на пути к использованию этих природных хищников бактерий в борьбе с антибиотико‑резистентными инфекциями.
Цитирование: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Ключевые слова: бактериофаги, микрофлюидные капли, фаговая терапия, инфекция на уровне одиночной клетки, антибиотикорезистентность