Clear Sky Science · pt
Quantificando a dinâmica fago‑hospedeiro usando microfluídica em gotas
Por que vírus minúsculos e gotas importam para nós
Vírus que matam bactérias, chamados bacteriófagos, estão sendo redescobertos como potenciais aliados contra infecções resistentes a medicamentos. Mas, para transformá‑los em terapias confiáveis, os cientistas precisam medir com precisão quão eficientemente vírus individuais infectam e destroem bactérias — algo que os métodos clássicos de laboratório têm dificuldade em fazer. Este artigo apresenta uma abordagem baseada em gotas que observa milhares de batalhas em miniatura entre vírus e bactérias únicas simultaneamente, revelando com que rapidez e com que frequência as infecções têm sucesso. Esses insights precisos podem orientar terapias fágicas melhores e aprofundar nossa compreensão do mundo viral oculto que molda a vida microbiana na Terra.
Limites dos testes tradicionais em placas de Petri
Por décadas, pesquisadores confiaram em ensaios de placas (plaque assays): misturar vírus com um tapete de bactérias em ágar mole, esperar durante a noite e então contar as manchas claras onde as bactérias foram eliminadas. Essas manchas estimam quantos vírus infecciosos estavam presentes. Embora robusto, esse método é lento, inflexível e fornece apenas um instantâneo final. Não é capaz de rastrear como as infecções se desenrolam ao longo do tempo, e mistura incontáveis rodadas de infecção e reinfecção. Outras abordagens, como fluorescência em volume ou testes baseados em DNA, ainda fazem média sobre populações enormes, tornando difícil ver eventos de infecção únicos ou ajustar condições como quantos vírus encontram cada bactéria.
Transformando cada infecção em um tubo de ensaio minúsculo
Os autores construíram uma plataforma de alto rendimento que embala bactérias e fagos em gotas microscópicas de água suspensas em óleo. Dois fluxos líquidos separados — um carregando bactérias, o outro vírus — se encontram apenas na estreita junção onde as gotas são formadas, de modo que o tempo de exposição começa precisamente na encapsulação. Cada gota torna‑se uma câmara de reação isolada com volume bem definido e uma razão controlada de fagos para bactérias. A equipe adiciona um corante fluorescente especial que acende fortemente quando o DNA bacteriano é liberado após a célula estourar, servindo como um indicador direto de lise bem‑sucedida em vez de apenas a presença de material genético viral.
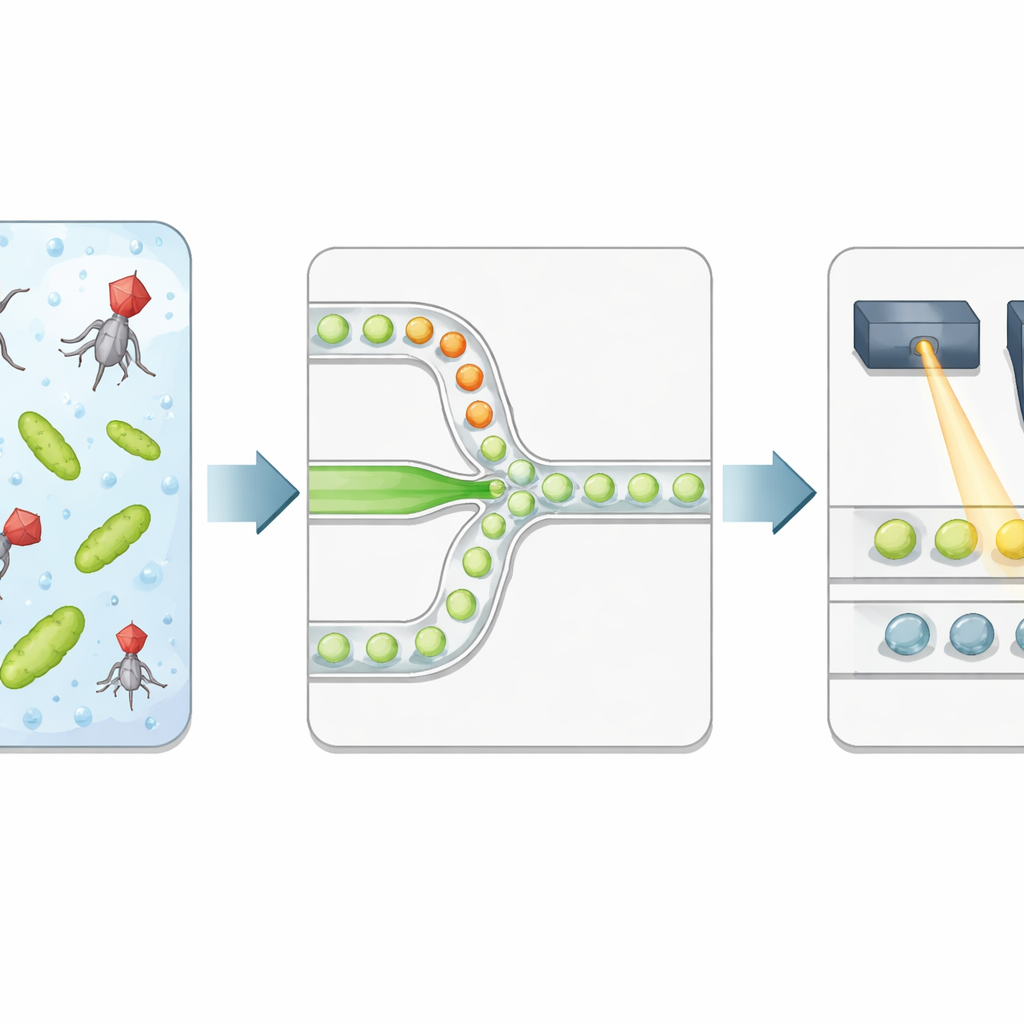
Lendo os resultados das gotas com luz
Após uma incubação controlada, a emulsão é escoada através de um segundo chip microfluídico que alinha as gotas uma a uma sob um laser focalizado. Um detector rápido registra fluorescência verde do corante de DNA e fluorescência vermelha de um corante de referência incluído durante a produção das gotas. O sinal vermelho indica o tamanho da gota e quanto da solução de vírus cada gota recebeu, enquanto o sinal verde indica se houve lise. Um método estatístico automatizado separa gotas escuras (sem lise) das brilhantes (pelo menos uma bactéria infectada e lisada), convertendo o experimento em uma sequência digital de 0s e 1s. Relacionando a fração de gotas brilhantes aos números esperados de vírus e bactérias por gota, os pesquisadores recuperam a concentração viral e a comparam com contagens clássicas por placa.
Ajustando condições e sondando cinéticas ocultas
A plataforma vai além da simples contagem. Ao alterar deliberadamente a razão de mistura das soluções de vírus e bactérias, a equipe gera subpopulações de gotas com diferentes razões vírus‑para‑hospedeiro, tudo dentro de um único experimento. Isso amplia efetivamente a faixa de concentrações na qual o ensaio fornece resultados precisos e até revela que nem todas as bactérias detectadas por medidas óticas em volume são realmente suscetíveis à infecção. Os autores também variam o tamanho das gotas e o tempo de incubação para observar como a parcela de gotas lisadas cresce. Seu modelo de adsorção de vírus em bactérias dentro das gotas mostra que o tempo e o sucesso da lise dependem do número real de células capazes de ser infectadas e da frequência com que partículas virais colidem com elas, mas não dependem fortemente do volume da gota em si.
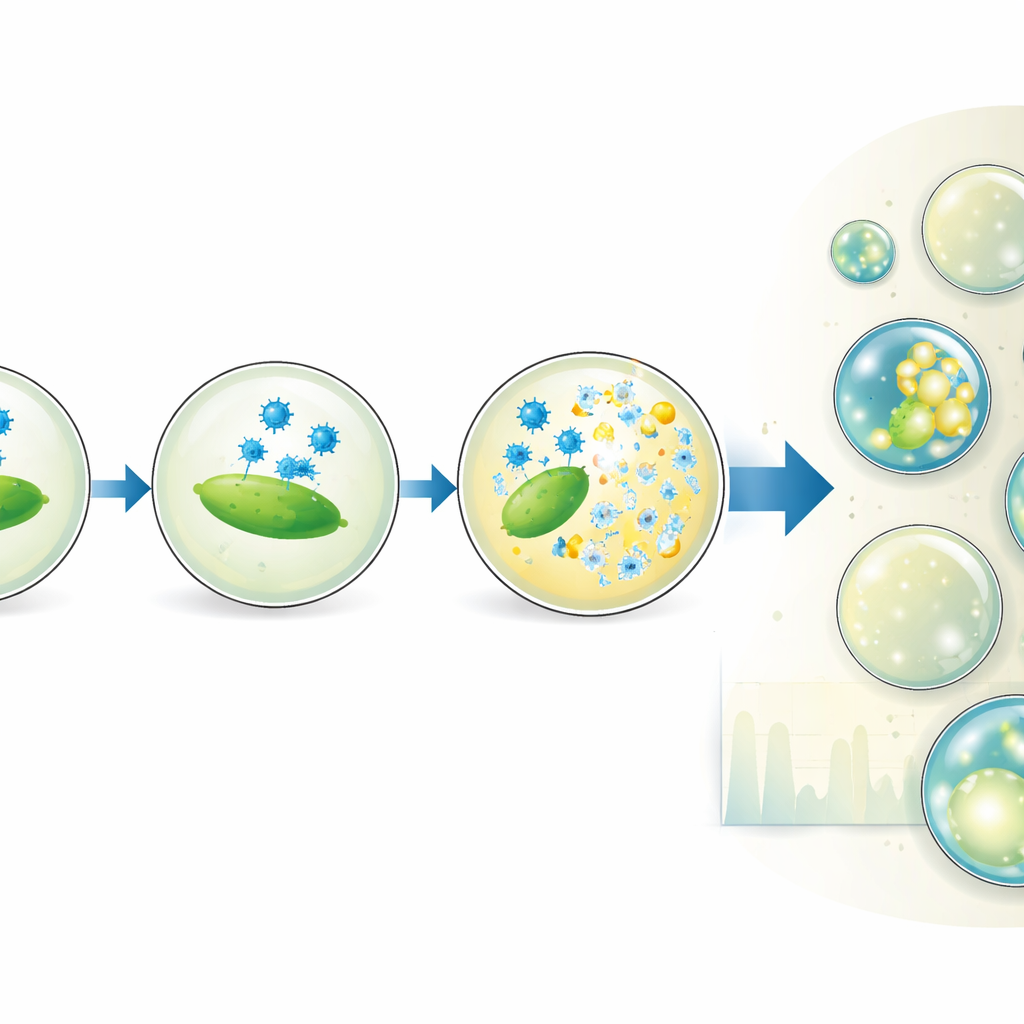
De ferramenta de laboratório a futuras terapias
Ao isolar e digitalizar eventos de infecção individuais, este método em gotas fornece contagens virais precisas que coincidem estreitamente com ensaios clássicos de placa, ao mesmo tempo em que adiciona informação resolvida no tempo e controle fino sobre as condições experimentais. Pode ser aplicado a muitos pares fago–bactéria líticos diferentes e escalado para milhões de gotas, abrindo a porta para triagens de alto rendimento de variantes de fagos, meios ou temperaturas. Em termos práticos, o trabalho oferece uma nova e poderosa forma de caracterizar quão bem fagos terapêuticos infectam seus alvos — um passo importante rumo ao uso desses predadores bacterianos naturais para ajudar a combater infecções resistentes a antibióticos.
Citação: Givelet, L., von Schönberg, S., Katzmeier, F. et al. Quantifying phage-host dynamics using droplet microfluidics. Nat Commun 17, 3857 (2026). https://doi.org/10.1038/s41467-026-72427-3
Palavras-chave: bacteriófagos, gotas microfluídicas, terapia fágica, infecção em célula única, resistência a antibióticos