Clear Sky Science · tr
İntrahepatik kolanjiyokarsinomun proteomik karakterizasyonu risk sınıflandırıcı alt grupları ve EIF4A1’i terapötik hedef olarak tanımlıyor
Bu karaciğer kanseri çalışması neden önemli
İntrahepatik kolanjiyokarsinom, karaciğer içinde ortaya çıkan nadir fakat giderek daha sık görülen bir safra kanalı kanseri türüdür. Genellikle geç evrede tespit edilir, cerrahi sonrası sıkça nüks eder ve doktorların hangi hastaların yeniden hastalanacağını ya da ek tedaviden fayda göreceğini güvenilir biçimde tahmin etme yolları sınırlıdır. Bu çalışma, ileri düzey protein analizini kullanarak bu tümörleri biyolojik olarak farklı gruplara ayırır ve yeni bir ilaçla hedeflenebilecek ortak bir zayıf nokta ortaya çıkarır.
Karaciğer tümörlerinde proteinlere yakından bakmak
Araştırmacılar, ABD ve Almanya’daki büyük tıp merkezlerinde tedavi gören iki hasta grubundan tümör örnekleri ve yakınındaki kanser dışı karaciğer dokusunu incelediler. DNA veya RNA yerine, her örnekte binlerce proteini eşzamanlı olarak nicelendirilebilen gelişmiş kütle spektrometrisiyle ölçtüler. Tümörleri çevre doku ile karşılaştırarak temel hücresel işlevlerde geniş çaplı yeniden düzenlenme gördüler: sağlıklı karaciğer bölgeleri metabolizma ile ilişkili proteinlerce zenginken, tümörler hücre bölünmesi, DNA yönetimi ve hücreleri çevreleyen fibröz madde ile ilişkili proteinlerle doluydu. Bu farklılıklar, protein düzeyindeki bakışın gen verisinden ayrı olarak hastalığın özelliklerini yakaladığını doğruladı.
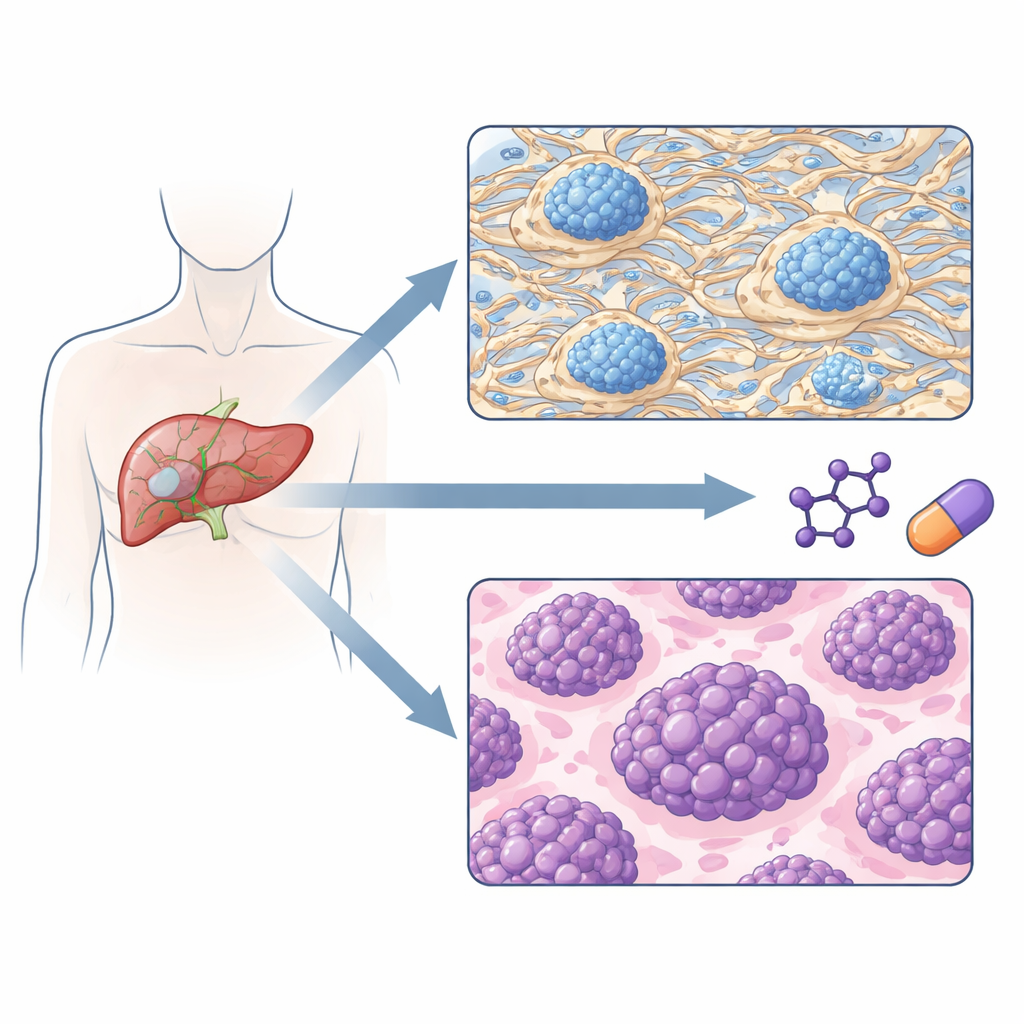
Farklı nüks riski taşıyan iki tümör tipi
Takım, tümörleri yalnızca protein desenlerine göre grupladığında iki ana alt tip ortaya çıktı. Bir alt tip hücreler arasındaki iskeleti oluşturan ekstrapelüler matriksi inşa eden ve yeniden şekillendiren proteinler ile kan pıhtılaşması bileşenleri ve belirli immün sinyallere ağırlık veriyordu. Diğer alt tip ise DNA çoğaltımı, RNA işlemesi ve protein sentezini tetikleyen proteinlerin hakim olduğu; hızlı büyüyen hücrelerin ayırt edici özelliklerini taşıyordu. Önemli olarak, bu iki protein tanımlı grup klinik seyir açısından çok farklıydı: “matrisçe zengin” gruptaki hastalar genellikle daha erken evre tümörlere sahipti ve kanserin tekrar ortaya çıkması daha uzun süre gecikiyordu; oysa “proliferasyon-ağırlıklı” gruptaki hastalar daha erken nüks etti ve genel sağkalımları daha kısaydı.
Hasta grupları arasında işe yarayan basit bir test
Bu bulguları pratik bir araca dönüştürmek için araştırmacılar, yalnızca iki alt tipi en iyi ayıran dört proteine dayalı bir sınıflandırıcı oluşturmak üzere makine öğrenimi kullandılar. Ana hasta setleri üzerinde birçok dört protein kombinasyonunu eğitip test ettiler ve çoğunun alt grupları doğru ayırabildiğini gördüler. En iyi performans gösteren seti kullanarak bu sınıflandırıcıyı, gen ve protein düzeylerinde daha önce karakterize edilmiş büyük bir Çin kohortu da dahil olmak üzere diğer hastanelerden iki bağımsız intrahepatik kolanjiyokarsinom koleksiyonuna uyguladılar. Her iki dış grupta da aynı iki proteomik desen yeniden ortaya çıktı ve matrisçe zengin gruba atanan hastalar yine proliferasyon-ağırlıklı gruptakilere kıyasla daha iyi seyretti. Bu, küçük bir protein panelinin farklı popülasyonlarda nüks riskini tahmin etmede yardımcı olabileceğini gösteriyor.
Her iki alt tipte de ortak bir ilaç hedefi bulmak
Risk tahmininin ötesinde, bilim insanları her iki gruptaki tümörlerde sürekli olarak yükselmiş olan ve terapötik açıdan hedeflenebilir olabilecek proteinleri aradılar. Ümit veren bir aday EIF4A1 oldu; RNA mesajlarını proteinlere çevirmeyi başlatan hücresel makinenin kilit bir bileşeni ve kanserle ilişkili yolaklarla bağlantılı. EIF4A1, alt tipten bağımsız olarak yakındaki karaciğer dokusuna kıyasla tümörlerde belirgin biçimde artmıştı. Ekip, EIF4A1’i bloke eden deneysel bir ilaç olan Zotatifin’i bu kanserlerden türetilmiş hücre hatlarında test etti ve düşük dozların özellikle başka bir yolak inhibitörü ile birlikte verildiğinde hücre canlılığını azalttığını buldu.
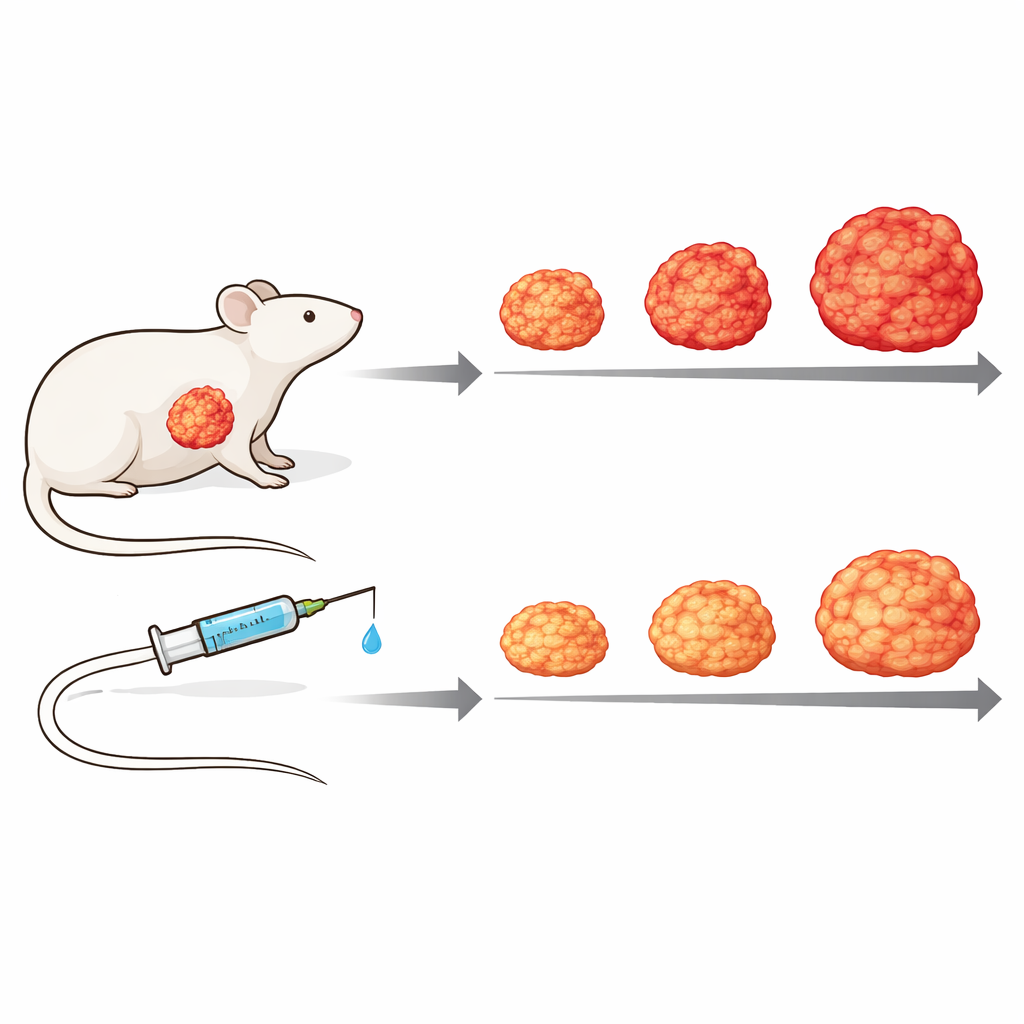
Canlı tümör modelinde ilacın test edilmesi
İnsan hastalığının karmaşıklığını daha iyi taklit etmek için araştırmacılar, bir kişinin tümör parçalarının bağışıklık yetmezliği olan farelere ekildiği hastadan türetilmiş ksenogreft modellerine geçti. İnsan tümör proteinlerini fare stromal proteinlerinden ayırt edebilen protein ölçümleri kullanarak, çevre bağ dokusunun tümörün içsel aktivitesine bağlı olarak farklı yanıt verdiğini gösterdiler; bu da tümör–stroma etkileşiminin önemini vurguluyor. Bu modellerden birinde, haftalık Zotatifin tedavisi tedavi edilmeyen farelere kıyasla tümör büyümesini önemli ölçüde yavaşlattı ve belirgin bir toksisite olmadan tümörler daha yavaş büyüdü, daha küçük kaldı ve tedavi edilen hayvanlar zaman içinde vücut ağırlıklarını daha iyi korudular.
Bu hastalar için ne anlama geliyor
Basitçe söylemek gerekirse, bu çalışma intrahepatik kolanjiyokarsinomun tek bir hastalık olmadığını, cerrahi sonrası nüks olasılığı farklı en az iki ana protein tanımlı tipe ayrıldığını gösteriyor. Odaklanmış dört proteinlik bir test, daha yoğun takip veya ek tedaviden yararlanabilecek daha yüksek riskli hastaları belirlemede doktorlara yardımcı olabilir. Aynı zamanda, her iki alt tipin de çeviri faktörü EIF4A1’e bağımlı olduğunun ve Zotatifin ile bloklanmasının gerçekçi modellerde tümör büyümesini azaltabildiğinin keşfi, potansiyel yeni bir tedavi stratejisine işaret ediyor. İnsanlarda güvenlik ve faydanın doğrulanması için klinik deneyler gerekecek olsa da bu çalışma derin protein profillemenin hem prognozu rafine edebileceğini hem de zor tedavi edilen bir kanserde hedeflenebilir ilaç hedefleri ortaya çıkarabileceğini gösteriyor.
Atıf: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Anahtar kelimeler: intrahepatik kolanjiyokarsinom, kanser proteomikleri, tümör alt tipleri, EIF4A1 inhibisyonu, hastadan türetilmiş ksenogreft