Clear Sky Science · he
אופיינות פרוטאומית של כלת-הכבד התוך-כבדית מזהה תת-קבוצות הממיינות סיכון ואת EIF4A1 כמטרה טיפולית
מדוע מחקר זה על סרטן כבד משמעותי
כלת-הכבד התוך-כבדית היא צורה נדירה אך הולכת וגדלה של סרטן צינורות המרה המתפתחת בתוך הכבד. לרוב היא מתגלה מאוחר, חוזרת לעיתים קרובות גם לאחר ניתוח, והרופאים כיום מעטים האמצעים האמינים לחזות אילו מטופלים יחוו הישנות או ירוויחו מטיפול נוסף. מחקר זה משתמש בניתוח חלבונים מתקדמים כדי למיין את הגידולים הללו לקבוצות ביולוגיות מובחנות ולחשוף נקודת תורפה משותפת שעשויה להיות ניתנת למיקוד באמצעות תרופה חדשה.
מבט קרוב על חלבונים בגידולי כבד
החוקרים בחנו מדגמי גידול ורקמת כבד סמוכה שאינה סרטנית משתי קבוצות מטופלים שטופלו במרכזים רפואיים מובילים בארצות הברית ובגרמניה. במקום להתמקד ב‑DNA או RNA, הם מדדו אלפי חלבונים בכל מדגם באמצעות ספקטרומטריית מסה מתקדמת, טכנולוגיה שיכולה לכמת רבות מולקולות בו‑זמנית. בהשוואת הגידולים אל מול הרקמה הסובבת נצפו שינויים נרחבים בתפקודים בסיסיים של התא: אזורים בריאים בכבד היו עשירים יותר בחלבונים הקשורים למטבוליזם, בעוד הגידולים היו מלאים בחלבונים הקשורים לחלוקת תאים, לעיבוד DNA ולחומר הסיבי שמקיף תאים. הבדלים אלה מאשרים שהמבט ברמת החלבון לוכד תכונות של המחלה שלא נראות מתוך נתוני גנים בלבד.
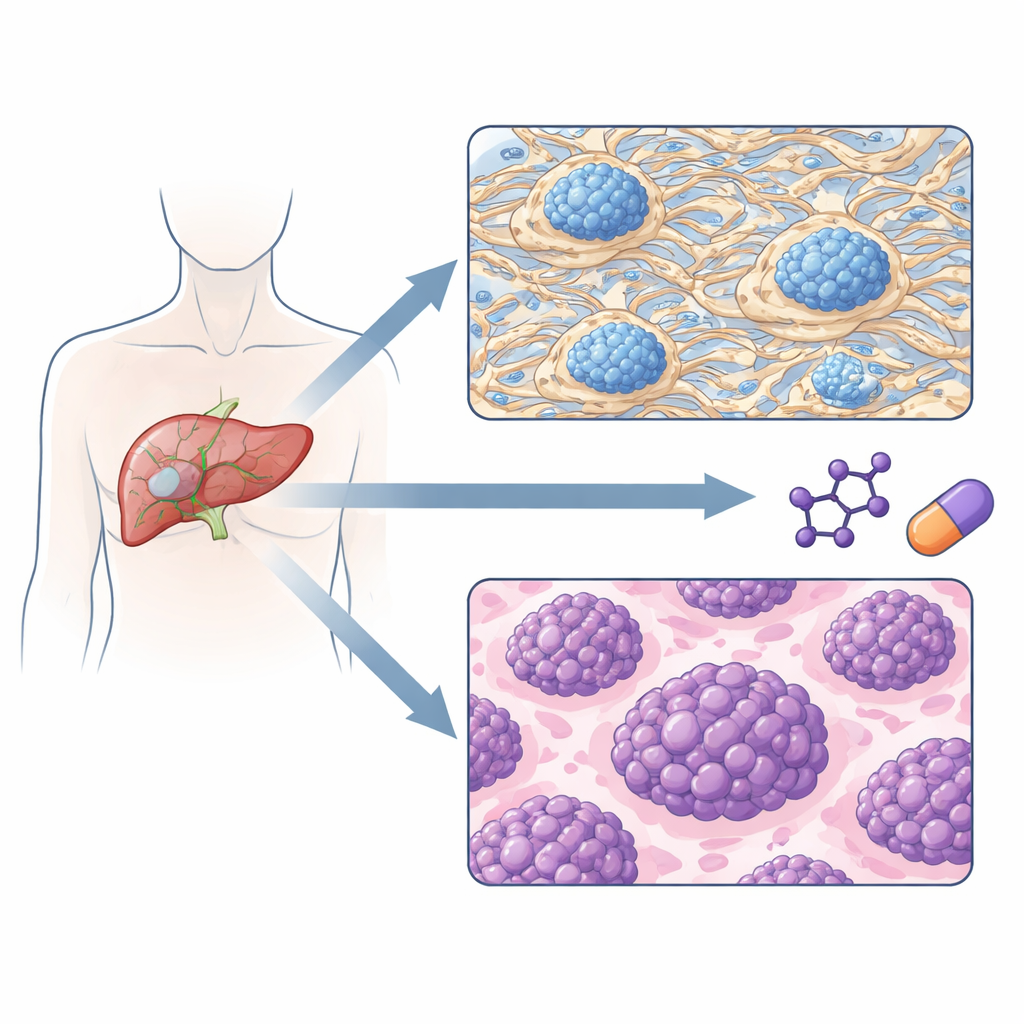
שני סוגי גידול עם סיכונים שונים להישנות
כאשר הקבוצה מיינה את הגידולים אך ורק לפי דפוסי החלבון שלהם, ע emergedו שני תת‑סוגים עיקריים. תת‑סוג אחד נשלט על ידי חלבונים הבונים ומחדשים את המטריצה החוץ‑תאית — השלד בין התאים — יחד עם מרכיבי קרישת דם ואותות חיסוניים מסוימים. התת‑סוג השני נשלט על ידי חלבונים שמניעים שכפול DNA, עיבוד RNA וסינתזת חלבון, כולם סימנים של תאים בעלי גדילה מהירה. באופן מהותי, שתי הקבוצות המוגדרות על‑פי פרוטאום הציגו מהלכים קליניים שונים מאוד: מטופלים בקבוצת "עשירה במטריצה" נטו להציג גידולים בשלבים מוקדמים וחוו פרק זמן ארוך יותר עד להישנות, בעוד מטופלים בקבוצת "כבדה בהתפשטות" חוו הישנות מוקדמת יותר והיו בעלי הישרדות כוללת קצרת יותר.
בדיקה פשוטה שעובדת בחלוקות מטופלים שונות
כדי להפוך תובנות אלו לכלי מעשי יותר, החוקרים השתמשו בלמידת מכונה לבניית מסווג המבוסס על ארבעה חלבונים בלבד שהבחינו בצורה הטובה ביותר בין שני התת‑סוגים. הם אימנו ובדקו קומבינציות רבות של ארבעה חלבונים על מערך המטופלים הראשי ומצאו שרוב הקומבינציות יכולות להפריד במדויק בין תת‑הקבוצות. באמצעות קבוצת החלבונים שהציגה את הביצועים הטובים ביותר, הם החליפו את המסווג לשתי אוספים בלתי תלויים של כלת‑הכבד התוך‑כבדית מבתי חולים אחרים, כולל קוהורט גדול מסין שתואר בעבר ברמות גן וחלבון. בשתי הקבוצות החיצוניות חזרו על עצמן אותם שני דפוסי פרוטאום, ומטופלים המיוחסים לקבוצת המטריצה עשירים שוב היו בתוצאה טובה יותר מאלו בקבוצת ההתפשטות. ממצא זה מרמז כי פאנל חלבונים קטן עשוי לסייע לרופאים להעריך סיכון להישנות באוכלוסיות שונות.
מציאת מטרה תרופתית משותפת בשני תת‑הסוגים
מעבר לניבוי סיכון, המדענים חיפשו חלבונים שהיו מוגברים באופן עקבי בגידולים משני התת‑סוגים ושהיו עשויים להיות ניתנים לטיפול תרופתי. מועמד מבטיח היה EIF4A1, מרכיב מפתח במכונת התא שמתחילה לתרגם מסרי RNA לחלבונים ומקושר למסלולים המקדמים סרטן. EIF4A1 היה מוגבר בעוצמה בגידולים בהשוואה לרקמת הכבד הסמוכה, ללא תלות בתת‑הסוג. הצוות בדק את Zotatifin, תרופה ניסיונית החוסמת את EIF4A1, בקווי תאים שמקורם בסרטן זה ומצא שמינונים נמוכים הפחיתו את הכדאיות שלהם, במיוחד בשילוב עם מעכב מסלול נוסף.
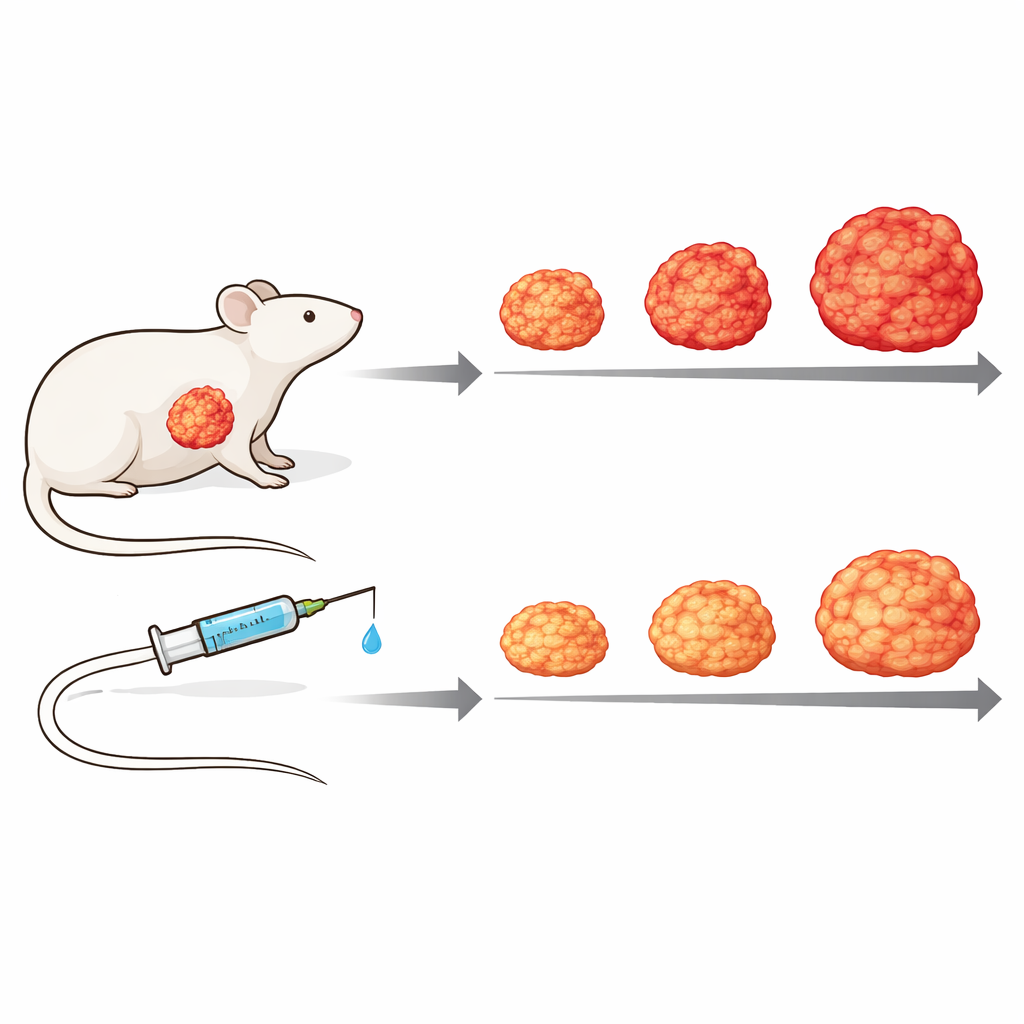
בדיקת התרופה במודל גידול חי
כדי לדמות את המורכבות של המחלה האנושית באופן קרוב יותר, החוקרים עברו למודלים של קושרי גידול הנגזרים ממטופלים, שבהם חלקי גידול של אדם מושתלים בעכברים חסרי מערכת חיסון. באמצעות מדידות חלבון שיכלו להבחין בין חלבוני גידול אנושיים לבין חלבונים של המזנכימה העכברית, הם הראו כי רקמת החיבור הסובבת מגיבה אחרת בהתאם לפעילות הפנימית של הגידול, מה שמדגיש את חשיבות התקשורת בין גידול למזנכימה. באחד המודלים הללו, טיפול שבועי ב‑Zotatifin האט במידה ניכרת את גדילת הגידול בהשוואה לעכברים שלא טופלו, ללא רעילות ברורה: הגידולים גדלו לאט יותר ונשארו קטנים יותר, ובעלי החיים המטופלים שמרו טוב יותר על משקל גופם לאורך זמן.
מבחינת המטופלים — מה משמעות הממצא
במונחים פשוטים, עבודה זו מראה שכלת‑הכבד התוך‑כבדית איננה מחלה אחת אחידה אלא לפחות שני סוגים עיקריים המוגדרים על‑ידי פרוטאום עם סיכויים שונים להישנות לאחר ניתוח. בדיקת חלבונים ממוקדת בארבעה רכיבים עשויה לסייע לרופאים לזהות מטופלים בסיכון גבוה יותר שעשויים להרוויח מעקב אינטנסיבי יותר או מטיפולים נוספים. במקביל, הגילוי ששני תת‑הסוגים תלויים בפקטור התרגום EIF4A1, ושחסימתו באמצעות Zotatifin יכולה לעכב גדילת גידולים במודלים ריאליסטיים, מצביע על אסטרטגיית טיפול פוטנציאלית חדשה. אף שיידרשו ניסויים קליניים לאישור הבטיחות והתועלת בבני אדם, מחקר זה מדגים כיצד פרופיל חלבוני עמוק יכול למקד תחזית ולחשוף מטרות תרופתיות ניתנות לפעולה בסרטן שקשה לטפל בו.
ציטוט: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
מילות מפתח: כלת-כבד תוך-כבדית, פרוטאומיקה של סרטן, תתי-סוגי גידול, עיכוב EIF4A1, קוקסנוגרפים ממטופלים