Clear Sky Science · pt
Caracterização proteômica do colangiocarcinoma intra-hepático identifica subgrupos estratificadores de risco e EIF4A1 como alvo terapêutico
Por que este estudo sobre câncer de fígado é importante
O colangiocarcinoma intra-hepático é uma forma rara, mas cada vez mais comum, de câncer dos ductos biliares que surge dentro do fígado. Geralmente é descoberto tardiamente, frequentemente retorna mesmo após cirurgia, e os médicos atualmente dispõem de poucas maneiras confiáveis de prever quais pacientes irão recair ou se beneficiar de tratamento adicional. Este estudo utiliza análise proteica de ponta para classificar esses tumores em grupos biologicamente distintos e para descobrir um ponto fraco comum que pode ser alvo de um novo fármaco.
Observando de perto as proteínas em tumores hepáticos
Os pesquisadores examinaram amostras de tumor e tecido hepático não canceroso adjacente de dois grupos de pacientes tratados em centros médicos importantes nos Estados Unidos e na Alemanha. Em vez de focar em DNA ou RNA, eles mediram milhares de proteínas em cada amostra usando espectrometria de massa avançada, uma tecnologia capaz de quantificar muitas moléculas simultaneamente. Ao comparar os tumores com o tecido circundante, observaram uma ampla reprogramação de funções celulares básicas: áreas saudáveis do fígado eram mais ricas em proteínas relacionadas ao metabolismo, enquanto os tumores estavam carregados de proteínas associadas à divisão celular, ao processamento do DNA e ao material fibroso que circunda as células. Essas diferenças confirmaram que a perspectiva em nível proteico captura aspectos da doença que não são visíveis apenas pelos dados genéticos.
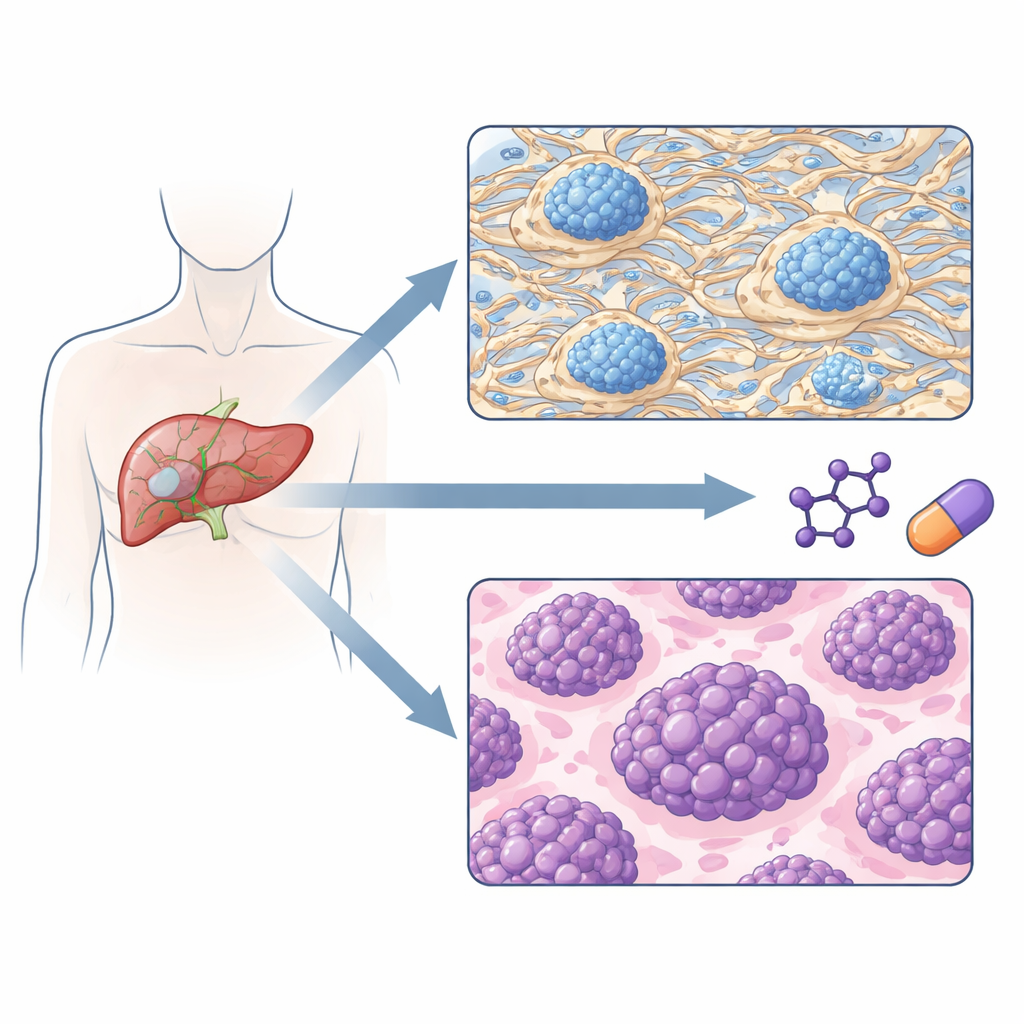
Dois tipos de tumor com riscos diferentes de recidiva
Quando a equipe agrupou os tumores puramente pelos padrões proteicos, surgiram dois subtipos principais. Um subtipo foi dominado por proteínas que constroem e remodelam a matriz extracelular — a estrutura entre as células — juntamente com componentes da coagulação sanguínea e certos sinais imunes. O outro subtipo foi dominado por proteínas que impulsionam a replicação do DNA, o processamento do RNA e a síntese proteica, todas marcas de células de rápido crescimento. Importante, esses dois grupos definidos por proteínas tiveram cursos clínicos muito diferentes: pacientes no grupo “rico em matriz” tenderam a ter tumores em estágios mais iniciais e demoraram muito mais até a recorrência, enquanto pacientes no grupo “de alta proliferação” recidivaram mais cedo e tiveram sobrevida global mais curta.
Um teste simples que funciona em diferentes populações
Para transformar essas descobertas em algo mais próximo de uma ferramenta prática, os pesquisadores usaram aprendizado de máquina para construir um classificador baseado em apenas quatro proteínas que melhor distinguiam os dois subtipos. Eles treinaram e testaram muitas combinações de quatro proteínas em seu conjunto principal de pacientes e verificaram que a maioria podia separar os subgrupos com precisão. Usando o conjunto de melhor desempenho, aplicaram então esse classificador a duas coleções independentes de colangiocarcinoma intra-hepático de outros hospitais, incluindo uma grande coorte chinesa previamente caracterizada em níveis gênicos e proteicos. Em ambos os grupos externos, os mesmos dois padrões proteômicos reapareceram, e os pacientes classificados no grupo rico em matriz novamente tiveram melhor prognóstico do que os do grupo de alta proliferação. Isso sugere que um painel pequeno de proteínas poderia ajudar os médicos a estimar o risco de recidiva em diferentes populações.
Encontrando um alvo medicamentoso comum a ambos os subtipos
Além da previsão de risco, os cientistas buscaram proteínas consistentemente elevadas em tumores de ambos os grupos e que pudessem ser passíveis de terapia. Um candidato promissor foi EIF4A1, um componente chave da maquinaria celular que inicia a tradução de mensagens de RNA em proteínas e que está ligado a vias promotoras do câncer. EIF4A1 estava fortemente aumentado nos tumores em comparação com o tecido hepático adjacente, independentemente do subtipo. A equipe testou Zotatifin, um fármaco experimental que bloqueia EIF4A1, em linhagens celulares derivadas desse câncer e verificou que baixas doses reduziram sua viabilidade, especialmente quando combinadas com um inibidor de outra via.
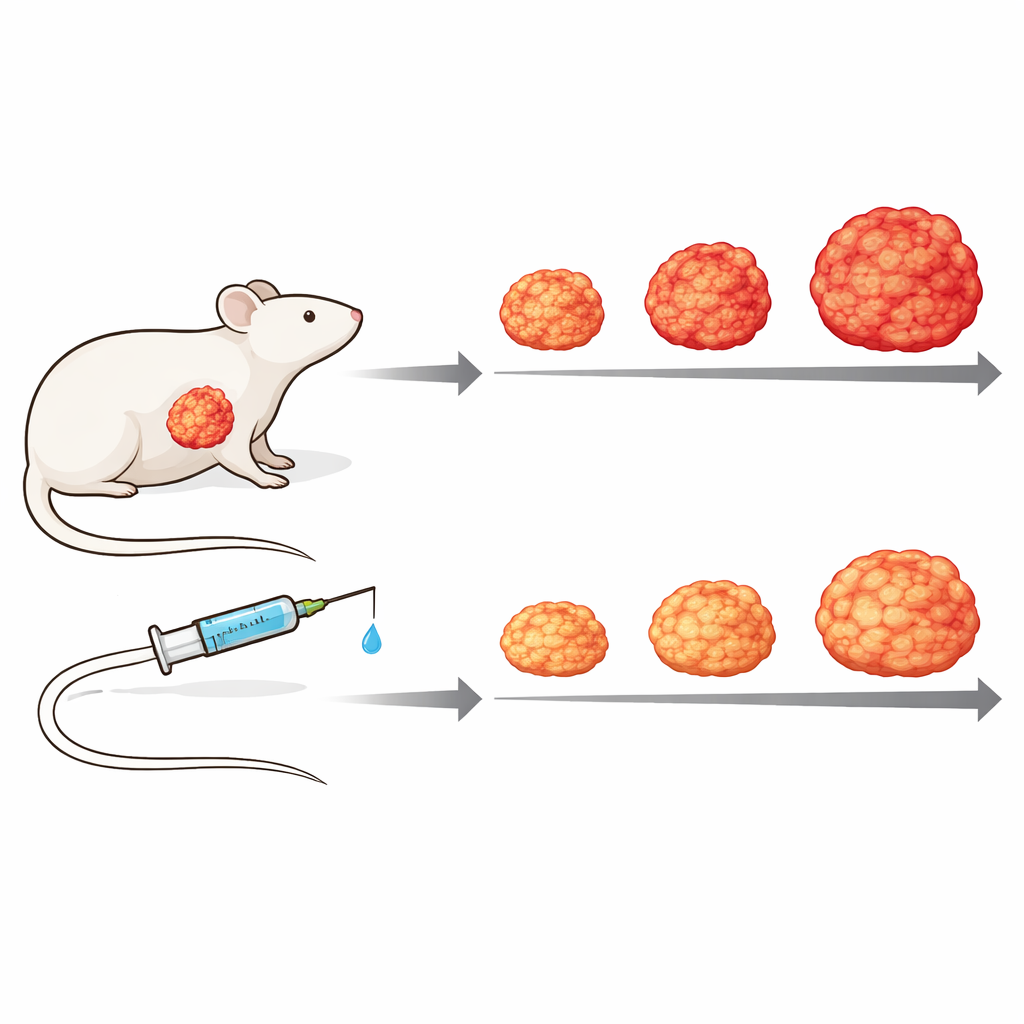
Testando o fármaco em um modelo tumoral vivo
Para imitar mais de perto a complexidade da doença humana, os pesquisadores avançaram para modelos de xenotransplante derivados de pacientes, nos quais pedaços do tumor de uma pessoa são implantados em camundongos imunodeficientes. Usando medições proteicas capazes de distinguir proteínas tumorais humanas das proteínas estromais do camundongo, eles mostraram que o tecido conjuntivo circundante responde de forma diferente dependendo da atividade interna do tumor, ressaltando a importância do diálogo tumor–estroma. Em um desses modelos, o tratamento semanal com Zotatifin desacelerou substancialmente o crescimento tumoral em comparação com camundongos não tratados, sem toxicidade óbvia: os tumores cresceram mais lentamente e permaneceram menores, e os animais tratados mantiveram melhor o peso corporal ao longo do tempo.
O que isso significa para os pacientes
Em termos simples, este trabalho mostra que o colangiocarcinoma intra-hepático não é uma única doença, mas pelo menos dois tipos principais definidos por proteínas com diferentes probabilidades de recorrência após cirurgia. Um teste focado em quatro proteínas poderia ajudar os médicos a identificar pacientes de maior risco que poderiam se beneficiar de acompanhamento mais intensivo ou terapia adicional. Ao mesmo tempo, a descoberta de que ambos os subtipos dependem do fator de tradução EIF4A1, e que seu bloqueio com Zotatifin pode conter o crescimento tumoral em modelos realistas, aponta para uma potencial nova estratégia terapêutica. Embora ensaios clínicos sejam necessários para confirmar segurança e benefício em humanos, este estudo demonstra como o perfil proteico profundo pode refinar o prognóstico e revelar alvos medicamentosos acionáveis em um câncer de difícil tratamento.
Citação: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Palavras-chave: colangiocarcinoma intra-hepático, proteômica do câncer, subtipos tumorais, inibição de EIF4A1, xenotransplante derivado de paciente