Clear Sky Science · fr
Caractérisation protéomique du cholangiocarcinome intra-hépatique identifie des sous-groupes stratifiant le risque et EIF4A1 comme cible thérapeutique
Pourquoi cette étude sur le cancer du foie est importante
Le cholangiocarcinome intra-hépatique est une forme rare mais de plus en plus fréquente de cancer des voies biliaires qui prend naissance à l’intérieur du foie. Il est généralement découvert tard, récidive souvent même après chirurgie, et les cliniciens disposent aujourd’hui de peu d’outils fiables pour prédire quels patients rechuteront ou bénéficieront d’un traitement complémentaire. Cette étude utilise des analyses protéiques de pointe pour classer ces tumeurs en groupes biologiquement distincts et pour mettre au jour une vulnérabilité partagée qui pourrait être ciblée par un nouveau médicament.
Un examen approfondi des protéines dans les tumeurs hépatiques
Les chercheurs ont analysé des échantillons de tumeur et de tissu hépatique non cancéreux adjacent provenant de deux cohortes de patients traités dans des centres médicaux majeurs aux États-Unis et en Allemagne. Plutôt que de se concentrer sur l’ADN ou l’ARN, ils ont quantifié des milliers de protéines dans chaque échantillon en utilisant la spectrométrie de masse avancée, une technologie capable de mesurer simultanément de nombreuses molécules. En comparant les tumeurs au tissu environnant, ils ont observé une réorganisation générale des fonctions cellulaires de base : les zones hépatiques saines étaient enrichies en protéines liées au métabolisme, tandis que les tumeurs contenaient en abondance des protéines associées à la division cellulaire, au traitement de l’ADN et à la matrice fibreuse qui entoure les cellules. Ces différences confirment que la vision au niveau protéique capture des caractéristiques de la maladie invisibles à partir des seules données génétiques.
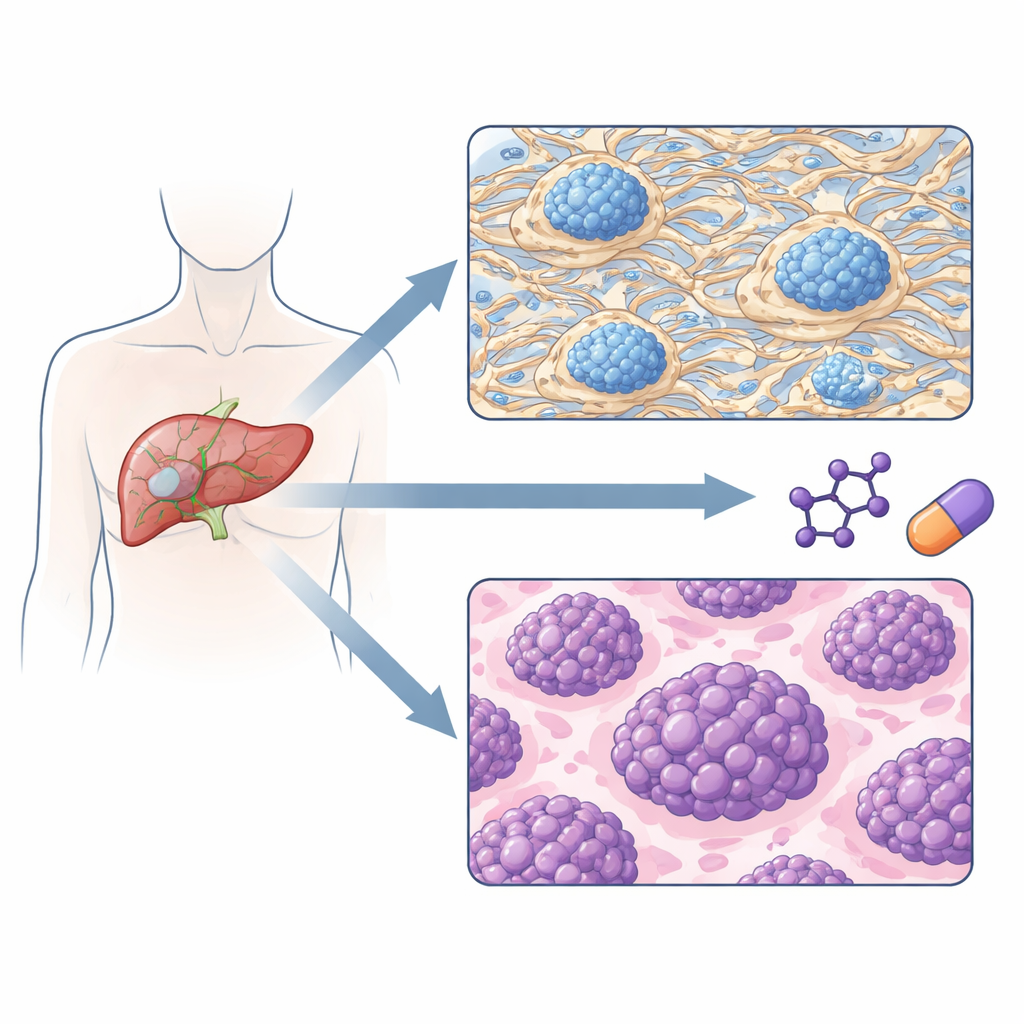
Deux types tumoraux avec des risques de récidive différents
Lorsque l’équipe a regroupé les tumeurs uniquement selon leurs profils protéiques, deux sous-types principaux sont apparus. Un sous-type était dominé par des protéines qui construisent et remodèlent la matrice extracellulaire — l’armature entre les cellules — ainsi que par des composants de la coagulation sanguine et certains signaux immunitaires. L’autre sous-type était dominé par des protéines qui stimulent la réplication de l’ADN, le traitement de l’ARN et la synthèse protéique, autant de signes de cellules à croissance rapide. Fait important, ces deux groupes définis par les protéines présentaient des trajectoires cliniques très différentes : les patients du groupe « riche en matrice » avaient tendance à avoir des tumeurs à un stade plus précoce et restaient beaucoup plus longtemps sans récidive, alors que les patients du groupe « à forte prolifération » rechutaient plus rapidement et présentaient une survie globale plus courte.
Un test simple qui fonctionne dans différentes cohortes
Pour rapprocher ces résultats d’un outil pratique, les chercheurs ont utilisé l’apprentissage automatique pour construire un classificateur basé sur seulement quatre protéines qui différenciaient le mieux les deux sous-types. Ils ont entraîné et testé de nombreuses combinaisons de quatre protéines sur leur série principale de patients et ont constaté que la plupart pouvaient séparer avec précision les sous-groupes. En utilisant l’ensemble le plus performant, ils ont ensuite appliqué ce classificateur à deux collections indépendantes de cholangiocarcinomes intra-hépatiques provenant d’autres hôpitaux, y compris une grande cohorte chinoise précédemment caractérisée au niveau génique et protéique. Dans ces deux cohortes externes, les mêmes deux profils protéomiques sont réapparus, et les patients classés dans le groupe riche en matrice présentaient à nouveau une meilleure évolution que ceux du groupe à forte prolifération. Cela suggère qu’un petit panel protéique pourrait aider les médecins à estimer le risque de récidive dans des populations différentes.
Trouver une cible médicamenteuse commune aux deux sous-types
Au-delà de la prédiction du risque, les scientifiques ont recherché des protéines systématiquement élevées dans les tumeurs des deux groupes et susceptibles d’être ciblées par une thérapie. Un candidat prometteur était EIF4A1, un composant clé de la machinerie cellulaire qui initie la traduction des messages d’ARN en protéines et qui est lié à des voies favorisant le cancer. EIF4A1 était fortement augmenté dans les tumeurs par rapport au tissu hépatique adjacent, indépendamment du sous-type. L’équipe a testé le Zotatifin, un médicament expérimental qui inhibe EIF4A1, sur des lignées cellulaires dérivées de ce cancer et a observé que de faibles doses réduisaient leur viabilité, en particulier lorsqu’elles étaient associées à un inhibiteur d’une autre voie.
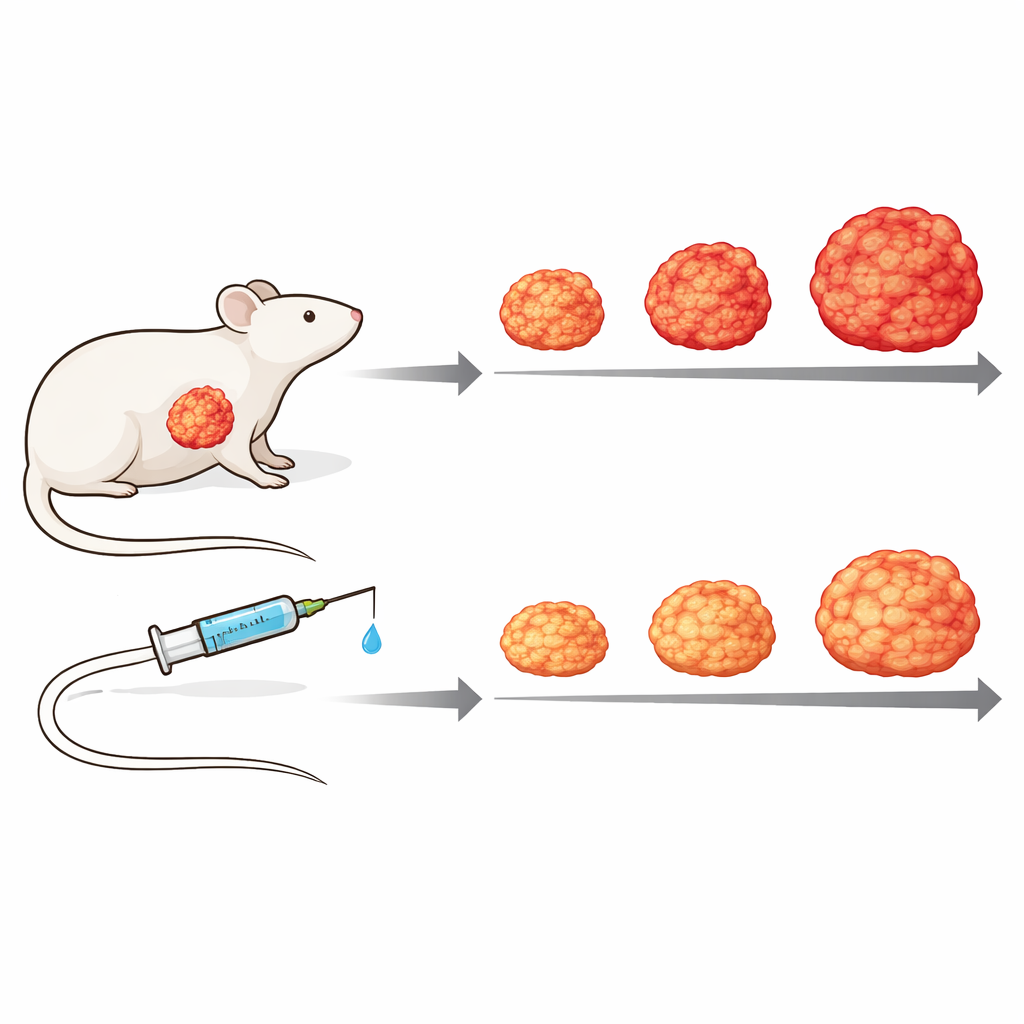
Tester le médicament dans un modèle tumoral vivant
Pour mieux reproduire la complexité de la maladie humaine, les chercheurs sont passés à des modèles de xénogreffes dérivées de patients, dans lesquels des fragments de tumeur humaine sont implantés chez des souris déficientes en immunité. En utilisant des mesures protéiques capables de distinguer les protéines tumorales humaines des protéines stromales murines, ils ont montré que le tissu conjonctif environnant répond différemment selon l’activité interne de la tumeur, soulignant l’importance des interactions tumeur–stroma. Dans l’un de ces modèles, un traitement hebdomadaire par Zotatifin a ralenti de manière substantielle la croissance tumorale par rapport aux souris non traitées, sans toxicité évidente : les tumeurs ont augmenté plus lentement et sont restées plus petites, et les animaux traités ont mieux maintenu leur poids corporel au fil du temps.
Ce que cela signifie pour les patients
En termes simples, ce travail montre que le cholangiocarcinome intra-hépatique n’est pas une maladie unique mais au moins deux types principaux définis par des profils protéiques et présentant des probabilités de récidive différentes après chirurgie. Un test ciblé basé sur quatre protéines pourrait aider les médecins à identifier les patients à risque élevé qui pourraient bénéficier d’un suivi plus intensif ou d’un traitement supplémentaire. Parallèlement, la découverte que les deux sous-types dépendent du facteur de traduction EIF4A1, et que son inhibition par le Zotatifin peut freiner la croissance tumorale dans des modèles réalistes, ouvre la voie à une stratégie thérapeutique potentielle. Des essais cliniques seront nécessaires pour confirmer la sécurité et l’efficacité chez l’homme, mais cette étude illustre comment un profilage protéique approfondi peut à la fois affiner le pronostic et révéler des cibles thérapeutiques exploitables dans un cancer difficile à traiter.
Citation: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Mots-clés: cholangiocarcinome intra-hépatique, protéomique du cancer, sous-types tumoraux, inhibition d’EIF4A1, xénogreffe dérivée de patient