Clear Sky Science · pl
Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target
Dlaczego to badanie raka wątroby ma znaczenie
Rak dróg żółciowych wewnątrzwątrobowy to rzadka, lecz coraz częstsza postać nowotworu dróg żółciowych, rozwijająca się wewnątrz wątroby. Zwykle wykrywany jest późno, często nawraca mimo operacji, a lekarze mają obecnie niewiele pewnych narzędzi, by przewidzieć, którzy pacjenci doświadczą nawrotu lub skorzystają z dodatkowego leczenia. To badanie wykorzystuje zaawansowaną analizę białek, aby podzielić te guzy na biologicznie odrębne grupy i odkryć wspólną słabą stronę, którą można by zaatakować nowym lekiem.
Uważne spojrzenie na białka w guzach wątroby
Naukowcy zbadali próbki guzów i przylegającej niezmienionej tkanki wątroby od dwóch grup pacjentów leczonych w czołowych ośrodkach medycznych w Stanach Zjednoczonych i Niemczech. Zamiast koncentrować się na DNA czy RNA, zmierzyli tysiące białek w każdej próbce za pomocą zaawansowanej spektrometrii mas, technologii zdolnej do jednoczesnej ilościowej analizy wielu molekuł. Porównując guzy z otaczającą tkanką, zaobserwowali szerokie przestawienie podstawowych funkcji komórkowych: zdrowe obszary wątroby były bogatsze w białka związane z metabolizmem, podczas gdy guzy zawierały wiele białek związanych z podziałem komórkowym, obróbką DNA i materiałem włóknistym otaczającym komórki. Te różnice potwierdzają, że spojrzenie na poziomie białek ujawnia cechy choroby, których nie widać wyłącznie na podstawie danych genowych.
Dwa typy guza o różnym ryzyku nawrotu
Gdy zespół pogrupował guzy wyłącznie według wzorców białkowych, wyłoniły się dwa główne podtypy. Jeden podtyp dominowały białka budujące i przebudowujące macierz zewnątrzkomórkową — rusztowanie między komórkami — wraz ze składnikami krzepnięcia krwi i pewnymi sygnałami immunologicznymi. Drugi podtyp dominowały białka napędzające replikację DNA, przetwarzanie RNA i syntezę białek, wszystkie cechy szybko rosnących komórek. Co ważne, te dwie grupy zdefiniowane na podstawie białek miały bardzo odmienne przebiegi kliniczne: pacjenci z grupy „bogatej w macierz” mieli zwykle guzy w wcześniejszych stadiach i znacznie dłużej pozostawali bez nawrotu, podczas gdy pacjenci z grupy „intensywnej proliferacji” nawroty mieli wcześniej i krótsze przeżycie ogólne.
Prosty test działający w różnych grupach pacjentów
Aby przekształcić te obserwacje w coś bliższego praktycznemu narzędziu, badacze użyli uczenia maszynowego do zbudowania klasyfikatora opartego tylko na czterech białkach, które najlepiej rozróżniały oba podtypy. Przeszkolili i przetestowali wiele kombinacji czterech białek na swojej głównej grupie pacjentów i stwierdzili, że większość z nich potrafiła dokładnie oddzielić podgrupy. Używając najlepszego zestawu, zastosowali następnie ten klasyfikator do dwóch niezależnych zbiorów przypadków raka wewnątrzwątrobowego z innych szpitali, w tym dużej chińskiej kohorty wcześniej scharakteryzowanej na poziomie genowym i białkowym. W obu zewnętrznych grupach pojawiły się te same dwa wzorce proteomiczne, a pacjenci przypisani do grupy bogatej w macierz ponownie mieli lepsze rokowania niż ci z grupy proliferacyjnej. To sugeruje, że mały panel białkowy mógłby pomóc lekarzom oszacować ryzyko nawrotu w różnych populacjach.
Poszukiwanie wspólnego celu leku w obu podtypach
Ponad prognozowaniem ryzyka, naukowcy szukali białek stale podwyższonych w guzach obu grup, które mogłyby być podatne na terapię. Obiecującym kandydatem okazał się EIF4A1, kluczowy element maszynerii komórkowej inicjującej tłumaczenie mRNA na białka, powiązany ze ścieżkami sprzyjającymi rozwojowi nowotworu. EIF4A1 był wyraźnie zwiększony w guzach w porównaniu z przylegającą tkanką wątroby, niezależnie od podtypu. Zespół przetestował Zotatifin, eksperymentalny lek blokujący EIF4A1, w liniach komórkowych pochodzących z tego nowotworu i odkrył, że niskie dawki ograniczały ich żywotność, szczególnie w połączeniu z inhibitorem innej ścieżki.
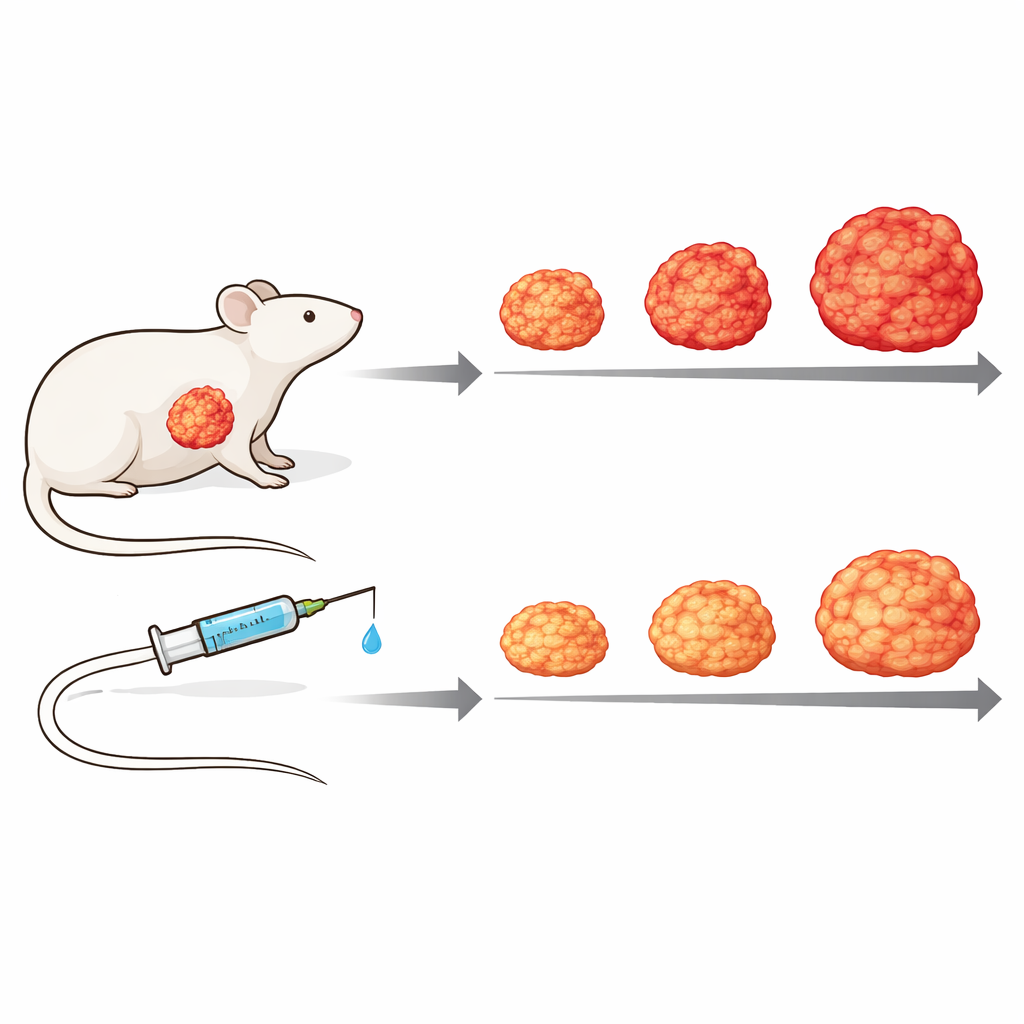
Testowanie leku w modelu żywego guza
Aby lepiej odzwierciedlić złożoność choroby u ludzi, badacze przeszli do modeli xenograftów pochodzących od pacjentów, w których fragmenty guza człowieka są wszczepiane do myszy z niedoborem odporności. Wykorzystując pomiary białkowe pozwalające odróżnić ludzkie białka guza od mysich białek zrębu, pokazali, że otaczająca tkanka łączna reaguje inaczej w zależności od wewnętrznej aktywności guza, co podkreśla wagę komunikacji między guzem a zrębem. W jednym z takich modeli cotygodniowe leczenie Zotatifinem znacznie spowolniło wzrost guza w porównaniu z myszami nieleczonymi, bez wyraźnej toksyczności: guzy rosły wolniej i pozostawały mniejsze, a leczone zwierzęta lepiej utrzymywały masę ciała w czasie.
Co to oznacza dla pacjentów
W prostych słowach, badanie pokazuje, że rak dróg żółciowych wewnątrzwątrobowy nie jest jedną chorobą, lecz co najmniej dwoma głównymi typami zdefiniowanymi przez profil białkowy, o różnych szansach na nawroty po operacji. Skoncentrowany test na cztery białka mógłby pomóc lekarzom zidentyfikować pacjentów o wyższym ryzyku, którzy mogliby skorzystać z intensywniejszej kontroli lub dodatkowego leczenia. Równocześnie odkrycie, że oba podtypy polegają na czynniku translacyjnym EIF4A1 i że jego blokada za pomocą Zotatifinu hamuje wzrost guza w realistycznych modelach, wskazuje na potencjalnie nową strategię leczenia. Choć konieczne będą badania kliniczne, aby potwierdzić bezpieczeństwo i korzyści u ludzi, praca ta pokazuje, jak dogłębne profilowanie białkowe może jednocześnie doprecyzować rokowanie i ujawnić możliwe cele terapeutyczne w trudnym do leczenia nowotworze.
Cytowanie: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Słowa kluczowe: intrahepatic cholangiocarcinoma, cancer proteomics, tumor subtypes, EIF4A1 inhibition, patient-derived xenograft