Clear Sky Science · ar
التحليل البروتيومي لسرطان الأقنية الصفراوية داخل الكبد يحدد مجموعات فرعية مصنّفة حسب المخاطر وEIF4A1 كهدف علاجي
لماذا تهم هذه الدراسة لسرطان الكبد
سرطان الأقنية الصفراوية داخل الكبد هو شكل نادر لكنه يتزايد من سرطانات القناة الصفراوية التي تنشأ داخل الكبد. عادةً ما يُكتشف في مراحل متأخرة، وغالبًا ما يعود حتى بعد الجراحة، ولا تمتلك الأوساط الطبية حاليًا طرقًا موثوقة كثيرة للتنبؤ بمن سيصاب بنكس أو سيستفيد من علاج إضافي. تستخدم هذه الدراسة تحليلاً بروتيوميًا متقدّمًا لتصنيف هذه الأورام إلى مجموعات حيوية مميزة وكشف نقطة ضعف مشتركة قد يمكن استهدافها بدواء جديد.
فحص البروتينات في أورام الكبد عن قرب
فحص الباحثون عينات الأورام والأنسجة الكبدية السليمة المجاورة من مجموعتين من المرضى الذين عولجوا في مراكز طبية كبرى في الولايات المتحدة وألمانيا. بدلاً من التركيز على الحمض النووي أو الحمض النووي الريبي، قاسوا آلاف البروتينات في كل عينة باستخدام طيف الكتلة المتقدم، وهي تقنية يمكنها قياس عدد كبير من الجزيئات دفعة واحدة. بالمقارنة بين الأورام والأنسجة المحيطة، لوحظ إعادة ترتيب واسعة لوظائف الخلية الأساسية: كانت مناطق الكبد السليمة أغنى ببروتينات مرتبطة بالتمثيل الغذائي، في حين أن الأورام كانت مكدسة ببروتينات مرتبطة بانقسام الخلايا، ومعالجة الحمض النووي، والمواد الليفية المحيطة بالخلايا. أكدت هذه الاختلافات أن الرؤية على مستوى البروتين تلتقط خصائص للمرض لا تظهر من بيانات الجينات وحدها.
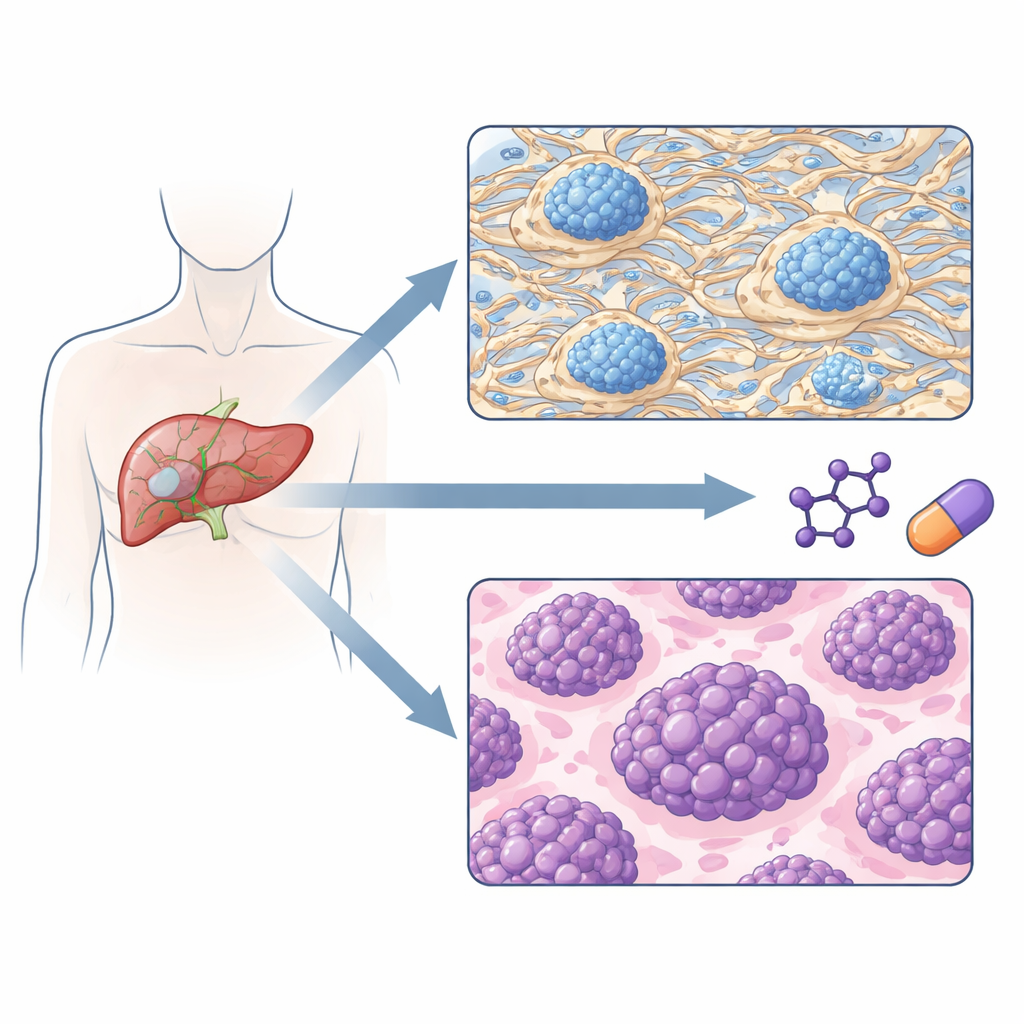
نوعان من الأورام يختلفان في خطر العودة
عندما صنّف الفريق الأورام بناءً على أنماطها البروتينية فقط، ظهرت مجموعتان فرعيتان رئيسيتان. كانت إحدى المجموعات مهيمنة عليها بروتينات تبني وتعيد تشكيل المصفوفة خارج الخلوية—الهيكل بين الخلايا—إلى جانب مكونات تجلط الدم وإشارات مناعية معينة. أما المجموعة الأخرى فكانت مهيمنة عليها بروتينات تحفز تكرار الحمض النووي، ومعالجة الحمض النووي الريبي، وتخليق البروتين، وهي سمات للخلايا سريعة النمو. والأهم أن هاتين المجموعتين المعرفة بروتينيًا سلكتا مسارات سريرية مختلفة: ميالون للمجموعة «الغنية بالمصفوفة» كان لديهم أورام في مراحل أبكر وظلوا لفترة أطول قبل أن يعود السرطان، بينما انتكست مجموعة «المتكاثرة» أسرع وكان لديها بقاء إجمالي أقصر.
اختبار بسيط يعمل عبر مجموعات المرضى
لتحويل هذه الرؤى إلى أداة أقرب للتطبيق العملي، استخدم الباحثون التعلم الآلي لبناء مصنّف يعتمد على أربعة بروتينات فقط تميز بين النوعين بشكل أمثل. دربوا واختبروا مجموعات عديدة مكوّنة من أربعة بروتينات على مجموعة المرضى الرئيسية لديهم ووجدوا أن معظمها يستطيع فصل الفئتين بدقة. باستخدام مجموعة الأداء الأفضل، طبقوا هذا المصنّف على مجموعتين مستقلتين من حالات سرطان الأقنية الصفراوية داخل الكبد من مستشفيات أخرى، بما في ذلك مجموعة صينية كبيرة سبق توصيفها على مستوى الجينات والبروتينات. في كلتا المجموعتين الخارجة، ظهرت نفس النماذج البروتيومية، ومرة أخرى كان أداء المرضى المصنفين في مجموعة الغنية بالمصفوفة أفضل من أولئك في مجموعة التكاثر. يشير ذلك إلى أن لوحة بروتينية صغيرة قد تساعد الأطباء في تقدير خطر النكس عبر مجموعات سكانية مختلفة.
إيجاد هدف دوائي مشترك في كلا النوعين
بعيدًا عن التنبؤ بالمخاطر، بحث العلماء عن بروتينات مرتفعة باستمرار في الأورام من كلا المجموعتين والتي قد تكون قابلة للعلاج. كان أحد المرشحين الواعدين هو EIF4A1، وهو مكوّن رئيسي في آلية الخلية التي تبدأ ترجمة رسائل الحمض النووي الريبي إلى بروتينات ومرتبط بمسارات تعزز السرطان. كان EIF4A1 مرتفعًا بقوة في الأورام مقارنة بالأنسجة الكبدية المجاورة، بغض النظر عن النوع الفرعي. اختبر الفريق زوتاتيفين، وهو دواء تجريبي يعيق EIF4A1، في خطوط خلوية مشتقة من هذا السرطان فوجدوا أن جرعات منخفضة قللت من حيويتها، خصوصًا عند دمجه مع مثبط لممر آخر.
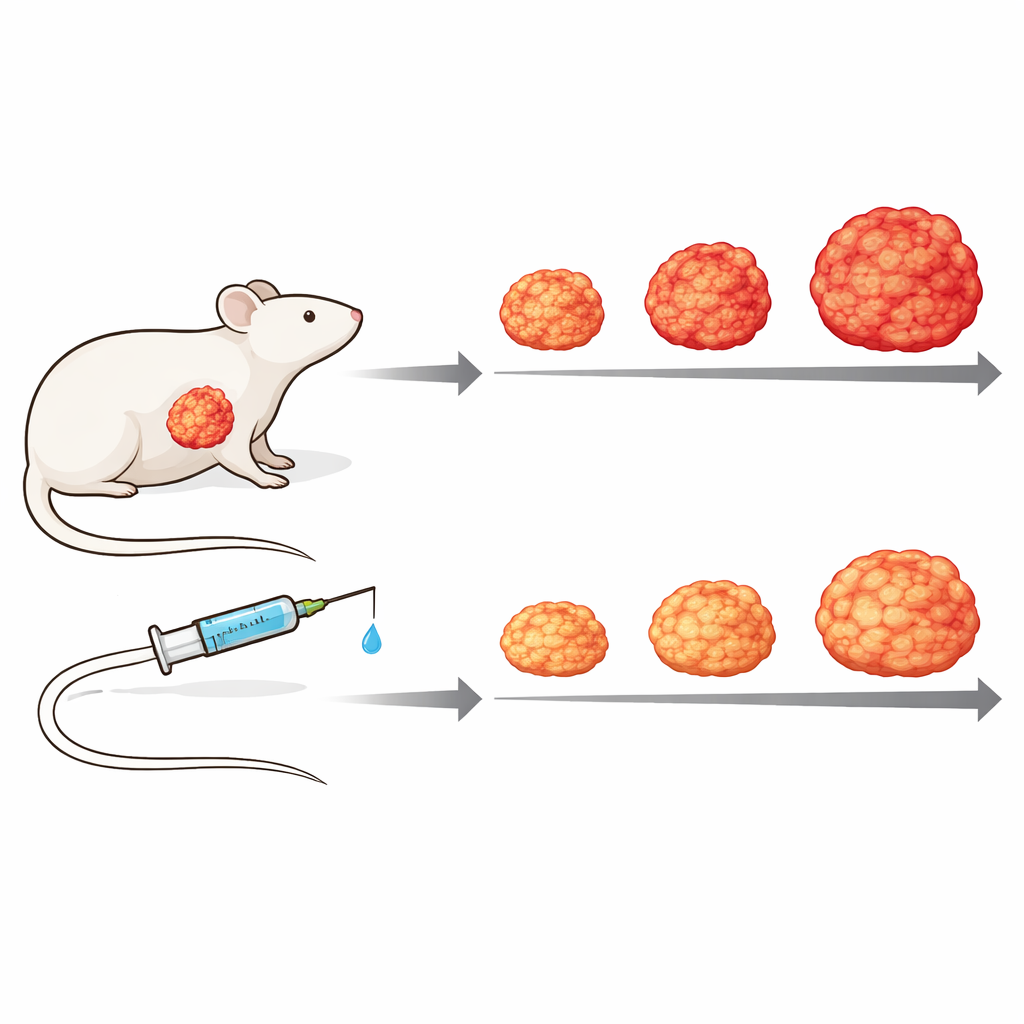
اختبار الدواء في نموذج ورم حي
لمحاكاة تعقيد المرض البشري عن قرب، انتقل الباحثون إلى نماذج زرع مشتق من المريض، حيث تُزرع قطع من ورم شخص في فئران ناقصة المناعة. باستخدام قياسات بروتينية قادرة على تمييز بروتينات الورم البشرية عن بروتينات النسيج الضام الفأرية، أظهروا أن النسيج الضام المحيط يستجيب بشكل مختلف اعتمادًا على النشاط الداخلي للورم، مما يؤكد أهمية التبادل بين الورم والنسج المحيطة به. في أحد هذه النماذج، أدى العلاج الأسبوعي بزوتاتيفين إلى إبطاء نمو الورم بشكل كبير مقارنة بالفئران غير المعالجة، دون سميّة واضحة: نمت الأورام ببطء وبقيت أصغر، وحافظت الحيوانات المعالجة على وزنها أفضل مع مرور الوقت.
ماذا يعني هذا للمرضى
بعبارة بسيطة، تُظهر هذه الدراسة أن سرطان الأقنية الصفراوية داخل الكبد ليس مرضًا واحدًا بل على الأقل نوعان رئيسيان محددان على مستوى البروتين لهما احتمالات مختلفة للعودة بعد الجراحة. قد يساعد اختبار مركز على أربعة بروتينات الأطباء في تحديد المرضى ذوي المخاطر الأعلى الذين قد يستفيدون من متابعة أكثر كثافة أو علاج إضافي. في الوقت نفسه، تشير اكتشافات أن كلا النوعين يعتمدان على عامل الترجمة EIF4A1، وأن حجب هذا العامل بزوتاتيفين يمكن أن يحد من نمو الورم في نماذج قريبة من الواقع، إلى استراتيجية علاجية جديدة محتملة. بينما ستحتاج التجارب السريرية لتأكيد السلامة والفائدة لدى البشر، تُبيّن هذه الدراسة كيف أن التحليل البروتيومي العميق يمكن أن يصقل التنبؤات ويكشف أهداف دوائية قابلة للتطبيق في سرطان يصعب علاجه.
الاستشهاد: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
الكلمات المفتاحية: سرطان الأقنية الصفراوية داخل الكبد, البروتيوميات السرطانية, أنواع الأورام, تثبيط EIF4A1, نموذج زرع مشتق من المريض