Clear Sky Science · de
Proteomische Charakterisierung des intrahepatischen Cholangiokarzinoms identifiziert risikostruatifizierende Subgruppen und EIF4A1 als therapeutisches Ziel
Warum diese Leberkrebsstudie wichtig ist
Das intrahepatische Cholangiokarzinom ist eine seltene, aber zunehmend häufigere Form des Gallengangkrebses, die innerhalb der Leber entsteht. Es wird meist spät entdeckt, tritt oft selbst nach einer Operation wieder auf, und Ärztinnen und Ärzte haben derzeit nur wenige verlässliche Methoden, um vorherzusagen, welche Patientinnen und Patienten rückfällig werden oder von zusätzlicher Behandlung profitieren. Diese Studie nutzt modernste Proteinanalytik, um solche Tumoren in biologisch unterschiedliche Gruppen zu unterteilen und eine gemeinsame Schwachstelle zu identifizieren, die sich mit einem neuen Wirkstoff angreifen lassen könnte.
Proteine in Lebertumoren genau betrachtet
Die Forschenden analysierten Tumorproben und benachbartes nicht-krebserregendes Lebergewebe aus zwei Patientengruppen, die an großen medizinischen Zentren in den USA und Deutschland behandelt wurden. Statt sich auf DNA oder RNA zu konzentrieren, maßen sie Tausende von Proteinen in jeder Probe mithilfe fortschrittlicher Massenspektrometrie — einer Technik, die viele Moleküle gleichzeitig quantifizieren kann. Im Vergleich von Tumoren mit dem umliegenden Gewebe zeigten sich weitreichende Umstellungen grundlegender Zellfunktionen: Gesunde Leberbereiche waren reicher an stoffwechselbezogenen Proteinen, während Tumoren viele Proteine aufwiesen, die mit Zellteilung, DNA-Verarbeitung und der faserigen extrazellulären Matrix verbunden sind. Diese Unterschiede bestätigen, dass die Proteomebene Merkmale der Erkrankung erfasst, die in Genom- oder Transkriptomdaten allein nicht sichtbar sind.
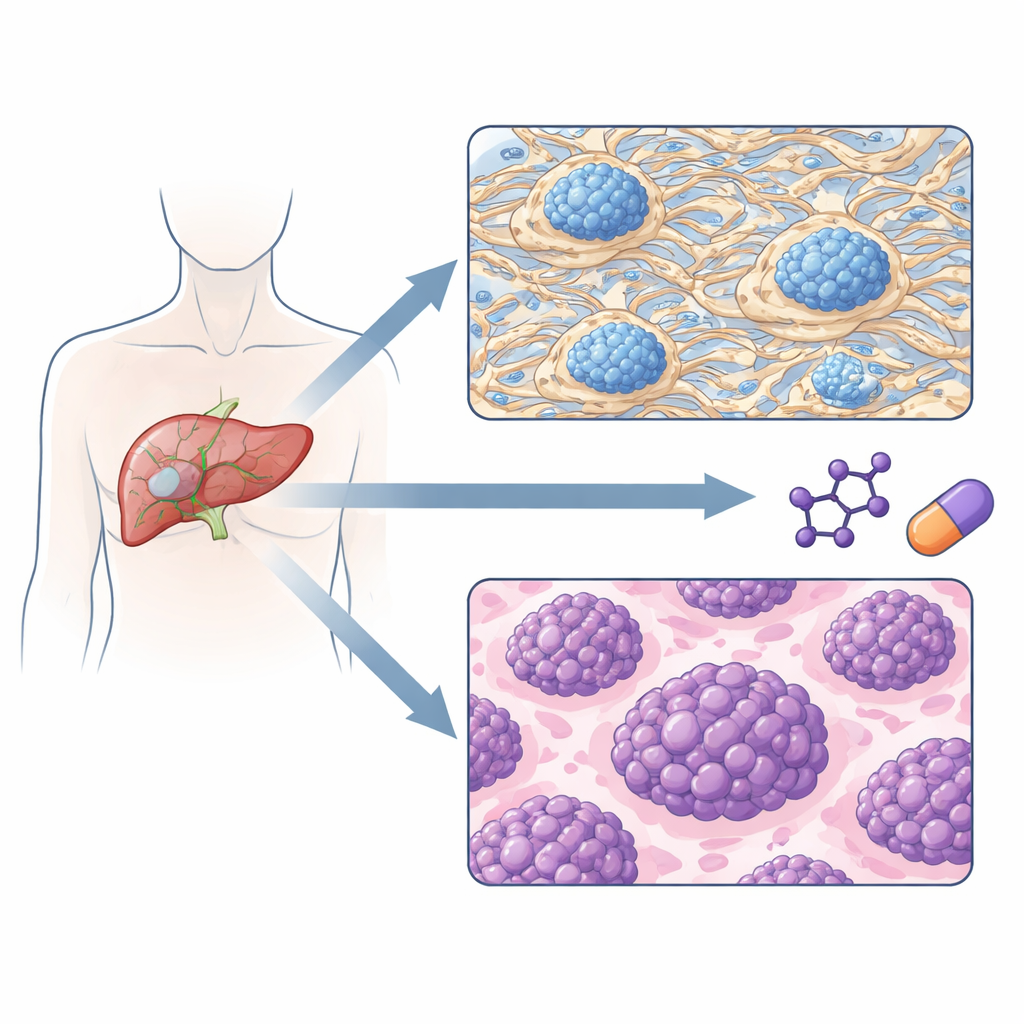
Zwei Tumortypen mit unterschiedlichem Rückfallrisiko
Als das Team die Tumoren allein nach ihren Proteinmustern gruppierte, traten zwei Hauptsubtypen hervor. Ein Subtyp war geprägt von Proteinen, die die extrazelluläre Matrix aufbauen und umgestalten — das Gerüst zwischen den Zellen — sowie von Komponenten der Blutgerinnung und bestimmten Immunmarkern. Der andere Subtyp war dominiert von Proteinen, die DNA-Replikation, RNA-Verarbeitung und Proteinsynthese antreiben — Kennzeichen schnell wachsender Zellen. Wichtig ist, dass diese beiden proteindefinierten Gruppen unterschiedliche klinische Verläufe zeigten: Patientinnen und Patienten der „matrixreichen“ Gruppe hatten tendenziell Tumoren in einem früheren Stadium und blieben deutlich länger tumorfrei, während die „proliferationsstarke“ Gruppe früher rückfällig wurde und eine kürzere Gesamtüberlebenszeit aufwies.
Ein einfacher Test, der in verschiedenen Patientengruppen funktioniert
Um diese Erkenntnisse in ein praktischeres Instrument zu überführen, verwendeten die Forschenden maschinelles Lernen, um einen Klassifikator zu entwickeln, der auf nur vier Proteinen basiert und die beiden Subtypen am besten unterscheidet. Sie trainierten und testeten viele Vier-Protein-Kombinationen an ihrem Hauppatientensatz und fanden, dass die meisten Kombinationen die Untergruppen zuverlässig trennen konnten. Mit dem leistungsstärksten Satz wandten sie den Klassifikator anschließend auf zwei unabhängige Sammlungen von intrahepatischem Cholangiokarzinom aus anderen Krankenhäusern an, darunter eine große chinesische Kohorte, die zuvor auf Gen- und Proteinebene charakterisiert worden war. In beiden externen Gruppen traten dieselben zwei proteomischen Muster wieder auf, und Patientinnen und Patienten, die der matrixreichen Gruppe zugewiesen wurden, schnitten erneut besser ab als jene der proliferationsstarken Gruppe. Das deutet darauf hin, dass ein kleines Proteinpanel Ärztinnen und Ärzten helfen könnte, das Rückfallrisiko in unterschiedlichen Populationen einzuschätzen.
Ein gemeinsames Arzneimittelziel in beiden Subtypen finden
Über die Risikoabschätzung hinaus suchten die Wissenschaftlerinnen und Wissenschaftler nach Proteinen, die in Tumoren beider Gruppen konsistent erhöht waren und sich therapeutisch ansprechen lassen könnten. Ein vielversprechender Kandidat war EIF4A1, ein Schlüsselfaktor in der zellulären Maschinerie, die die Übersetzung von RNA-Botschaften in Proteine initiiert und mit krebsfördernden Signalwegen verknüpft ist. EIF4A1 war in Tumoren im Vergleich zum umliegenden Lebergewebe stark erhöht, unabhängig vom Subtyp. Das Team testete Zotatifin, ein experimentelles Mittel, das EIF4A1 blockiert, in Zelllinien dieses Krebses und stellte fest, dass niedrige Dosen deren Überlebensfähigkeit reduzierten, besonders in Kombination mit einem anderen Signalweg-Inhibitor.
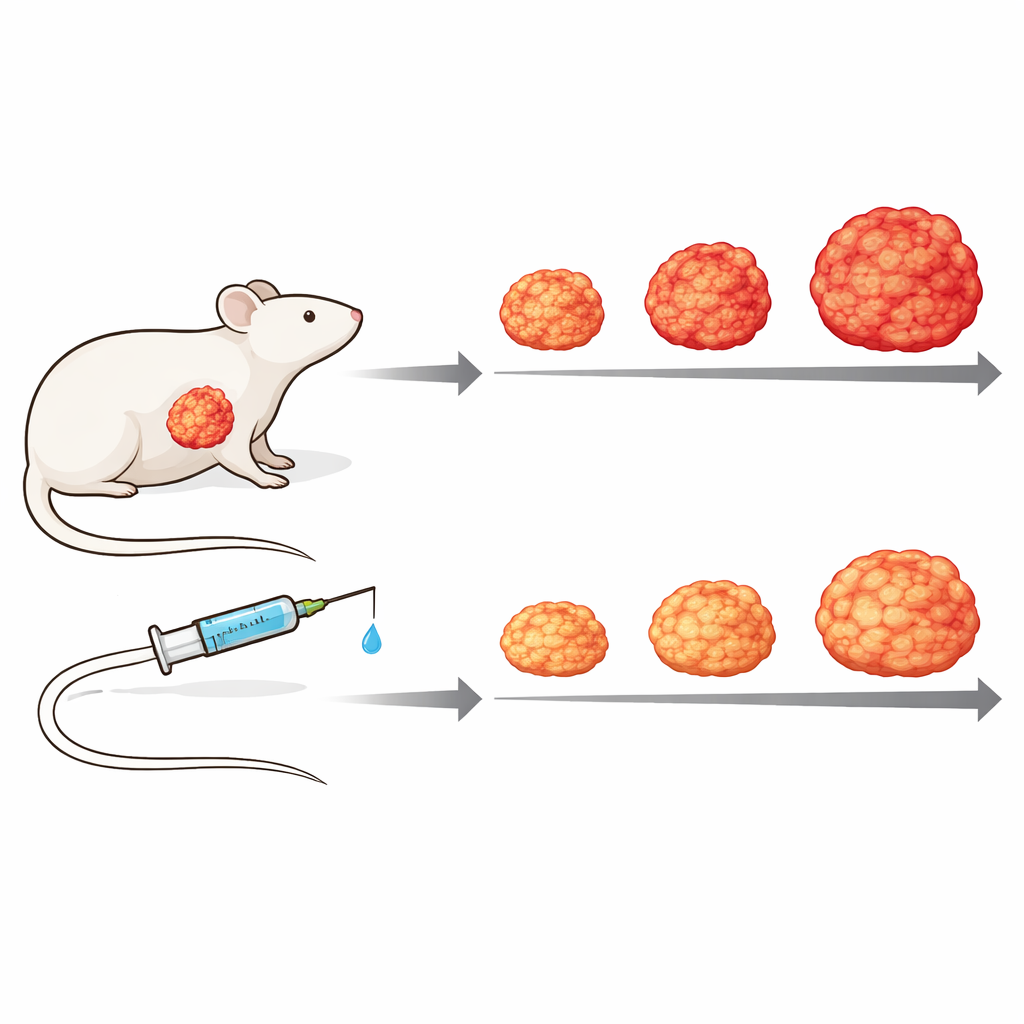
Test des Medikaments in einem lebenden Tumormodell
Um die Komplexität der menschlichen Erkrankung besser abzubilden, wechselten die Forschenden zu patientenabgeleiteten Xenograft-Modellen, bei denen Tumorstücke eines Menschen in immundefiziente Mäuse implantiert werden. Mithilfe von Proteinmessungen, die humane Tumorproteine von Maus-Stroma-Proteinen unterscheiden konnten, zeigten sie, dass das umliegende Bindegewebe je nach innerer Aktivität des Tumors unterschiedlich reagiert — ein Hinweis auf die Bedeutung des Tumor–Stroma-Wechsels. In einem solchen Modell verlangsamte die wöchentliche Behandlung mit Zotatifin das Tumorwachstum deutlich im Vergleich zu unbehandelten Mäusen, ohne erkennbare Toxizität: Tumoren wuchsen langsamer und blieben kleiner, und behandelte Tiere hielten ihr Körpergewicht im Verlauf besser.
Was das für Patientinnen und Patienten bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass das intrahepatische Cholangiokarzinom keine einheitliche Erkrankung ist, sondern mindestens zwei proteindefinierte Haupttypen mit unterschiedlicher Rückfallwahrscheinlichkeit nach einer Operation umfasst. Ein fokussierter Vier-Protein-Test könnte Ärztinnen und Ärzten helfen, Hochrisikopatientinnen und -patienten zu identifizieren, die von intensiverer Nachsorge oder zusätzlicher Therapie profitieren könnten. Gleichzeitig weist die Entdeckung, dass beide Subtypen auf den Translationsfaktor EIF4A1 angewiesen sind und dessen Blockade durch Zotatifin das Tumorwachstum in realistischen Modellen hemmen kann, auf eine potenzielle neue Behandlungsstrategie hin. Klinische Studien werden nötig sein, um Sicherheit und Nutzen beim Menschen zu bestätigen, doch die Studie demonstriert, wie tiefgehende Proteinprofile sowohl Prognose verbessern als auch verwertbare Arzneimittelziele in einem schwer behandelbaren Krebs aufdecken können.
Zitation: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Schlüsselwörter: intrahepatisches Cholangiokarzinom, Krebsproteomik, Tumorsubtypen, EIF4A1-Inhibition, patientenabgeleitetes Xenograft