Clear Sky Science · ru
Протеомная характеристика внутрипечёночной холангиокарциномы выявляет подгруппы с разным риском и EIF4A1 как терапевтическую мишень
Почему это исследование рака печени важно
Внутрипечёночная холангиокарцинома — редкая, но становящаяся всё более распространённой форма рака желчных протоков, развивающаяся внутри печени. Обычно её обнаруживают на поздних стадиях, часто опухоль рецидивирует даже после операции, и у врачей пока мало надёжных средств предсказать, у каких пациентов произойдёт рецидив или кто получит пользу от дополнительного лечения. В этом исследовании применили современные методы анализа белков, чтобы разделить эти опухоли на биологически разные группы и выявить общую уязвимость, которую можно было бы атаковать новым лекарством.
Внимательное изучение белков в опухолях печени
Исследователи проанализировали образцы опухолей и близкой некопченой печёночной ткани у двух групп пациентов, лечившихся в крупных медицинских центрах США и Германии. Вместо того чтобы сосредотачиваться на ДНК или РНК, они измерили тысячи белков в каждом образце с помощью современной масс-спектрометрии — технологии, способной количественно оценивать множество молекул одновременно. Сравнивая опухоли с окружающей тканью, они обнаружили широкую перенастройку базовых клеточных функций: в здоровых участках печени доминировали белки, связанные с обменом веществ, тогда как в опухолях было много белков, ассоциированных с делением клеток, обработкой ДНК и внеклеточным матриксом. Эти различия подтвердили, что уровень белков даёт информацию о болезни, которая не видна при анализе генов.
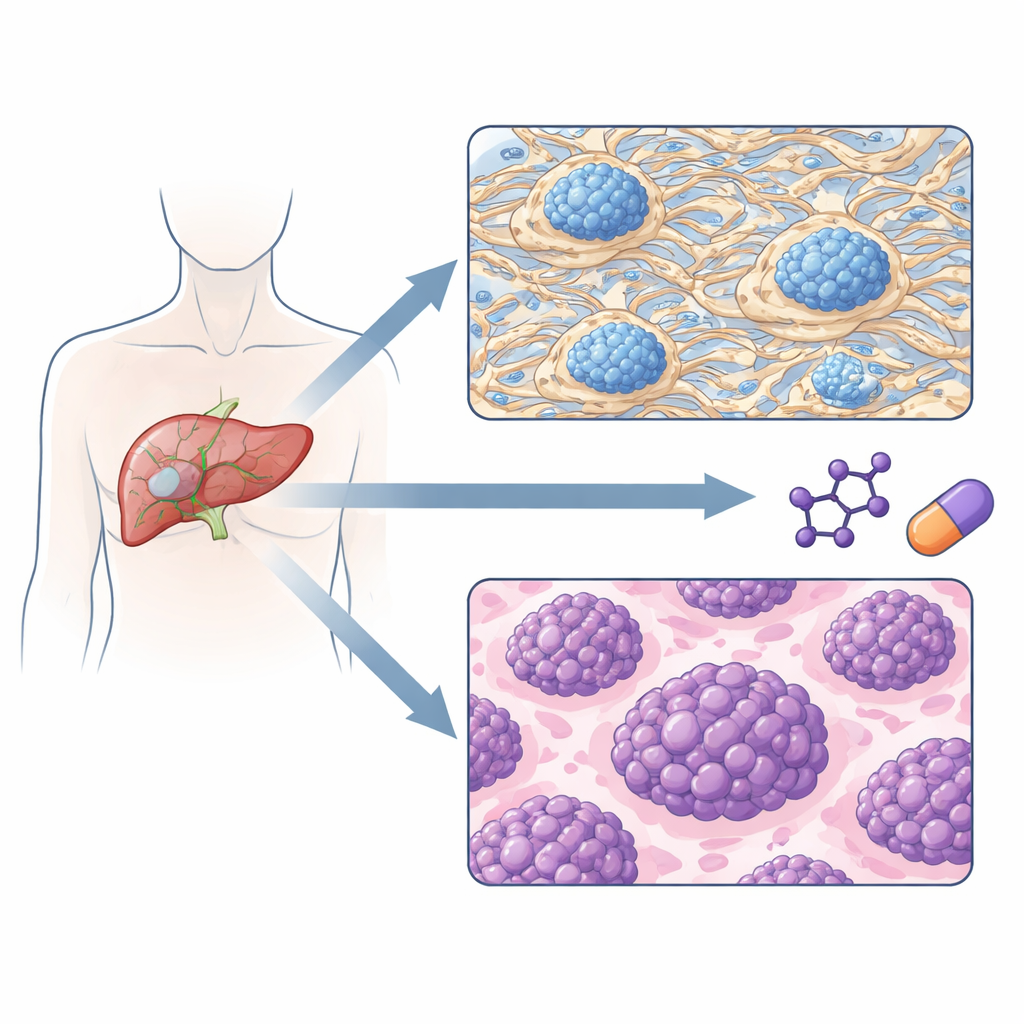
Два типа опухолей с разным риском рецидива
Когда команда сгруппировала опухоли исключительно по протеиновым профилям, выявились два основных подтипа. Один подтип был связан преимущественно с белками, формирующими и ремоделирующими внеклеточный матрикс — «каркас» между клетками — а также с компонентами свертывания крови и определёнными иммунными сигналами. Другой подтип характеризовался преобладанием белков, запускающих репликацию ДНК, обработку РНК и синтез белков — признаков быстрорастущих клеток. Что важно, эти две группы, определённые по белкам, имели очень разное клиническое течение: пациенты из «обогащённой матриксом» группы как правило имели опухоли на более ранних стадиях и дольше оставались без рецидива, тогда как пациенты из «пролиферативной» группы рецидивировали раньше и имели меньше общей выживаемости.
Простой тест, работающий в разных группах пациентов
Чтобы приблизить результаты к практическому инструментарю, исследователи с помощью машинного обучения создали классификатор, основанный всего на четырёх белках, которые наилучшим образом различали два подтипа. Они обучали и тестировали множество четырёхбелковых комбинаций на основной выборке пациентов и обнаружили, что большинство из них достаточно точно разделяют подгруппы. Используя наиболее удачную комбинацию, они затем применили этот классификатор к двум независимым коллекциям внутрипечёночной холангиокарциномы из других клиник, включая большую китайскую когорту, ранее охарактеризованную на уровне генов и белков. В обеих внешних группах те же два протеомных паттерна снова проявились, и пациенты, отнесённые к группе с богатым матриксом, вновь имели лучший прогноз, чем пациенты из пролиферативной группы. Это говорит о том, что небольшой панельный белковый тест может помочь врачам оценивать риск рецидива в разных популяциях.
Поиск общей лекарственной мишени в обоих подтипах
Кроме прогнозирования риска, учёные искали белки, которые последовательно повышены в опухолях обоих групп и могли бы быть доступны для терапии. Одним из перспективных кандидатов оказался EIF4A1 — ключевой компонент клеточного аппарата, запускающего трансляцию РНК в белки, связанный с путями, способствующими онкогенности. EIF4A1 был значительно повышен в опухолях по сравнению с прилежащей печёночной тканью, независимо от подтипа. Команда протестировала Zotatifin, экспериментальное лекарство, блокирующее EIF4A1, на клеточных линиях, полученных из этой опухоли, и обнаружила, что низкие дозы снижают их жизнеспособность, особенно в сочетании с ингибитором другого пути.
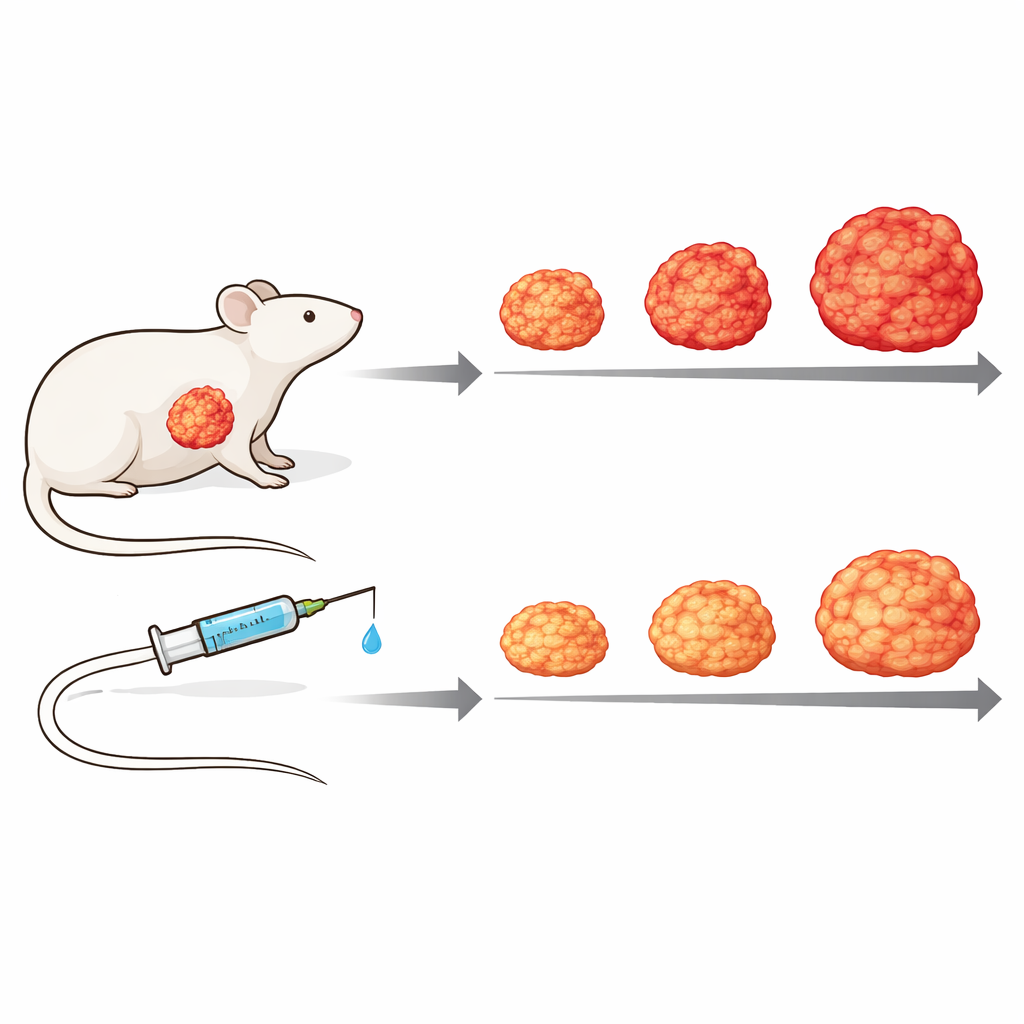
Испытание препарата в модели живой опухоли
Чтобы лучше отразить сложность человеческой болезни, исследователи перешли к моделям ксенотрансплантатов пациента, в которых фрагменты опухоли человека имплантируют иммунодефицитным мышам. С помощью протеиновых измерений, позволяющих различать человеческие опухолевые белки и белки мышиного стромы, они показали, что окружающая соединительная ткань реагирует по-разному в зависимости от внутренней активности опухоли, подчёркивая важность взаимодействия опухоли со стромой. В одной из таких моделей еженедельное лечение Zotatifin заметно замедляло рост опухоли по сравнению с нелечёными мышами без явной токсичности: опухоли росли медленнее и оставались меньшими, а лечёные животные лучше сохраняли вес с течением времени.
Что это значит для пациентов
Проще говоря, работа показывает, что внутрипечёночная холангиокарцинома не является единым заболеванием, а по крайней мере представляет два основных протеиномных типа с разной вероятностью рецидива после операции. Фокусированный тест из четырёх белков мог бы помочь врачам выявлять пациентов с более высоким риском, которые могут получить пользу от усиленного наблюдения или дополнительной терапии. Одновременно открытие того, что оба подтипа зависят от фактора трансляции EIF4A1, и что его блокада с помощью Zotatifin может сдерживать рост опухоли в реалистичных моделях, указывает на потенциальную новую стратегию лечения. Хотя для подтверждения безопасности и эффективности у людей потребуются клинические испытания, это исследование демонстрирует, как глубокое протеомное профилирование может уточнять прогноз и выявлять практически применимые лекарственные мишени в трудно поддающемся лечению раке.
Цитирование: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Ключевые слова: внутрипечёночная холангиокарцинома, раковая протеомика, подтипы опухолей, ингибирование EIF4A1, ксенотрансплантат пациента