Clear Sky Science · it
Caratterizzazione proteomica del colangiocarcinoma intraepatico identifica sottogruppi stratificanti il rischio e EIF4A1 come bersaglio terapeutico
Perché questo studio sul cancro al fegato è importante
Il colangiocarcinoma intraepatico è una forma rara ma in aumento del tumore delle vie biliari che origina all’interno del fegato. Viene di solito scoperto in fase avanzata, spesso recidiva anche dopo intervento chirurgico, e i medici hanno attualmente pochi strumenti affidabili per prevedere quali pazienti andranno incontro a recidiva o trarranno beneficio da terapie aggiuntive. Questo studio utilizza analisi proteiche all’avanguardia per classificare questi tumori in gruppi biologicamente distinti e per individuare una vulnerabilità condivisa che potrebbe essere bersaglio di un nuovo farmaco.
Uno sguardo ravvicinato alle proteine nei tumori epatici
I ricercatori hanno esaminato campioni tumorali e tessuto epatico non canceroso adiacente provenienti da due gruppi di pazienti trattati in grandi centri medici negli Stati Uniti e in Germania. Invece di concentrarsi su DNA o RNA, hanno misurato migliaia di proteine in ciascun campione usando spettrometria di massa avanzata, una tecnologia capace di quantificare contemporaneamente molte molecole. Confrontando i tumori con il tessuto circostante, hanno osservato un ampio riorientamento delle funzioni cellulari di base: le aree epatiche sane risultavano più ricche di proteine legate al metabolismo, mentre i tumori erano pieni di proteine associate alla divisione cellulare, alla gestione del DNA e alla matrice fibrosa che circonda le cellule. Queste differenze confermano che la prospettiva a livello proteico cattura aspetti della malattia non evidenziabili solo dai dati genomici.
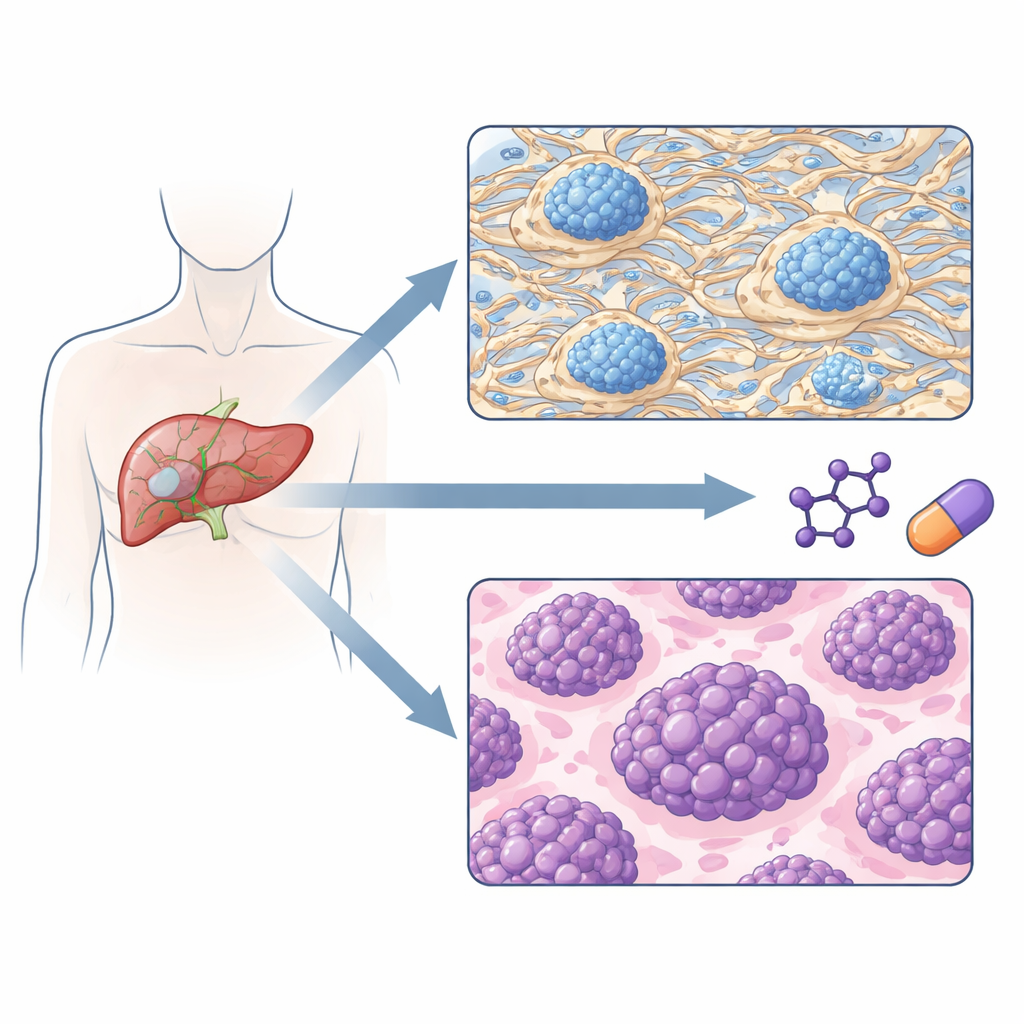
Due tipi tumorali con rischi diversi di recidiva
Quando il team ha raggruppato i tumori esclusivamente in base ai loro pattern proteici, sono emersi due sottotipi principali. Un sottotipo era dominato da proteine che costruiscono e rimodellano la matrice extracellulare—l’impalcatura tra le cellule—insieme a componenti della coagulazione e a alcuni segnali immunitari. L’altro sottotipo era dominato da proteine che guidano la replicazione del DNA, l’elaborazione dell’RNA e la sintesi proteica, tutti tratti distintivi di cellule a rapida crescita. È rilevante che questi due gruppi definiti dalle proteine avessero corsi clinici molto diversi: i pazienti nel gruppo “ricco di matrice” tendevano ad avere tumori in stadio più precoce e hanno impiegato molto più tempo prima della recidiva, mentre i pazienti nel gruppo “ad alta proliferazione” recidivavano prima e presentavano una sopravvivenza globale più breve.
Un test semplice che funziona tra diverse coorti
Per tradurre queste intuizioni in qualcosa di più vicino a uno strumento pratico, i ricercatori hanno usato l’apprendimento automatico per costruire un classificatore basato su appena quattro proteine che distinguono al meglio i due sottotipi. Hanno addestrato e testato molte combinazioni di quattro proteine sul loro set principale di pazienti e hanno trovato che la maggior parte riusciva a separare con precisione i sottogruppi. Utilizzando il set con le migliori prestazioni, hanno poi applicato questo classificatore a due raccolte indipendenti di colangiocarcinoma intraepatico provenienti da altri ospedali, inclusa una grande coorte cinese precedentemente caratterizzata a livello genico e proteico. In entrambe le coorti esterne sono riapparsi gli stessi due pattern proteomici, e i pazienti assegnati al gruppo ricco di matrice hanno nuovamente avuto esiti migliori rispetto a quelli del gruppo ad alta proliferazione. Ciò suggerisce che un piccolo pannello proteico potrebbe aiutare i clinici a stimare il rischio di recidiva in popolazioni diverse.
Individuare un bersaglio farmacologico comune a entrambi i sottotipi
Oltre alla predizione del rischio, gli scienziati hanno cercato proteine costantemente elevate nei tumori di entrambi i gruppi e suscettibili di intervento terapeutico. Un candidato promettente è risultato EIF4A1, una componente chiave della macchina cellulare che avvia la traduzione dei messaggi di RNA in proteine ed è collegata a vie promuoventi il cancro. EIF4A1 risultava fortemente aumentata nei tumori rispetto al tessuto epatico circostante, indipendentemente dal sottotipo. Il team ha testato Zotatifin, un farmaco sperimentale che blocca EIF4A1, in linee cellulari derivate da questo tumore e ha trovato che dosi basse ne riducevano la vitalità, soprattutto se combinate con un altro inibitore di via di segnalazione.
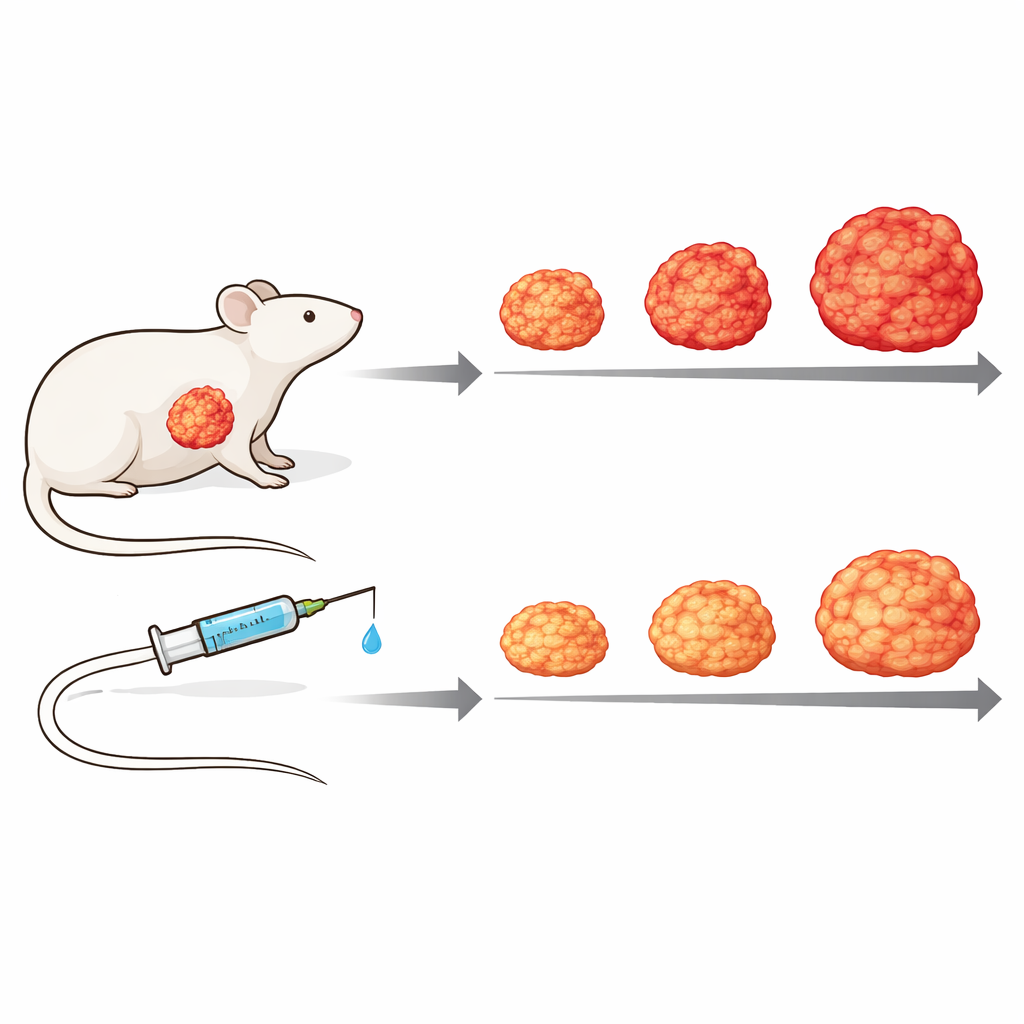
Testare il farmaco in un modello tumorale vivo
Per avvicinarsi maggiormente alla complessità della malattia umana, i ricercatori sono passati a modelli di xenotrapianto derivati da pazienti, in cui frammenti del tumore di una persona vengono impiantati in topi immunodeficienti. Usando misure proteiche in grado di distinguere le proteine tumorali umane da quelle stromali murine, hanno mostrato che il tessuto connettivo circostante risponde in modo diverso a seconda dell’attività interna del tumore, sottolineando l’importanza del dialogo tumore–stroma. In uno di questi modelli, il trattamento settimanale con Zotatifin ha rallentato sostanzialmente la crescita tumorale rispetto ai topi non trattati, senza tossicità evidente: i tumori crescevano più lentamente e restavano più piccoli, e gli animali trattati mantenevano meglio il peso corporeo nel tempo.
Cosa significa questo per i pazienti
In termini chiari, questo lavoro mostra che il colangiocarcinoma intraepatico non è una singola malattia ma almeno due tipi principali definiti a livello proteico con diverse probabilità di recidiva dopo chirurgia. Un test mirato basato su quattro proteine potrebbe aiutare i medici a identificare i pazienti a rischio più elevato che potrebbero beneficiare di un follow-up più intensivo o di terapie aggiuntive. Allo stesso tempo, la scoperta che entrambi i sottotipi dipendono dal fattore di traduzione EIF4A1, e che il suo blocco con Zotatifin può limitare la crescita tumorale in modelli realistici, indica una potenziale nuova strategia terapeutica. Sebbene saranno necessari studi clinici per confermare sicurezza e beneficio negli esseri umani, questo studio dimostra come un’analisi proteomica profonda possa affinare la prognosi e rivelare bersagli farmacologici aggredibili in un tumore difficile da trattare.
Citazione: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Parole chiave: colangiocarcinoma intraepatico, proteomica del cancro, sottotipi tumorali, inibizione di EIF4A1, xenotrapianto derivato dal paziente