Clear Sky Science · es
Caracterización proteómica del colangiocarcinoma intrahepático identifica subgrupos estratificadores de riesgo y EIF4A1 como diana terapéutica
Por qué importa este estudio sobre el cáncer de hígado
El colangiocarcinoma intrahepático es una forma rara pero cada vez más común de cáncer de las vías biliares que se origina dentro del hígado. Suele detectarse en estadios avanzados, con frecuencia reaparece incluso tras la cirugía, y los médicos disponen actualmente de pocas formas fiables para predecir qué pacientes recaerán o se beneficiarán de tratamientos adicionales. Este estudio emplea análisis proteómicos de última generación para clasificar estos tumores en grupos biológicamente distintos y descubrir una vulnerabilidad común que podría dirigirse con un nuevo fármaco.
Mirando de cerca las proteínas en tumores hepáticos
Los investigadores examinaron muestras tumorales y tejido hepático no canceroso adyacente de dos cohortes de pacientes tratados en centros médicos importantes de Estados Unidos y Alemania. En lugar de centrarse en ADN o ARN, midieron miles de proteínas en cada muestra mediante espectrometría de masas avanzada, una técnica capaz de cuantificar muchos moléculas a la vez. Al comparar los tumores con el tejido circundante, observaron un amplio reordenamiento de funciones celulares básicas: las zonas hepáticas sanas eran más ricas en proteínas relacionadas con el metabolismo, mientras que los tumores acumulaban proteínas asociadas a la división celular, el manejo del ADN y la matriz fibrosa que rodea a las células. Estas diferencias confirmaron que la visión a nivel proteico captura rasgos de la enfermedad que no pueden verse solo con datos genéticos.
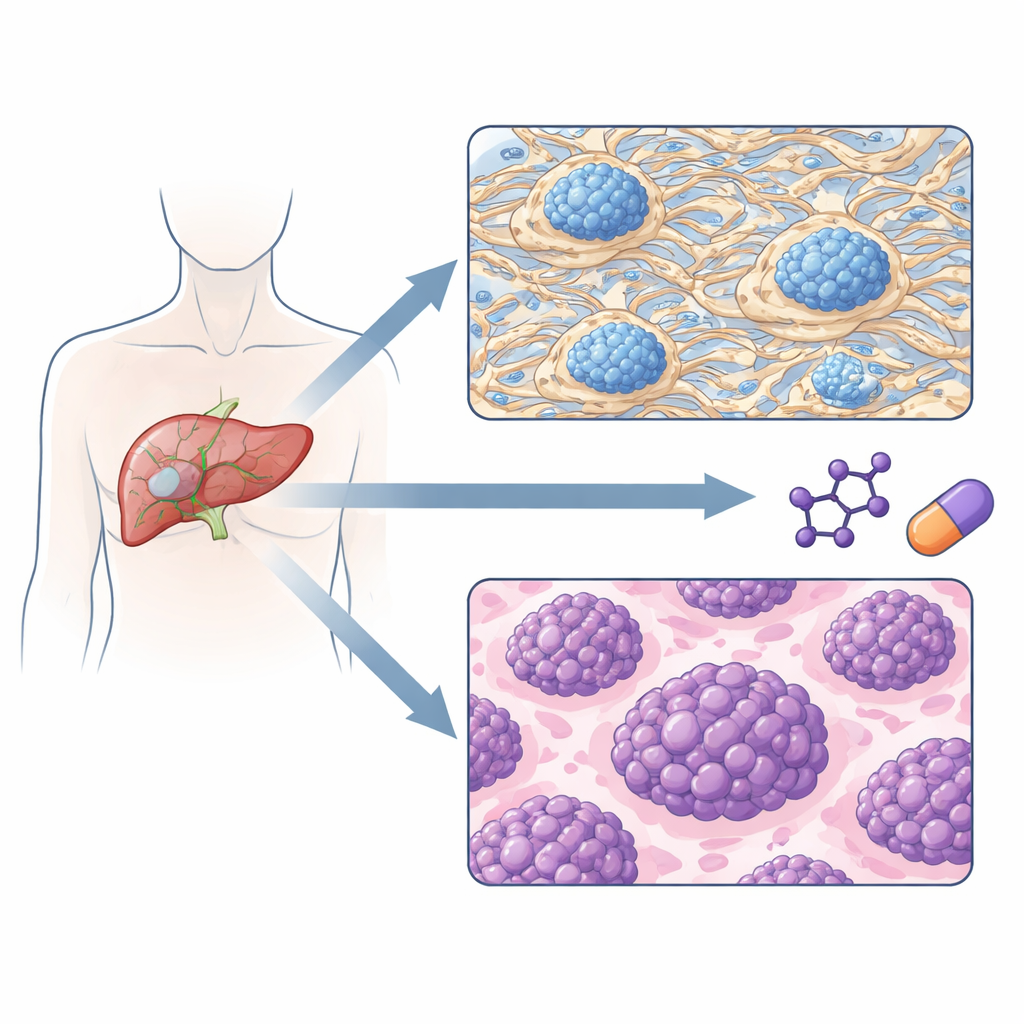
Dos tipos tumorales con distinto riesgo de recurrencia
Cuando el equipo agrupó los tumores únicamente por sus patrones proteicos, surgieron dos subtipos principales. Un subtipo estaba dominado por proteínas que construyen y remodelan la matriz extracelular—el andamiaje entre células—junto con componentes de la coagulación y ciertas señales inmunitarias. El otro subtipo estaba dominado por proteínas que impulsan la replicación del ADN, el procesamiento del ARN y la síntesis de proteínas, marcadores de células de rápido crecimiento. Es importante destacar que estos dos grupos definidos por la proteómica seguían cursos clínicos muy diferentes: los pacientes del grupo «rico en matriz» tendían a presentar tumores en estadios más tempranos y tardaban mucho más en experimentar una recaída, mientras que los del grupo «proliferativo» recaían antes y tenían una supervivencia global más corta.
Una prueba sencilla que funciona en distintas cohortes
Para convertir estos hallazgos en algo más cercano a una herramienta práctica, los investigadores usaron aprendizaje automático para construir un clasificador basado en solo cuatro proteínas que distinguían mejor los dos subtipos. Entrenaron y probaron muchas combinaciones de cuatro proteínas en su conjunto principal de pacientes y encontraron que la mayoría podían separar con precisión los subgrupos. Con el mejor conjunto, aplicaron luego este clasificador a dos colecciones independientes de colangiocarcinoma intrahepático de otros hospitales, incluida una gran cohorte china previamente caracterizada a niveles genómico y proteómico. En ambos grupos externos reaparecieron los mismos dos patrones proteómicos, y los pacientes asignados al grupo rico en matriz volvieron a presentar mejor pronóstico que los del grupo proliferativo. Esto sugiere que un panel reducido de proteínas podría ayudar a los médicos a estimar el riesgo de recaída en distintas poblaciones.
Encontrando una diana farmacológica común en ambos subtipos
Más allá de la predicción de riesgo, los científicos buscaron proteínas consistentemente elevadas en tumores de ambos grupos y que pudieran ser susceptibles de tratamiento. Un candidato prometedor fue EIF4A1, un componente clave de la maquinaria celular que inicia la traducción de los mensajes de ARN en proteínas y que está vinculado a vías promotoras del cáncer. EIF4A1 se encontró fuertemente aumentado en los tumores frente al tejido hepático cercano, independientemente del subtipo. El equipo probó Zotatifin, un fármaco experimental que bloquea EIF4A1, en líneas celulares derivadas de este cáncer y observó que dosis bajas redujeron su viabilidad, especialmente cuando se combinaban con un inhibidor de otra vía.
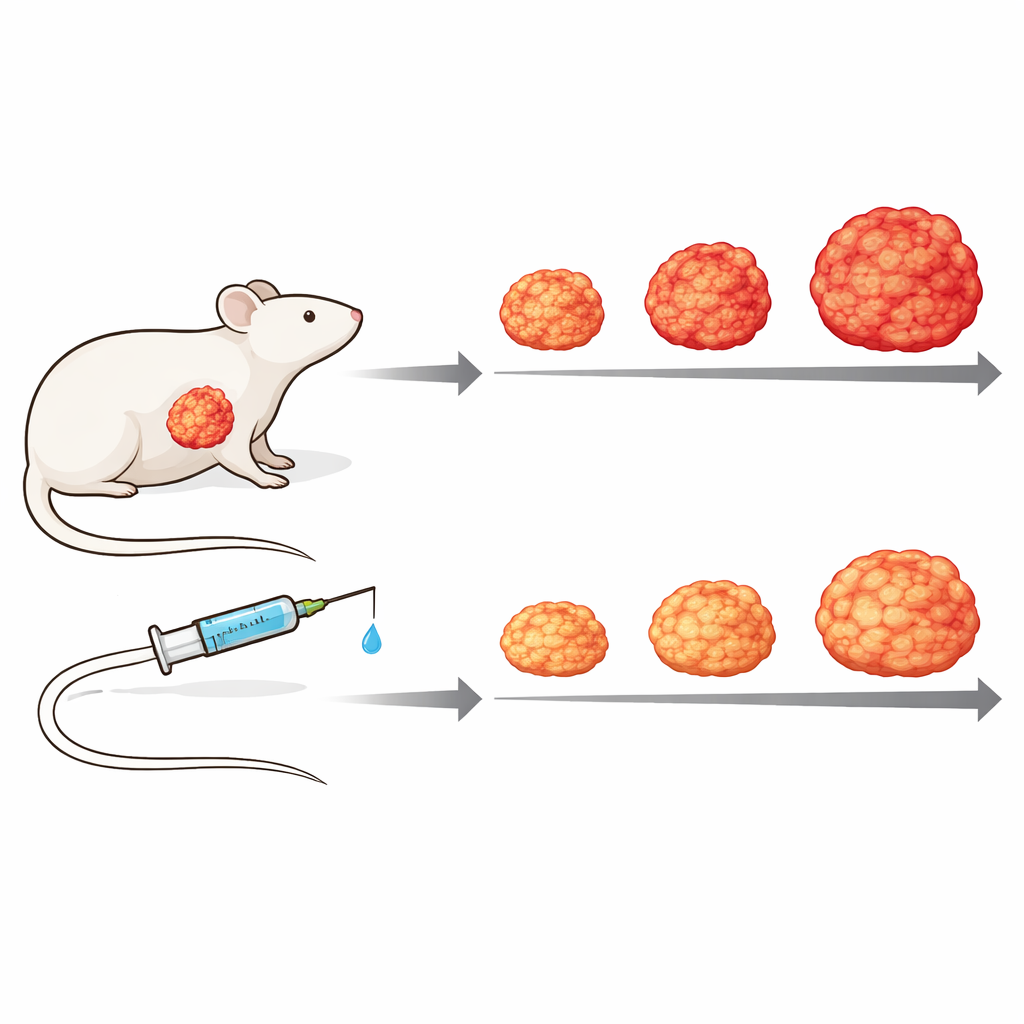
Probando el fármaco en un modelo tumoral vivo
Para reproducir con mayor fidelidad la complejidad de la enfermedad humana, los investigadores avanzaron a modelos de xenoinjertos derivados de pacientes, en los que fragmentos del tumor humano se implantan en ratones inmunodeficientes. Usando mediciones proteicas que pueden distinguir proteínas tumorales humanas de proteínas del estroma murino, demostraron que el tejido conectivo circundante responde de forma distinta según la actividad interna del tumor, subrayando la importancia del diálogo tumor–estroma. En uno de estos modelos, el tratamiento semanal con Zotatifin ralentizó sustancialmente el crecimiento tumoral en comparación con ratones no tratados, sin toxicidad evidente: los tumores crecieron más despacio y se mantuvieron más pequeños, y los animales tratados conservaron mejor su peso corporal a lo largo del tiempo.
Qué significa esto para los pacientes
En términos sencillos, este trabajo muestra que el colangiocarcinoma intrahepático no es una sola enfermedad, sino al menos dos tipos principales definidos por su proteoma y con distintas probabilidades de reaparecer tras la cirugía. Una prueba focalizada de cuatro proteínas podría ayudar a identificar a pacientes de mayor riesgo que podrían beneficiarse de un seguimiento más intensivo o de terapias adicionales. Al mismo tiempo, el descubrimiento de que ambos subtipos dependen del factor de traducción EIF4A1, y que su bloqueo con Zotatifin puede frenar el crecimiento tumoral en modelos realistas, apunta a una posible nueva estrategia terapéutica. Aunque serán necesarios ensayos clínicos para confirmar seguridad y beneficio en humanos, este estudio demuestra cómo el perfilado proteómico profundo puede refinar el pronóstico y descubrir dianas farmacológicas accionables en un cáncer difícil de tratar.
Cita: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Palabras clave: colangiocarcinoma intrahepático, proteómica del cáncer, subtipos tumorales, inhibición de EIF4A1, xenoinjerto derivado del paciente