Clear Sky Science · sv
Proteomisk karaktärisering av intrahepatisk kolangiokarcinom identifierar riskstratifierande undergrupper och EIF4A1 som ett terapeutiskt mål
Varför denna levercancerstudie är viktig
Intrahepatisk kolangiokarcinom är en ovanlig men allt vanligare form av gallgångscancer som uppstår inuti levern. Den upptäcks ofta sent, recidiverar frekvent även efter operation, och läkare har idag få pålitliga metoder för att förutsäga vilka patienter som kommer att få återfall eller dra nytta av ytterligare behandling. Denna studie använder avancerad proteinanalyser för att dela upp dessa tumörer i biologiskt distinkta grupper och för att avslöja en gemensam sårbarhet som skulle kunna riktas med ett nytt läkemedel.
Närstudie av proteiner i levertumörer
Forskarna undersökte tumörprover och närliggande icke‑cancerös levervävnad från två patientgrupper som behandlats vid stora medicinska centrum i USA och Tyskland. Istället för att fokusera på DNA eller RNA mätte de tusentals proteiner i varje prov med hjälp av avancerad masspektrometri, en teknik som kan kvantifiera många molekyler samtidigt. Genom att jämföra tumörer med omgivande vävnad såg de en omfattande ombyggnad av grundläggande cellfunktioner: friska leverområden var rikare på protein kopplade till metabolism, medan tumörer var fyllda med proteiner knutna till celldelning, DNA‑hantering och det fibrösa material som omger celler. Dessa skillnader bekräftade att proteomnivån fångar sjukdomsegenskaper som inte alltid syns i gendata.
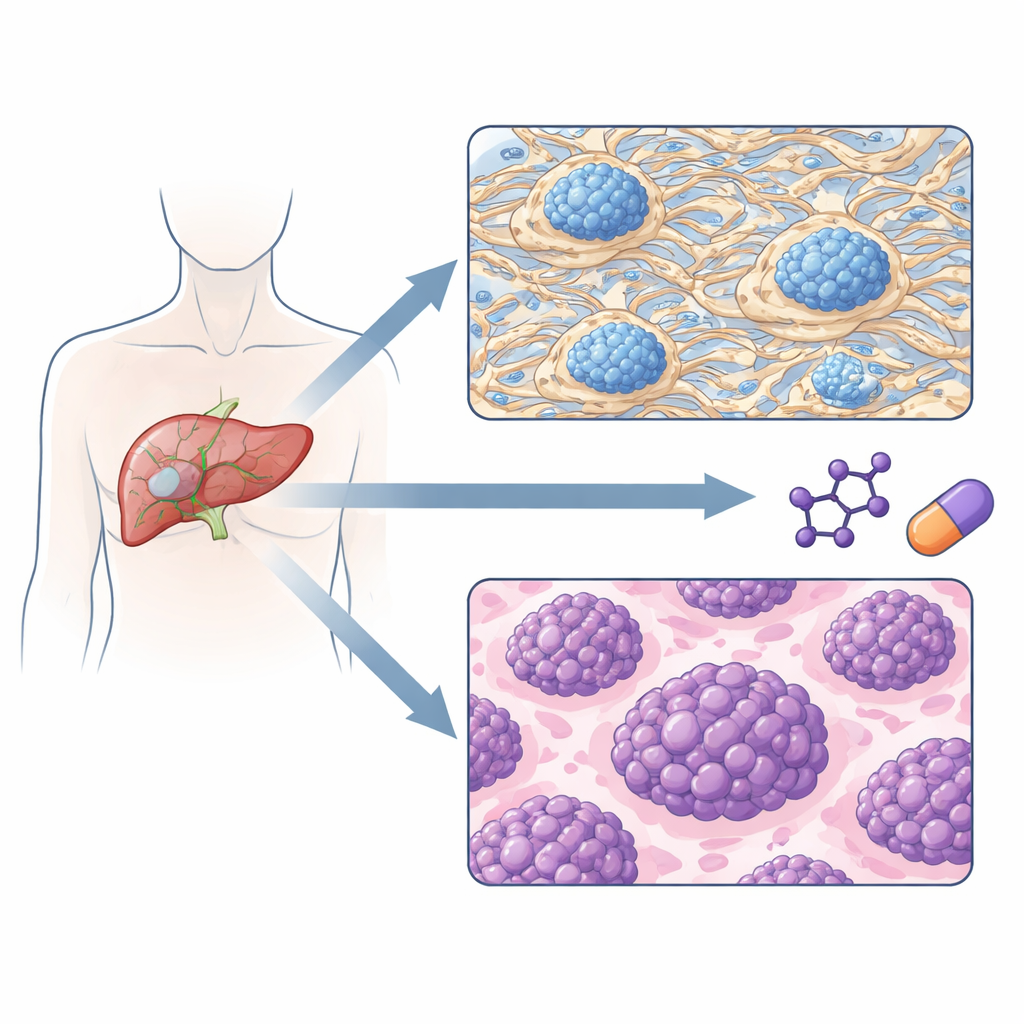
Två tumörtyper med olika återfallsrisk
När teamet grupperade tumörer enbart utifrån deras proteinmönster framträdde två huvudsakliga subtyper. En subtyp dominerades av proteiner som bygger och omformar den extracellulära matrisen — stommen mellan celler — tillsammans med komponenter för blodkoagulation och vissa immunsignaler. Den andra subtypen dominerades av proteiner som driver DNA‑replikation, RNA‑bearbetning och proteinsyntes, alla kännetecken för snabbt växande celler. Viktigt är att dessa två protein‑definierade grupper hade mycket olika kliniska förlopp: patienter i den "matrisrika" gruppen tenderade att ha tumörer i ett tidigare stadium och gick betydligt längre innan cancern återkom, medan patienter i den "proliferationsdominerade" gruppen relapserade snabbare och hade kortare total överlevnad.
Ett enkelt test som fungerar över patientgrupper
För att omvandla dessa insikter till något som ligger närmare ett praktiskt verktyg använde forskarna maskininlärning för att bygga en klassificerare baserad på bara fyra proteiner som bäst särskilde de två subtyperna. De tränade och testade många kombinationer av fyra proteiner på sin huvudpatientserie och fann att de flesta kunde separera undergrupperna med hög noggrannhet. Med den bäst presterande uppsättningen tillämpade de sedan denna klassificerare på två oberoende samlingar av intrahepatisk kolangiokarcinom från andra sjukhus, inklusive en stor kinesisk kohort som tidigare karaktäriserats på gen‑ och proteinnivå. I båda externa grupperna återkom samma två proteomiska mönster, och patienter som placerades i den matrisrika gruppen hade återigen bättre utfall än de i den proliferationsdominerade gruppen. Detta tyder på att ett litet proteinpanel skulle kunna hjälpa kliniker att uppskatta återfallsrisk över olika populationer.
Att hitta ett gemensamt läkemedelsmål i båda subtyperna
Bortom riskprediktion sökte forskarna efter proteiner som konsekvent var förhöjda i tumörer från båda grupperna och som kunde vara mål för terapi. En lovande kandidat var EIF4A1, en nyckelkomponent i cellens maskineri som initierar översättning av RNA‑budskap till proteiner och som är kopplad till cancerfrämjande vägar. EIF4A1 var starkt uppreglerat i tumörer jämfört med närliggande levervävnad, oberoende av subtyp. Teamet testade Zotatifin, ett experimentellt läkemedel som blockerar EIF4A1, i cellinjer härledda från denna cancer och fann att låga doser minskade cellernas överlevnad, särskilt i kombination med en annan signalvägshämmare.
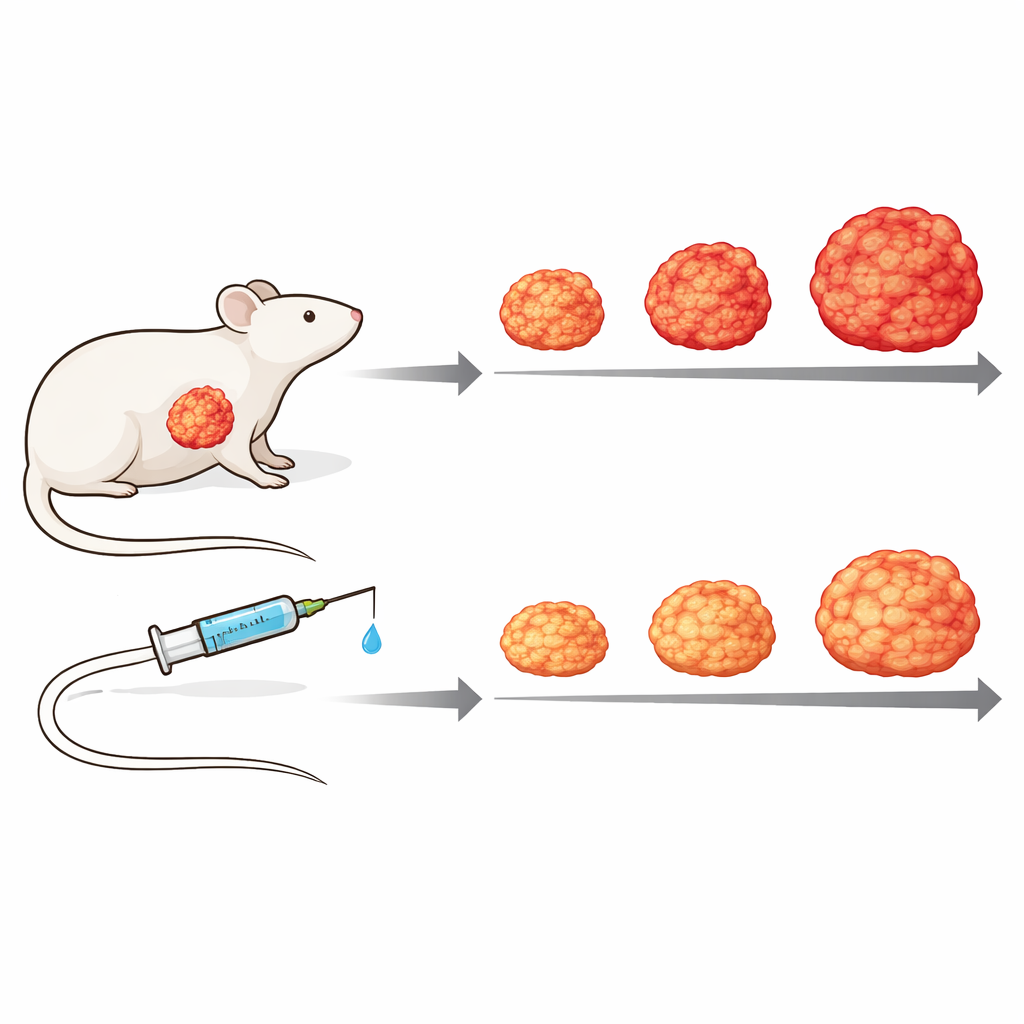
Test av läkemedlet i en levande tumörmodell
För att bättre efterlikna komplexiteten hos mänsklig sjukdom gick forskarna vidare till patientderiverade xenograftmodeller, där bitar av en persons tumör implanteras i immundefekta möss. Genom proteininmätningar som kunde särskilja humana tumörproteiner från musens stromala proteiner visade de att den omgivande bindväven svarar olika beroende på tumörens interna aktivitet, vilket understryker vikten av tumör–stroma‑korsprat. I en sådan modell bromsade veckobehandling med Zotatifin tumörtillväxten avsevärt jämfört med obehandlade möss, utan uppenbar toxicitet: tumörerna växte långsammare och förblev mindre, och behandlade djur bibehöll sin kroppsvikt bättre över tiden.
Vad detta betyder för patienter
Enkelt uttryckt visar detta arbete att intrahepatisk kolangiokarcinom inte är en enda sjukdom utan åtminstone två huvudtyper definierade av proteiner med olika sannolikhet för återfall efter operation. Ett fokuserat fyra‑proteins test skulle kunna hjälpa läkare att identifiera patienter med högre risk som kan ha nytta av intensivare uppföljning eller tilläggsbehandling. Samtidigt pekar upptäckten att båda subtyperna är beroende av translationsfaktorn EIF4A1, och att blockering med Zotatifin kan dämpa tumörtillväxt i realistiska modeller, mot en möjlig ny behandlingsstrategi. Kliniska prövningar krävs för att bekräfta säkerhet och nytta hos människor, men studien visar hur djup proteomprofilering både kan förfina prognos och avslöja åtgärdbara läkemedelsmål i en svårbehandlad cancer.
Citering: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Nyckelord: intrahepatisk kolangiokarcinom, cancerproteomik, tumörsubtyper, EIF4A1-hämning, patientderiverad xenograft