Clear Sky Science · nl
Proteomische karakterisering van intrahepatische cholangiokarcinoom identificeert risicostratificerende subgroepen en EIF4A1 als therapeutisch doelwit
Waarom deze leverkankerstudie ertoe doet
Intrahepatisch cholangiokarcinoom is een zeldzame maar steeds vaker voorkomende vorm van galwegkanker die in de lever ontstaat. Het wordt meestal laat ontdekt, keert vaak terug na een operatie, en artsen hebben momenteel weinig betrouwbare manieren om te voorspellen welke patiënten zullen terugvallen of baat hebben bij aanvullende behandeling. Deze studie gebruikt geavanceerde proteïne-analyse om deze tumoren in biologisch onderscheiden groepen in te delen en om een gedeelde kwetsbaarheid aan het licht te brengen die mogelijk met een nieuw geneesmiddel kan worden aangepakt.
Nauwkeurige bestudering van eiwitten in levertumoren
De onderzoekers onderzochten tumorstalen en nabijgelegen niet-kankerachtig leverweefsel van twee groepen patiënten die werden behandeld in grote medische centra in de Verenigde Staten en Duitsland. In plaats van zich te concentreren op DNA of RNA, maten ze duizenden eiwitten in elk staal met behulp van geavanceerde massaspectrometrie, een techniek die veel moleculen tegelijk kan kwantificeren. Door tumoren te vergelijken met het omringende weefsel zagen ze een brede herprogrammering van basale cellulaire functies: gezonde leverregio’s bevatten meer eiwitten die met metabolisme te maken hebben, terwijl tumoren vol zaten met eiwitten die verbonden zijn met celdeling, DNA-hantering en het vezelige materiaal rond cellen. Deze verschillen bevestigen dat het proteïne-niveau kenmerken van de ziekte vangt die niet uit gengegevens alleen zichtbaar zijn.
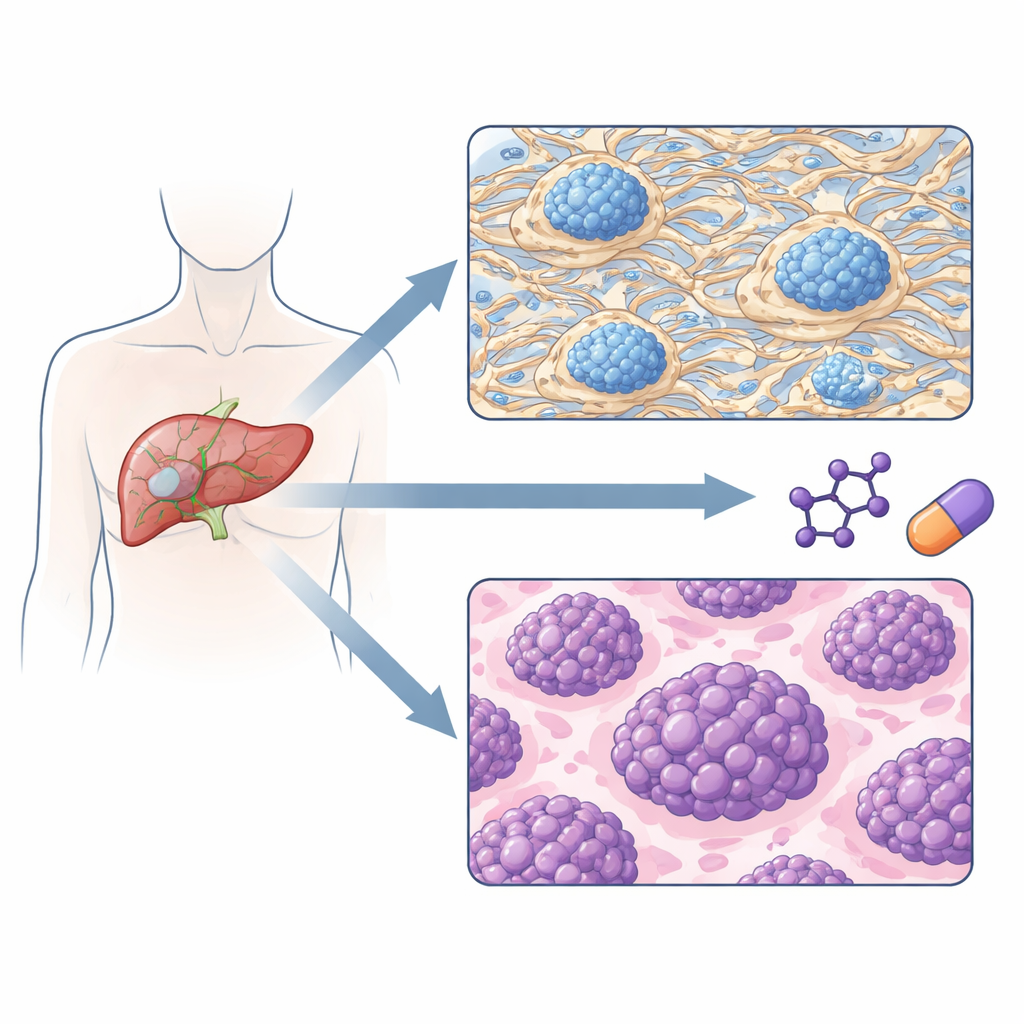
Twee tumortypen met verschillend terugkeer-risico
Toen het team tumoren puur groepeerde op basis van hun eiwitpatronen, ontstonden twee hoofdsubtypen. Het ene subtype werd gedomineerd door eiwitten die de extracellulaire matrix opbouwen en remodelleren — het geraamte tussen cellen — samen met componenten van bloedstolling en bepaalde immuunsignalen. Het andere subtype werd gedomineerd door eiwitten die DNA-replicatie, RNA-verwerking en eiwitsynthese aansturen, allemaal kenmerken van snelgroeiende cellen. Belangrijk is dat deze twee proteomisch gedefinieerde groepen zeer verschillende klinische beloop vertoonden: patiënten in de ‘matrix-rijke’ groep hadden vaker tumoren in een eerder stadium en bleven veel langer vrij van terugkeer, terwijl patiënten in de ‘proliferatie-zware’ groep eerder recidiveerden en een kortere totale overleving hadden.
Een eenvoudige test die in verschillende patiëntengroepen werkt
Om deze inzichten om te zetten in iets dichter bij een praktische tool, gebruikten de onderzoekers machine learning om een classifier te bouwen op basis van slechts vier eiwitten die de twee subtypen het beste onderscheidden. Ze trainden en testten veel vier-eiwitcombinaties op hun hoofdcohort en vonden dat de meeste combinaties de subgroepen nauwkeurig konden scheiden. Met de best presterende set pasten ze deze classifier vervolgens toe op twee onafhankelijke verzamelingen intrahepatische cholangiokarcinomen van andere ziekenhuizen, waaronder een grote Chinese cohorte die eerder op gen- en eiwitniveau was gekarakteriseerd. In beide externe groepen verschenen dezelfde twee proteomische patronen opnieuw, en patiënten toegewezen aan de matrix-rijke groep deden het opnieuw beter dan die in de proliferatie-zware groep. Dit suggereert dat een klein eiwitpaneel artsen kan helpen het terugkeerrisico over verschillende populaties heen in te schatten.
Een gemeenschappelijk geneesmiddeldoel in beide subtypen vinden
Naast risicovoorspelling zochten de wetenschappers naar eiwitten die in tumoren van beide groepen consequent verhoogd waren en mogelijk therapeutisch aan te pakken zijn. Een veelbelovende kandidaat was EIF4A1, een sleutelelement van de cellulaire machinerie die het vertalen van RNA-boodschappen naar eiwitten start en verbonden is met kankerverhogende paden. EIF4A1 was sterk verhoogd in tumoren vergeleken met nabijgelegen leverweefsel, ongeacht subtype. Het team testte Zotatifin, een experimenteel geneesmiddel dat EIF4A1 blokkeert, in cellijnen afgeleid van deze kanker en ontdekte dat lage doses hun levensvatbaarheid verminderden, vooral in combinatie met een remmer van een ander pad.
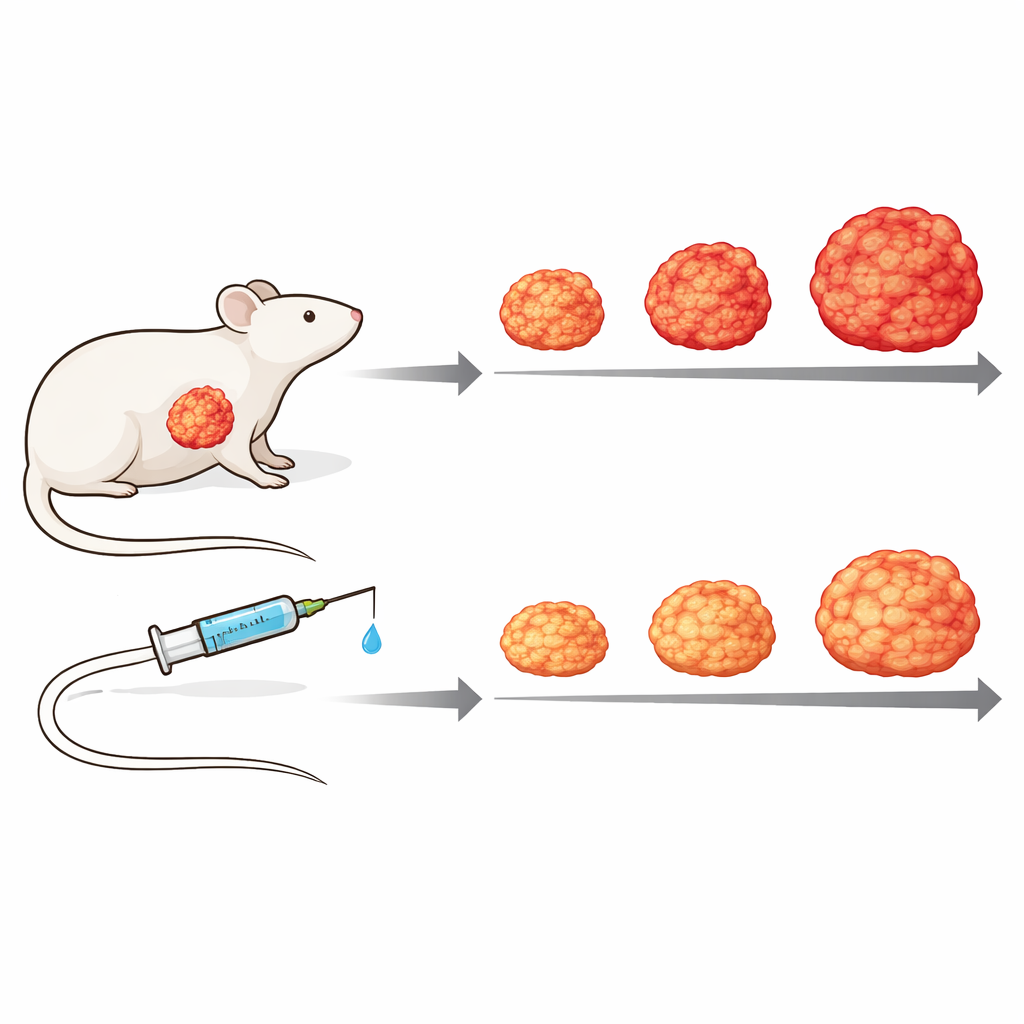
Het medicijn testen in een levend tumormodel
Om de complexiteit van menselijke ziekte beter na te bootsen, gingen de onderzoekers over op patiënt-afgeleide xenograft-modellen, waarbij stukjes van een menselijke tumor in immuungecompromitteerde muizen worden geïmplanteerd. Met eiwitmetingen die menselijke tumorproteïnen van muizene stroma-eiwitten konden onderscheiden, toonden ze aan dat het omringende bindweefsel verschillend reageert afhankelijk van de interne activiteit van de tumor, wat het belang van tumor–stroma crosstalk onderstreept. In één zo’n model vertraagde wekelijkse behandeling met Zotatifin de tumorgroei aanzienlijk in vergelijking met onbehandelde muizen, zonder duidelijke toxiciteit: tumoren groeiden trager en bleven kleiner, en behandelde dieren behielden beter hun lichaamsgewicht in de tijd.
Wat dit voor patiënten betekent
Simpel gezegd laat dit werk zien dat intrahepatisch cholangiokarcinoom geen eenduidige ziekte is maar ten minste twee belangrijke, proteomisch gedefinieerde types met verschillende kansen op terugkeer na operatie. Een gericht vier-eiwittest kan artsen helpen hogere-risico patiënten te identificeren die mogelijk baat hebben bij intensievere follow-up of aanvullende therapie. Tegelijk wijst de ontdekking dat beide subtypen afhankelijk zijn van de translatiefactor EIF4A1, en dat blokkade met Zotatifin tumorgroei in realistische modellen kan remmen, op een potentiële nieuwe behandelingsstrategie. Hoewel klinische onderzoeken nodig zullen zijn om veiligheid en voordeel bij mensen te bevestigen, toont deze studie aan hoe diepe proteïneprofilering zowel prognose kan verfijnen als hanteerbare geneesmiddeldoelen kan onthullen in een moeilijk te behandelen kanker.
Bronvermelding: Werner, T., Thiery, J., Budau, KL. et al. Proteomic characterization of intrahepatic cholangiocarcinoma identifies risk-stratifying subgroups and EIF4A1 as a therapeutic target. Nat Commun 17, 2741 (2026). https://doi.org/10.1038/s41467-026-70817-1
Trefwoorden: intrahepatisch cholangiokarcinoom, kankerproteomica, tumorsubtypen, EIF4A1-remming, patiënt-afgeleide xenograft