Clear Sky Science · tr
Notch sinyalini hedefleyerek fare modellerinde sinir gelişimi ve davranışları eski haline getirmek
Bu araştırma aileler ve toplum için neden önemli
Otizm spektrum bozukluğu (OSB), insanların iletişim, sosyalleşme ve çevreye yanıt verme biçimini etkiler; ancak biyolojik kökenleri hâlâ karmaşıktır. Bu fare çalışması büyük bir soruyu ele alıyor: otizme yönelik çok farklı risk faktörleri — genetik değişiklikler, gebelik sırasında enfeksiyonlar veya belirli ilaçlar — aynı beyin yolunu mu bozuyor? Araştırmacılar, Notch adı verilen bir gelişimsel sinyalleşme sisteminde ortak bir bozulma buluyor ve doğum öncesi bu yolu dikkatli biçimde baskılamanın birkaç OSB-benzeri fare modelinde daha normal beyin bağlantıları ve sosyal davranışı yeniden sağlayabildiğini gösteriyor.
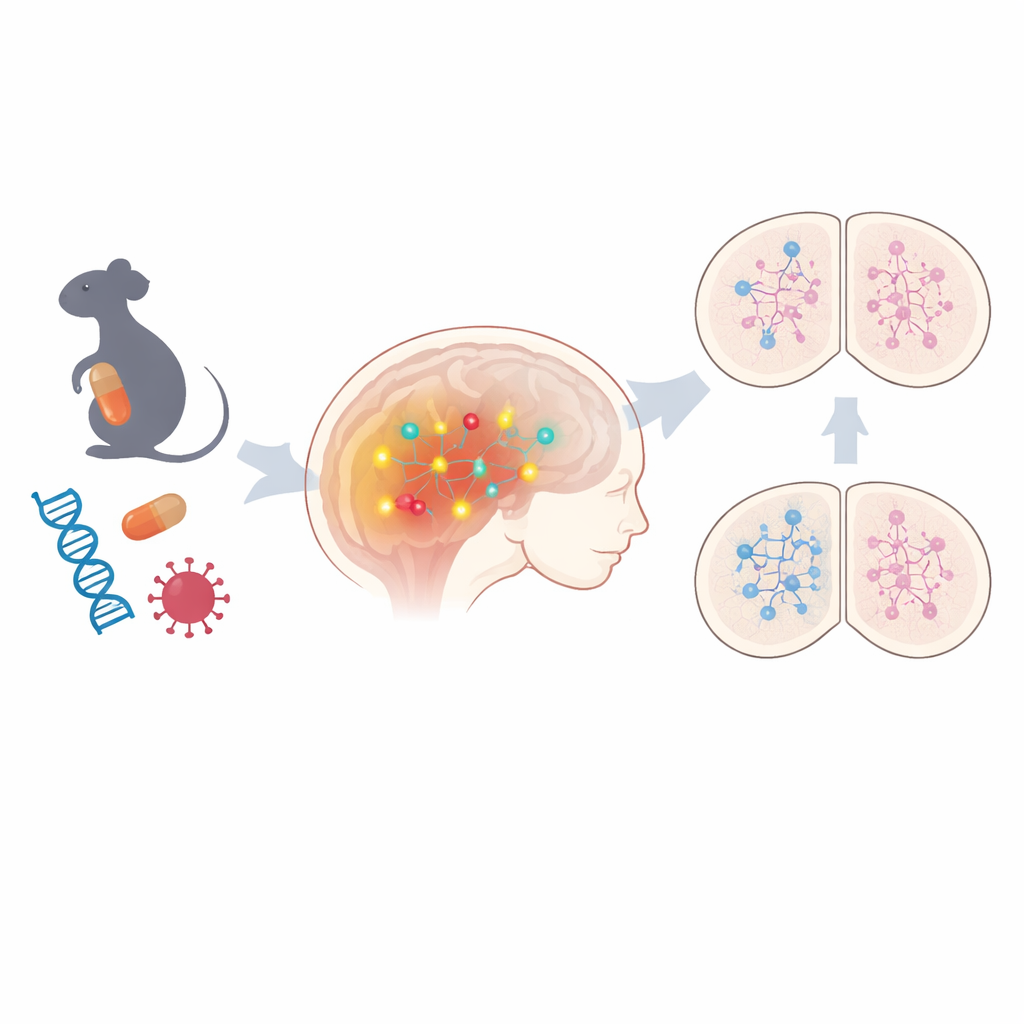
Çeşitli risklerin arkasındaki ortak bir yol
Ekip, iki genetik olmayan OSB modelinden fetal fare beyinlerini inceleyerek başladı: biri gebe farelerin antikonvülzant valproik aside maruz kaldığı model, diğeri anne kaynaklı viral enfeksiyonu taklit eden model. Geniş çaplı gen aktivitesi profillemesi kullanarak, her iki modelde de yüzlerce genin değiştiğini ve DNA’yı değiştirmeden genleri açıp kapatan kimyasal işaretler olan epigenetik düzenlemede güçlü bozulma imzaları olduğunu buldular. Paylaşılan değişiklikler arasında öne çıkan bir yol vardı: Notch sinyalleşmesi — olgunlaşmamış beyin hücrelerinin hangi tür nöron olacaklarına karar vermelerinde kilit bir denetleyici. Bu yolun bileşenleri, çekirdek reseptörler ve aşağı akış etkileyiciler dahil, sürekli olarak artmış durumdaydı. Bilim insanları, otizmle ilişkilendirilmiş bazı genetik varyantları taşıyan insan kök hücre bazlı nöron modellerine baktıklarında da birkaç durumda Notch ile ilişkili gen aktivitesinin yükseldiğini gördüler; bu da bu yolun hem çevresel hem kalıtsal OSB formları arasında ortak bir ipucu olabileceğini düşündürür.
Aktiviteyi ince ayarlayan kırılgan beyin hücreleri
Notch aşırı aktivitesinin sonuçlarını anlamak için araştırmacılar korteksteki uyarıcı ve baskılayıcı sinyalleşme dengesine odaklandı — genellikle otizmde bozulan bir denge. Kortikal devrelerin gelen uyarıya ne kadar güçlü yanıt vereceğini düzenlemeye yardımcı olan VIP adlı küçük bir baskılayıcı sinir hücresi popülasyonuna yoğunlaştılar. Hem valproik asit hem de maternal bağışıklık aktivasyonu modellerinde bu VIP hücreleri kortekste dramatik şekilde azalmışken, diğer çoğu interneuron tipi büyük ölçüde korunmuştu. Bu hücrelerin kökenini kaudal ganglionel eminens adlı fetal beyin bölgesine kadar izlediklerinde, oradaki progenitör hücrelerin aşırı çoğaldığını ancak doğru şekilde post-mitozik VIP öncü hücrelere dönüşüp kortekse göç edemediklerini buldular. Bu desen, aşırı aktif Notch sinyalinin bu progenitörleri “hiç büyümeyen” bir durumda sıkıştırarak kalıcı VIP interneuron eksikliğine ve aşırı uyarılmaya eğilim yarattığını gösteriyordu.
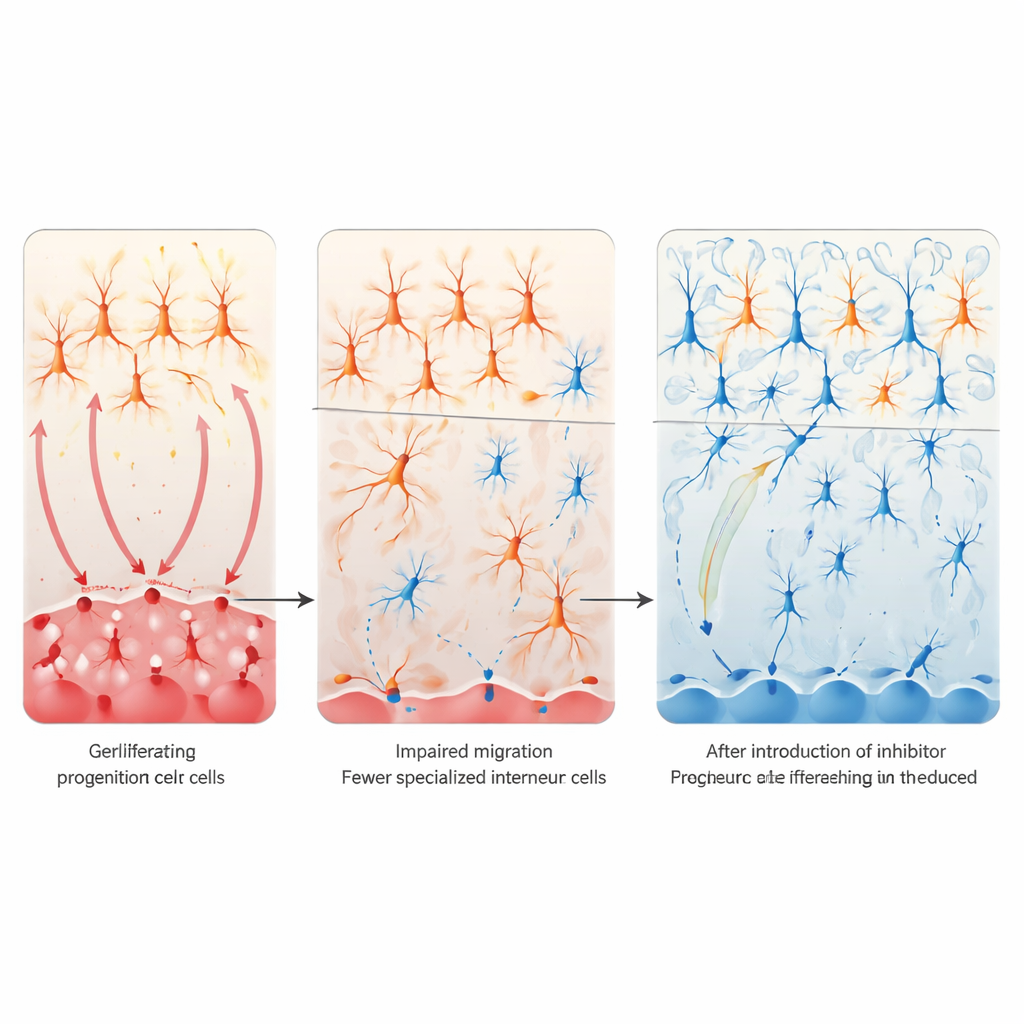
Notch’u kısarak beyin devrelerini geri kazandırmak
Sıradaki soru, Notch sinyalini yatıştırmanın bu kusurları düzeltebilip düzeltemeyeceğiydi. Hücre kültürlerinde, Notch reseptörünün aktif formunu gelişen ön beyin hücrelerine zorla verince VIP interneuron belirteçlerinde azalma görüldü; oysa Notch’u genetik olarak veya bir γ-sekretaz inhibitörü ile engellemek ters etki yaptı ve valproik asit maruziyetinden sonra bile VIP belirteçlerini yeniden sağlayabildi. Canlı farelerde ekip, kaudal ganglionel eminens kaynaklı hücrelerde seçici olarak Notch1 ve Notch2’yi sildi. Bu yerel genetik “fren”, kortikal VIP interneuronlarının kaybını önledi ve gestasyon sırasında valproik aside maruz kalan yavrularda sosyal etkileşim davranışlarını büyük ölçüde normalleştirdi. Yetişkin beyinlerin transkriptomik analizi, bu kurtarmanın ayrıca uyarıcı glutamat sinapslarıyla bağlantılı genlerin anormal yükselişini de bastırdığını gösterdi; bu da baskılayıcı VIP devrelerini geri getirmenin daha geniş kortikal ağları yeniden dengelemeye yardımcı olduğunu düşündürüyor.
Gelişimi yeniden şekillendiren tek doz prenatal ilaç
Genetik müdahaleler insanlarda pratik olmadığından, araştırmacılar ilaç temelli bir strateji denedi. Daha önce kanser ve Alzheimer denemelerinde değerlendirilen güçlü bir γ-sekretaz inhibitörü olan Ro4929097’yi kullandılar ve tek dozu valproik asit ile birlikte gebe farelere uyguladılar. Bu kısa prenatal tedavi aktif Notch protein düzeylerini azalttı, yavruların korteksinde VIP interneuron sayılarını büyük ölçüde geri getirdi ve tekrarlayıcı tımar davranışı ve sosyal eksiklikler dahil olmak üzere birden çok OSB-benzeri davranışı iyileştirdi. Yeni doğan beyinlerin tek hücre RNA dizilemesi, ilacın yalnızca VIP soyunu normalleştirmekle kalmadığını; aynı zamanda sinir progenitörleri, oligodendrositler (miyelin oluşturan hücreler) ve diğer hücre popülasyonlarındaki daha geniş bozulmaları da düzelttiğini ve genel hücresel bileşimi kontrol hayvanlarda görülen duruma doğru ittiğini ortaya koydu.
Otizmi anlama ve tedavi etme açısından bunun anlamı
Halk için çıkarılacak temel mesaj, çeşitli otizme ilişkin etkilerin gelişen beyinde ortak bir “anahtar panel” üzerinde birleşebileceğidir. Kritik bir fetal pencere sırasında Notch yolu “açık” pozisyonda takılı kalırsa, önemli baskılayıcı sinir hücreleri olgunlaşmayı başaramaz ve kortikal devreler dengesizleşir; bu da sosyal ve davranışsal problemlere katkıda bulunur. Farelerde, bu yolu dikkatle zamanlanmış biçimde — belirli hücre tiplerinde veya tek bir prenatal ilaç dozu ile — baskılamak normal gelişim ve davranışı büyük ölçüde geri getirebilir. Böyle bir yaklaşımı insanlara çevirmek büyük bir özen gerektirecek olsa da, bu bulgular Notch sinyalleşmesini ve özellikle VIP interneuronların gelişimini, erken dönem müdahalelerle OSB ilişkili beyin işlev bozukluklarının en az bazı biçimlerini önlemeye yönelik umut verici hedefler olarak öne çıkarıyor.
Atıf: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Anahtar kelimeler: otizm spektrum bozukluğu, Notch sinyalleşmesi, VIP interneuronlar, nörogelişim, epigenetik