Clear Sky Science · es
Dirigir la señalización Notch para restaurar el desarrollo neural y el comportamiento en modelos de ratón del TEA
Por qué esta investigación importa para las familias y la sociedad
El trastorno del espectro autista (TEA) afecta la forma en que las personas se comunican, se relacionan socialmente y responden al mundo que les rodea, pero sus raíces biológicas siguen siendo enigmáticas. Este estudio en ratones aborda una pregunta importante: ¿acaban factores de riesgo muy distintos para el autismo —genes, infecciones durante el embarazo o ciertos medicamentos— alterando la misma vía cerebral? Los investigadores descubren una alteración compartida en un sistema de señalización del desarrollo llamado Notch y muestran que reducir cuidadosamente esta vía antes del nacimiento puede restaurar un cableado cerebral y un comportamiento social más normales en varios modelos de ratón con rasgos similares al TEA.
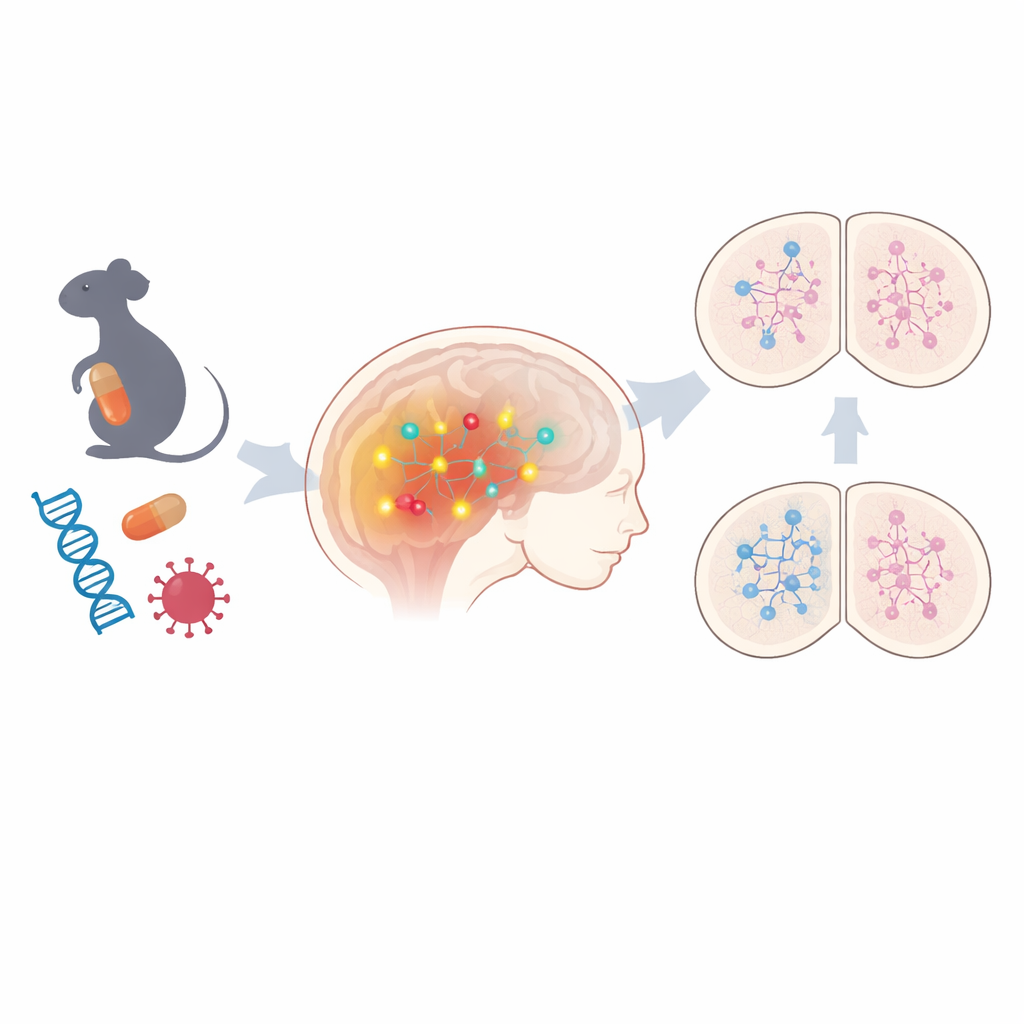
Una vía común tras muchos riesgos diferentes
El equipo comenzó examinando cerebros fetales de ratón de dos modelos no genéticos de TEA: uno en el que las hembras embarazadas fueron expuestas al fármaco anticonvulsivante valproato, y otro que imita una infección viral materna. Mediante un perfil amplio de la actividad génica, encontraron que cientos de genes estaban alterados en ambos modelos, con señales claras de una regulación epigenética perturbada —marcas químicas que activan o desactivan genes sin cambiar el ADN—. Entre los cambios compartidos, destacó una vía: la señalización Notch, un controlador clave de cómo las células cerebrales inmaduras deciden en qué tipo de neurona convertirse. Componentes de esta vía, incluidos receptores centrales y efectores posteriores, se encontraban consistentemente aumentados. Cuando los científicos observaron modelos neuronales derivados de células madre humanas que portaban algunas variantes genéticas vinculadas al autismo, de nuevo vieron una mayor actividad génica relacionada con Notch en varios casos, lo que sugiere que esta vía puede ser un hilo común tanto en formas ambientales como hereditarias del TEA.
Células cerebrales vulnerables que afinan la actividad
Para entender las consecuencias de la sobreactividad de Notch, los investigadores se centraron en el equilibrio entre la señalización excitadora e inhibitoria en la corteza —a menudo alterado en el autismo. Se fijaron en una pequeña población de células nerviosas inhibitorias llamadas interneuronas VIP, que ayudan a regular la intensidad con la que los circuitos corticales responden a las entradas. En los modelos de ratón con valproato y con activación inmune materna, estas células VIP estaban drásticamente reducidas en la corteza, mientras que la mayoría de otros tipos de interneuronas quedaban mayormente preservados. Rastreando el origen de estas células hasta una región cerebral fetal llamada eminencia ganglionar caudal, encontraron que las células progenitoras allí proliferaban en exceso pero no lograban convertirse correctamente en precursores VIP posmitóticos ni migrar a la corteza. El patrón sugería que la señalización Notch hiperactiva estaba atrapando a estos progenitores en un estado de “nunca madurar”, provocando una escasez duradera de interneuronas VIP y una inclinación hacia la excitación excesiva.
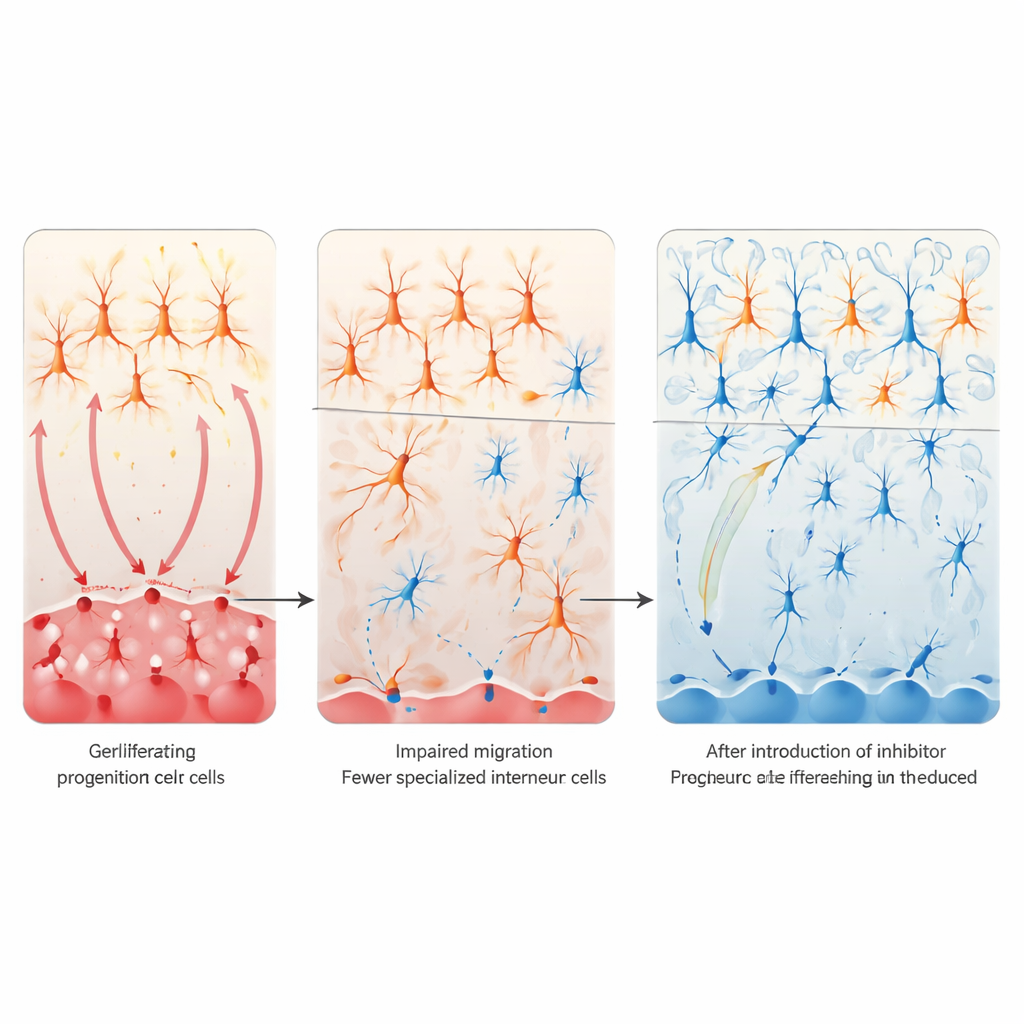
Reducir Notch para rescatar circuitos cerebrales
La siguiente pregunta fue si calmar la señalización Notch podía rescatar estos defectos. En cultivo celular, forzar la forma activa del receptor Notch en células del prosencéfalo en desarrollo redujo marcadores de interneuronas VIP, mientras que bloquear Notch genéticamente o con un inhibidor de γ-secretasa produjo el efecto opuesto y pudo restaurar los marcadores VIP incluso después de la exposición al valproato. En ratones vivos, el equipo eliminó selectivamente Notch1 y Notch2 en células derivadas de la eminencia ganglionar caudal. Este “freno” genético local evitó la pérdida de interneuronas VIP en la corteza y normalizó en gran medida los comportamientos de interacción social en las crías expuestas al valproato durante la gestación. El análisis transcriptómico de cerebros adultos mostró que este rescate también atenuó una regulación anormal al alza de genes vinculados a sinapsis glutamatérgicas excitadoras, lo que sugiere que restaurar los circuitos inhibitorios VIP ayuda a reequilibrar redes corticales más amplias.
Un fármaco prenatal de una sola dosis que remodela el desarrollo
Dado que las intervenciones genéticas no son prácticas en humanos, los investigadores probaron una estrategia basada en fármacos. Usaron Ro4929097, un potente inhibidor de γ-secretasa previamente evaluado en ensayos contra el cáncer y el Alzheimer, y administraron una única dosis a ratonas embarazadas junto con valproato. Este tratamiento prenatal breve redujo los niveles de la proteína Notch activa, restauró en gran medida el número de interneuronas VIP en la corteza de las crías y mejoró múltiples comportamientos similares al TEA, incluidos el acicalamiento repetitivo y los déficits sociales. La secuenciación de ARN a nivel de célula única en cerebros de recién nacidos reveló que el fármaco no solo normalizó la línea VIP; también corrigió alteraciones más amplias en progenitores neuronales, oligodendrocitos (células formadoras de mielina) y otras poblaciones celulares, empujando la composición celular general hacia la observada en animales controles.
Qué significa esto para entender y tratar el autismo
Para un público general, la conclusión es que influencias diversas relacionadas con el autismo pueden converger en una “central” compartida en el cerebro en desarrollo. Cuando la vía Notch queda atascada en la posición de “activada” durante una ventana fetal crítica, células nerviosas inhibitorias clave no maduran y los circuitos corticales se desequilibran, lo que contribuye a problemas sociales y conductuales. En ratones, atenuar esta vía en el momento adecuado —ya sea en tipos celulares específicos o con una única dosis prenatal de fármaco— puede restaurar en gran medida el desarrollo y el comportamiento normales. Si bien traducir un enfoque así a humanos requerirá extrema cautela, estos hallazgos señalan a la señalización Notch, y en particular al desarrollo de las interneuronas VIP, como objetivos prometedores para intervenciones tempranas destinadas a prevenir al menos algunas formas de disfunción cerebral asociada al TEA.
Cita: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Palabras clave: trastorno del espectro autista, señalización Notch, interneuronas VIP, neurodesarrollo, epigenética