Clear Sky Science · ru
Таргетирование сигнальной системы Notch для восстановления нейронного развития и поведения в мышиных моделях РАС
Почему это исследование важно для семей и общества
Расстройство аутистического спектра (РАС) меняет способы общения, социализации и восприятия мира, однако его биологические корни остаются не до конца понятными. В этом исследовании на мышах поставлен крупный вопрос: приводят ли очень разные факторы риска — генетические нарушения, инфекции во время беременности или некоторые лекарства — к нарушению одной и той же мозговой дорожки? Учёные обнаруживают общее нарушение в развивающейся сигнальной системе Notch и показывают, что её аккуратное подавление до рождения может восстановить более нормальную схему проводки мозга и социальное поведение в нескольких моделях мышей с чертами РАС.
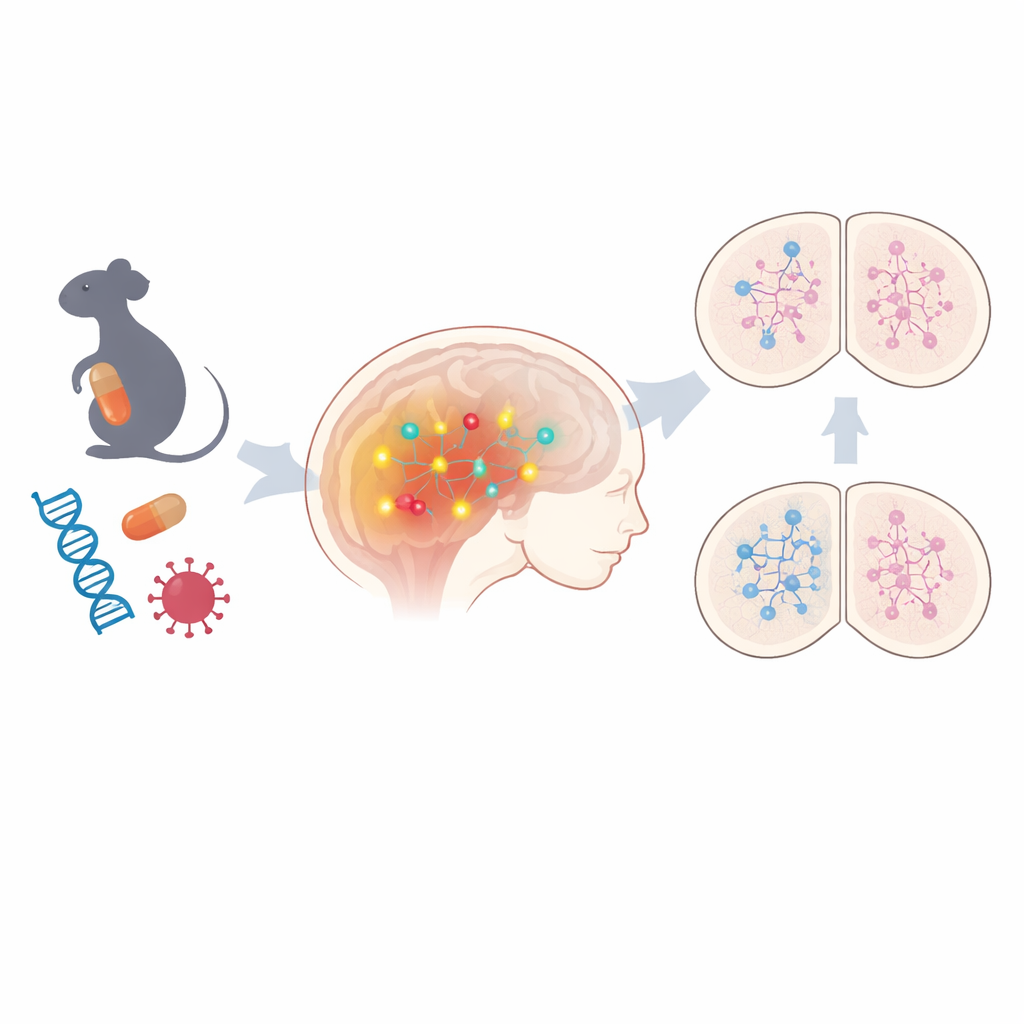
Общая дорожка, лежащая в основе разных факторов риска
Команда начала с изучения эмбриональных мозгов мышей в двух негенных моделях РАС: одна имитировала воздействие на беременных противоэпилептического препарата вальпроевой кислоты, другая — материнскую вирусную инфекцию. С помощью широкой профилизации активности генов они обнаружили, что сотни генов изменены в обеих моделях, с выраженными признаками нарушения эпигенетической регуляции — химических меток, включающих или выключающих гены без изменения ДНК. Среди общих изменений выделялась одна дорожка: сигналинг Notch, ключевой регулятор того, как незрелые клетки мозга решают, в какой тип нейронов дифференцироваться. Компоненты этой системы, включая основные рецепторы и эффекторные молекулы, стабильно были повышены. При изучении человеческих моделей нейронов на основе стволовых клеток, несущих некоторые варианты, связанные с аутизмом, в ряде случаев также наблюдали усиленную активность генов, связанных с Notch, что наводит на мысль, что эта дорожка может быть общей нитью как для факторов окружающей среды, так и для наследственных форм РАС.
Уязвимые клетки, которые тонко настраивают активность
Чтобы понять последствия гиперактивности Notch, исследователи сосредоточились на балансе возбуждающей и тормозящей сигнализации в коре — часто нарушаемом при аутизме. Они обратили внимание на небольшую популяцию тормозных нейронов, называемых VIP-внутреннейронами, которые помогают регулировать силу реакции кортикальных схем на входящие сигналы. В обеих моделях — при вальпроатной экспозиции и при активации материнского иммунитета — число этих VIP-клеток в коре было резко уменьшено, тогда как большинство других типов интернейронов в основном сохранялись. Прослеживая происхождение этих клеток до эмбриональной области, называемой каудальной ганглионарной эминенцией, они обнаружили, что там клеточные предшественники избыточно пролиферировали, но не переключались должным образом в постмитотические VIP-предшественники и не мигрировали в кору. Эта картина указывала на то, что гиперактивный сигналинг Notch удерживает предшественники в состоянии «никогда не взрослеют», что приводит к постоянному дефициту VIP-интернейронов и сдвигу в сторону чрезмерного возбуждения.
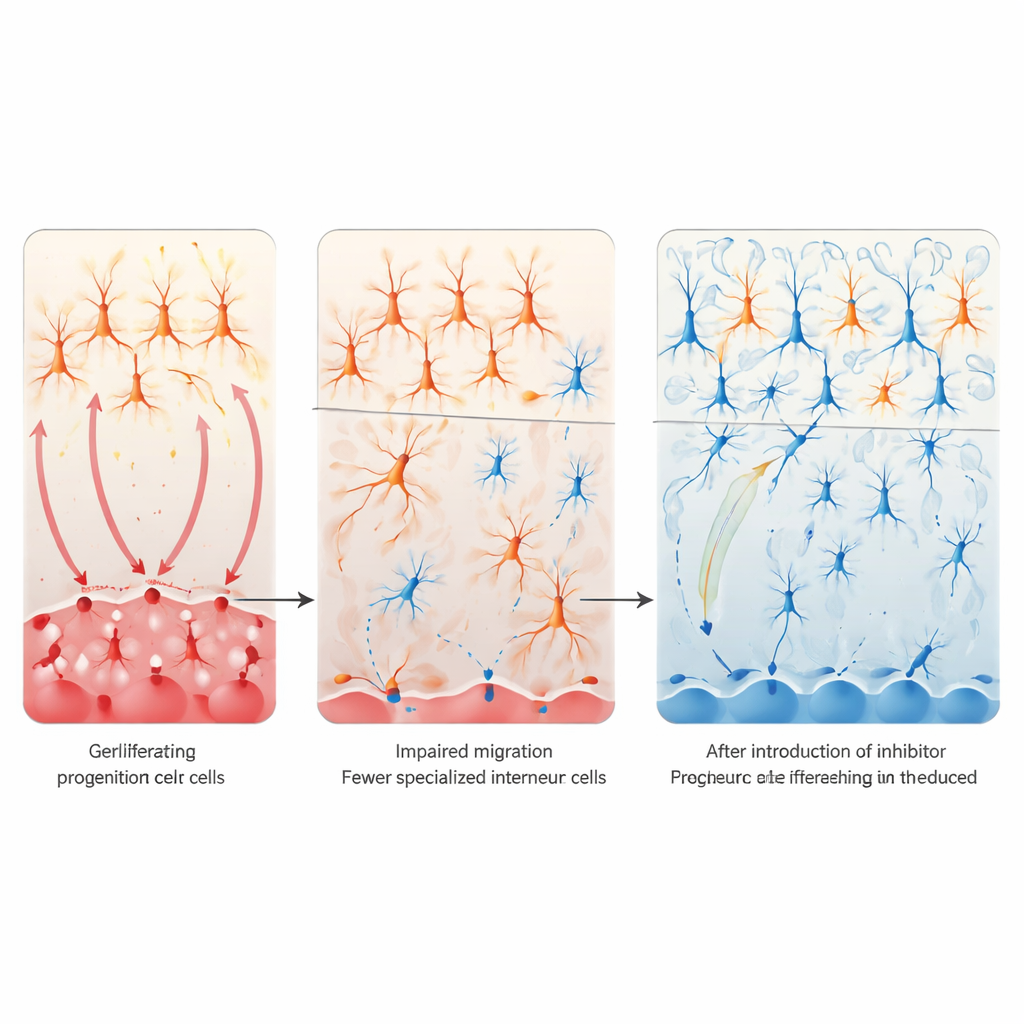
Подавление Notch для спасения мозговых цепей
Следующий вопрос заключался в том, может ли успокоение сигналинга Notch исправить эти дефекты. В клеточных культурах введение активной формы рецептора Notch в развивающиеся клетки переднего мозга снижало маркеры VIP-интернейронов, тогда как генетическое блокирование Notch или применение ингибитора γ-секретазы имели обратный эффект и могли восстановить маркеры VIP даже после воздействия вальпроевой кислоты. У живых мышей команда избирательно удаляла Notch1 и Notch2 в клетках, происходящих из каудальной ганглионарной эминенции. Этот локальный генетический «тормоз» предотвратил потерю кортикальных VIP-интернейронов и в значительной степени нормализовал социальное поведение потомства, подвергавшегося воздействию вальпроевой кислоты во время беременности. Транскриптомный анализ взрослых мозгов показал, что такое восстановление также ослабляло аномальное повышение экспрессии генов, связанных с возбуждающими глутаматными синапсами, что указывает на то, что восстановление ингибирующих VIP-схем помогает перебалансировать более широкие кортикальные сети.
Однократный пренатальный препарат, который перекраивает развитие
Поскольку генетические вмешательства непрактичны для людей, исследователи опробовали лекарственную стратегию. Они использовали Ro4929097, мощный ингибитор γ-секретазы, ранее изучавшийся в онко- и альцгеймеровских клинических испытаниях, и ввели единственную дозу беременным мышам вместе с вальпроевой кислотой. Это краткое пренатальное лечение снизило уровни активного белка Notch, в значительной степени восстановило число VIP-интернейронов в коре потомства и улучшило несколько поведенческих проявлений, похожих на РАС, включая навязчивое вылизывание и социальные дефициты. Одноклеточный РНК-секвенсинг новорождённых мозгов показал, что препарат нормализовал не только линию VIP; он также корректировал более широкие нарушения в нейропредшественниках, олигодендроцитах (клетках, формирующих миелин) и других популяциях клеток, подталкивая общую клеточную композицию ближе к наблюдаемой в контрольных животных.
Что это значит для понимания и лечения аутизма
Для неспециалиста главный вывод таков: разнообразные влияния, связанные с аутизмом, могут сходиться на общем «распределительном щите» в развивающемся мозге. Когда путь Notch застревает во включённом положении в критическое эмбриональное окно, ключевые ингибирующие нейроны не успевают созреть, и кортикальные схемы становятся несбалансированными, что способствует социальным и поведенческим проблемам. У мышей осторожное снижение активности этого пути в нужное время — либо в конкретных типах клеток, либо однократной пренатальной дозой препарата — может в значительной степени восстановить нормальное развитие и поведение. Перенос такого подхода на людей потребует большой осторожности, но эти результаты выделяют сигнальное звено Notch и особенно развитие VIP-интернейронов как перспективные мишени для вмешательств в раннем периоде жизни с целью предотвращения по крайней мере некоторых форм нарушений мозга, связанных с РАС.
Цитирование: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Ключевые слова: расстройство аутистического спектра, сигналинг Notch, VIP-внутреннейронные клетки, нейроразвитие, эпигенетика