Clear Sky Science · nl
Gerichte remming van Notch‑signaaltransductie om neurale ontwikkeling en gedrag te herstellen in muismodellen van ASS
Waarom dit onderzoek van belang is voor families en de maatschappij
Autisme spectrum stoornis (ASS) beïnvloedt hoe mensen communiceren, socialiseren en reageren op hun omgeving, maar de biologische oorzaken blijven onduidelijk. Deze muisstudie pakt een belangrijke vraag aan: leiden uiteenlopende risicofactoren voor autisme — genen, infecties tijdens de zwangerschap of bepaalde geneesmiddelen — uiteindelijk tot verstoring van hetzelfde hersenpad? De onderzoekers ontdekken een gedeelde verstoring in een ontwikkelingssignaleringssysteem genaamd Notch en tonen aan dat het zorgvuldig terugschakelen van dit pad vóór de geboorte de hersenbedrading en sociaal gedrag in meerdere ASS‑achtige muismodellen kan herstellen.
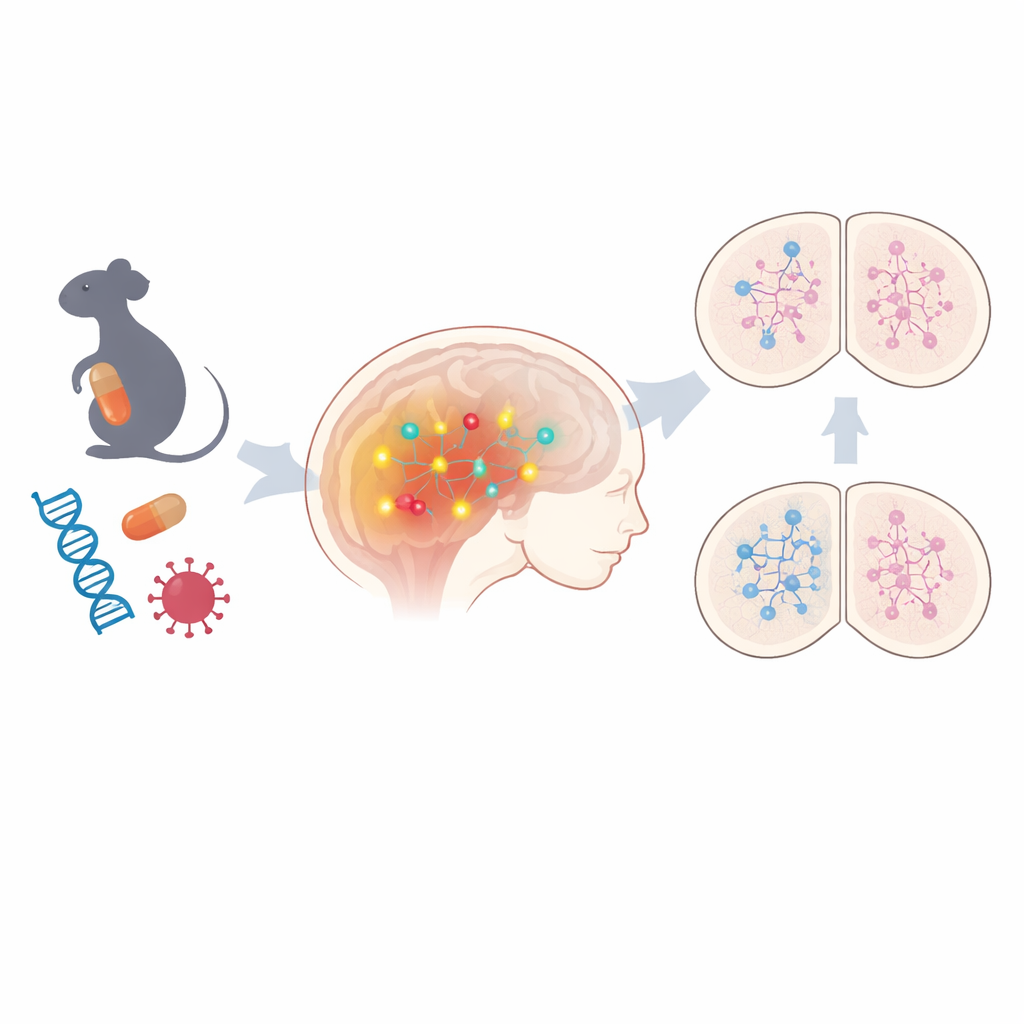
Een gemeenschappelijk pad achter diverse risico’s
Het team begon met het bestuderen van foetale muizenhersenen uit twee niet‑genetische ASS‑modellen: één waarin drachtige muizen werden blootgesteld aan het anti‑epilepticum valproïnezuur en een ander dat maternale virale infectie nabootst. Met brede profiling van genactiviteit vonden ze dat honderden genen in beide modellen waren veranderd, met duidelijke tekenen van verstoorde epigenetische regulatie — chemische markeringen die genen aan of uit zetten zonder het DNA zelf te veranderen. Onder de gedeelde veranderingen stak één pad eruit: Notch‑signaaltransductie, een sleutelregulator van hoe onrijpe hersencellen beslissen welk type neuron ze worden. Componenten van dit pad, waaronder kernreceptoren en downstream effectoren, waren consequent verhoogd. Toen de wetenschappers humane stamcel‑gebaseerde neuraalmodellen met enkele aan autisme gelinkte genetische varianten onderzochten, zagen ze in meerdere gevallen opnieuw verhoogde Notch‑gerelateerde genactiviteit, wat suggereert dat dit pad een gemeenschappelijke factor kan zijn bij zowel omgevings‑ als erfelijke vormen van ASS.
Kwetsbare hersencellen die activiteit fijnregelen
Om de gevolgen van Notch‑overactiviteit te begrijpen, richtten de onderzoekers zich op de balans tussen exciterende en inhiberende signalering in de cortex — vaak verstoord bij autisme. Ze concentreerden zich op een kleine populatie remmende zenuwcellen genaamd VIP‑interneuronen, die helpen reguleren hoe sterk corticale circuits op input reageren. In zowel het valproïnezuur‑ als het maternale immuun‑activatiemodel waren deze VIP‑cellen in de cortex sterk verminderd, terwijl de meeste andere interneurontypes grotendeels gespaard bleven. Terugstuderend naar de oorsprong van deze cellen in een foetale hersenregio, de caudale ganglionaire eminentie, ontdekten ze dat voorlopercellen daar excessief deelden maar niet goed overschakelden naar post‑mitotische VIP‑voorlopers en niet naar de cortex migreerden. Het patroon suggereerde dat overactieve Notch‑signaaltransductie deze voorlopercellen vastzette in een ‘nooit volwassen worden’ toestand, wat leidt tot een blijend tekort aan VIP‑interneuronen en een verschuiving naar overmatige excitatie.
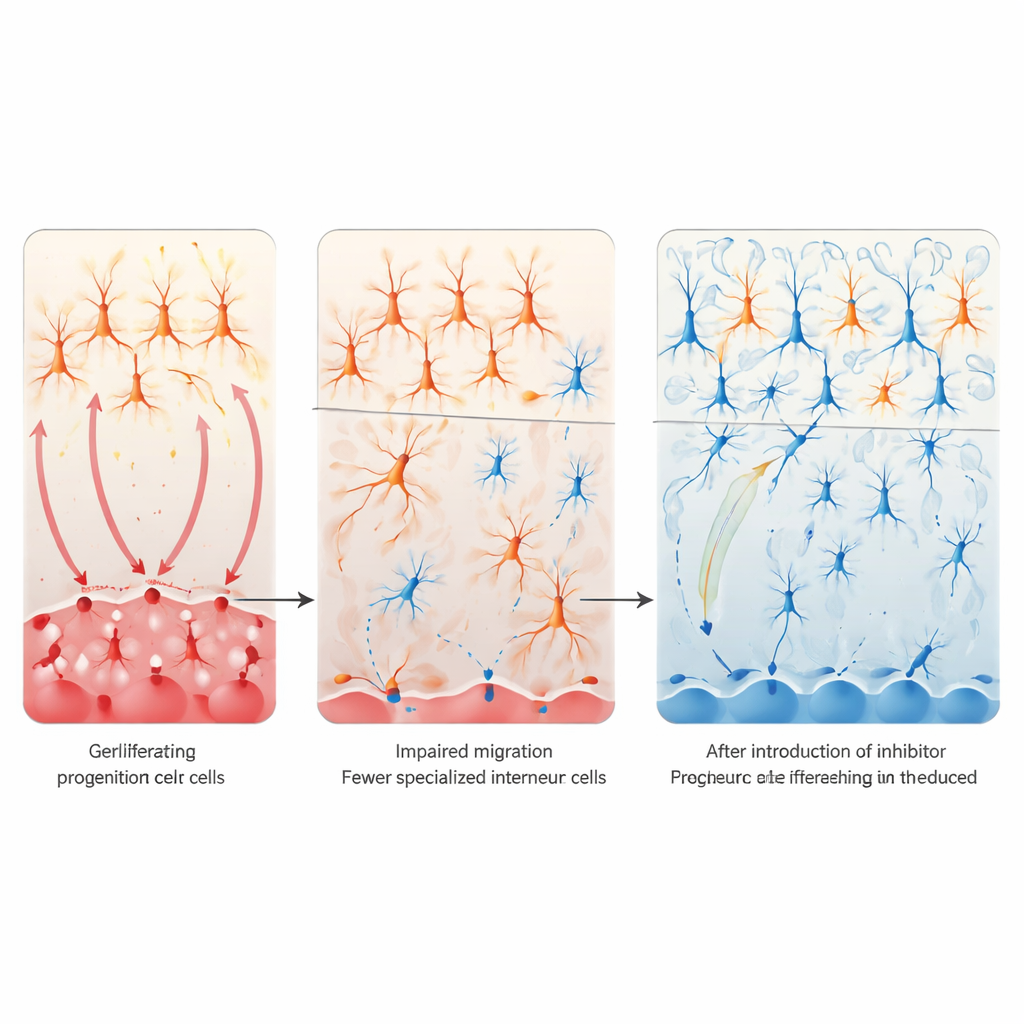
Notch dempen om hersencircuits te herstellen
De volgende vraag was of het kalmeren van Notch‑signaaltransductie deze defecten kon herstellen. In celkweek verminderde het forceren van de actieve vorm van de Notch‑receptor in zich ontwikkelende voorhersencellen markers van VIP‑interneuronen, terwijl het genetisch blokkeren van Notch of het gebruik van een γ‑secretaseremmer het tegenovergestelde effect had en VIP‑markers kon herstellen, zelfs na blootstelling aan valproïnezuur. In levende muizen verwijderde het team selectief Notch1 en Notch2 in cellen afkomstig uit de caudale ganglionaire eminentie. Deze lokale genetische ‘rem’ voorkwam het verlies van corticale VIP‑interneuronen en normaliseerde grotendeels sociaal gedrag bij nakomelingen die tijdens de zwangerschap aan valproïnezuur waren blootgesteld. Transcriptomische analyse van volwassen hersenen liet zien dat dit herstel ook een abnormale opwaartse regulatie van genen gekoppeld aan exciterende glutamaat‑synapsen dempte, wat suggereert dat het herstellen van remmende VIP‑circuits helpt bredere corticale netwerken in balans te brengen.
Een eenmalig prenataal geneesmiddel dat ontwikkeling hervormt
Aangezien genetische ingrepen niet praktisch zijn bij mensen, testten de onderzoekers een op medicatie gebaseerde strategie. Ze gebruikten Ro4929097, een krachtige γ‑secretaseremmer die eerder is onderzocht in kanker‑ en Alzheimer‑studies, en gaven één dosis aan drachtige muizen samen met valproïnezuur. Deze korte prenatale behandeling verlaagde de niveaus van actieve Notch‑eiwitten, herstelde grotendeels het aantal VIP‑interneuronen in de cortex van de nakomelingen en verbeterde meerdere ASS‑achtige gedragingen, waaronder repetitief verzorgen en sociale tekorten. Single‑cell RNA‑sequencing van pasgeboren hersenen toonde aan dat het middel niet alleen de VIP‑lijn normaliseerde; het corrigeerde ook bredere verstoringen in neurale voorlopercellen, oligodendrocyten (myeline‑vormende cellen) en andere celpopulaties, waardoor de algehele cellulaire samenstelling weer dichter bij die van controle‑dieren kwam.
Wat dit betekent voor begrip en behandeling van autisme
Voor niet‑specialisten is de kernboodschap dat diverse autismegerelateerde invloeden kunnen samenkomen op een gemeenschappelijke ‘schakelcentrale’ in de zich ontwikkelende hersenen. Wanneer het Notch‑pad tijdens een kritisch foetaal venster in de ‘aan’‑stand blijft staan, falen belangrijke remmende zenuwcellen om te rijpen en raakt het corticale circuit uit balans, wat bijdraagt aan sociale en gedragsproblemen. Bij muizen kan zorgvuldig getimede demping van dit pad — hetzij in specifieke celtypes, hetzij met een eenmalige prenatale dosis medicatie — grotendeels normale ontwikkeling en gedrag herstellen. Het vertalen van zo’n aanpak naar mensen vereist grote voorzichtigheid, maar deze bevindingen wijzen op Notch‑signaaltransductie, en in het bijzonder de ontwikkeling van VIP‑interneuronen, als veelbelovende doelen voor vroege interventies die mogelijk sommige vormen van ASS‑gerelateerde hersendysfunctie kunnen voorkomen.
Bronvermelding: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Trefwoorden: autisme spectrum stoornis, Notch‑signaaltransductie, VIP‑interneuronen, neuroontwikkeling, epigenetica