Clear Sky Science · sv
Riktad hämning av Notch‑signalering för att återställa neuralt utveckling och beteende i musmodeller för ASD
Varför denna forskning är viktig för familjer och samhället
Autismspektrumtillstånd (ASD) påverkar hur människor kommunicerar, umgås och reagerar på omvärlden, men dess biologiska rötter är fortfarande svårbegripliga. Denna studie i möss tar itu med en central fråga: leder mycket olika riskfaktorer för autism — gener, infektioner under graviditet eller vissa läkemedel — till samma störning i en hjärnväg? Forskarna hittar en gemensam rubbning i ett utvecklingsmässigt signalsystem kallat Notch och visar att en kontrollerad dämpning av denna väg före födseln kan återställa mer normal hjärnkoppling och socialt beteende i flera ASD‑lika musmodeller.
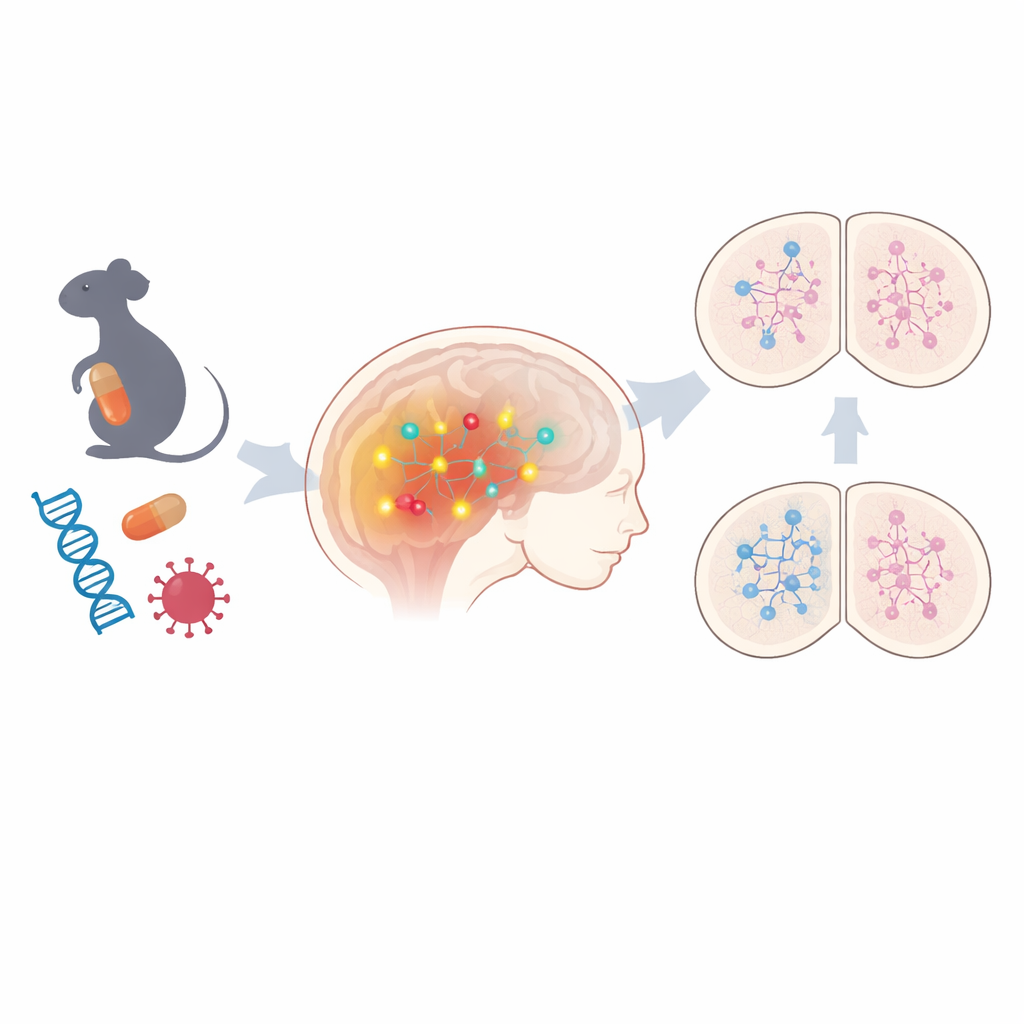
En gemensam väg bakom många olika risker
Teamet började med att undersöka fosterhjärnor från två icke‑genetiska ASD‑modeller: en där dräktiga möss exponerades för antiepileptikumet valproinsyra, och en annan som efterliknade maternell virusinfektion. Genom omfattande genaktivitetsprofilering fann de att hundratals gener var förändrade i båda modellerna, med tydliga tecken på störd epigenetisk reglering — kemiska markörer som slår på eller av gener utan att ändra DNA. Bland de delade förändringarna framträdde en väg särskilt tydligt: Notch‑signalering, en central regulator av hur omogna hjärnceller bestämmer vilken celltyp de ska bli. Komponenter i denna väg, inklusive kärnreceptorer och nedströms effektorer, var konsekvent uppreglerade. När forskarna tittade på människobaserade stamcellsneuroner som bär vissa autismkopplade genetiska varianter såg de återigen förhöjd Notch‑relaterad genaktivitet i flera fall, vilket antyder att denna väg kan vara en gemensam nämnare för både miljö‑ och ärftliga former av ASD.
Sårbara hjärnceller som finjusterar aktivitet
För att förstå konsekvenserna av överaktiv Notch fokuserade forskarna på balansen mellan excitatorisk och inhibitorisk signalering i cortex — ett område som ofta är rubbat vid autism. De inriktade sig på en liten population inhibitoriska nervceller kallade VIP‑interneuroner, som hjälper till att reglera hur starkt kortikala kretsar svarar på input. I både valproinsyra‑ och maternell immunaktiveringsmodeller var dessa VIP‑celler dramatiskt reducerade i cortex, medan de flesta andra interneurontyper i huvudsak var förskonade. Genom att följa cellernas ursprung till en fosterhjärnregion kallad caudal ganglionic eminence fann de att progenitorceller där överprolifererade men misslyckades med att korrekt differentiera till post‑mitotiska VIP‑prekursorer och migrera till cortex. Mönstret talade för att överaktiv Notch‑signalering fångade dessa progenitorer i ett "aldrig bli vuxen"‑tillstånd, vilket ledde till en bestående brist på VIP‑interneuroner och en lutning mot överdriven excitation.
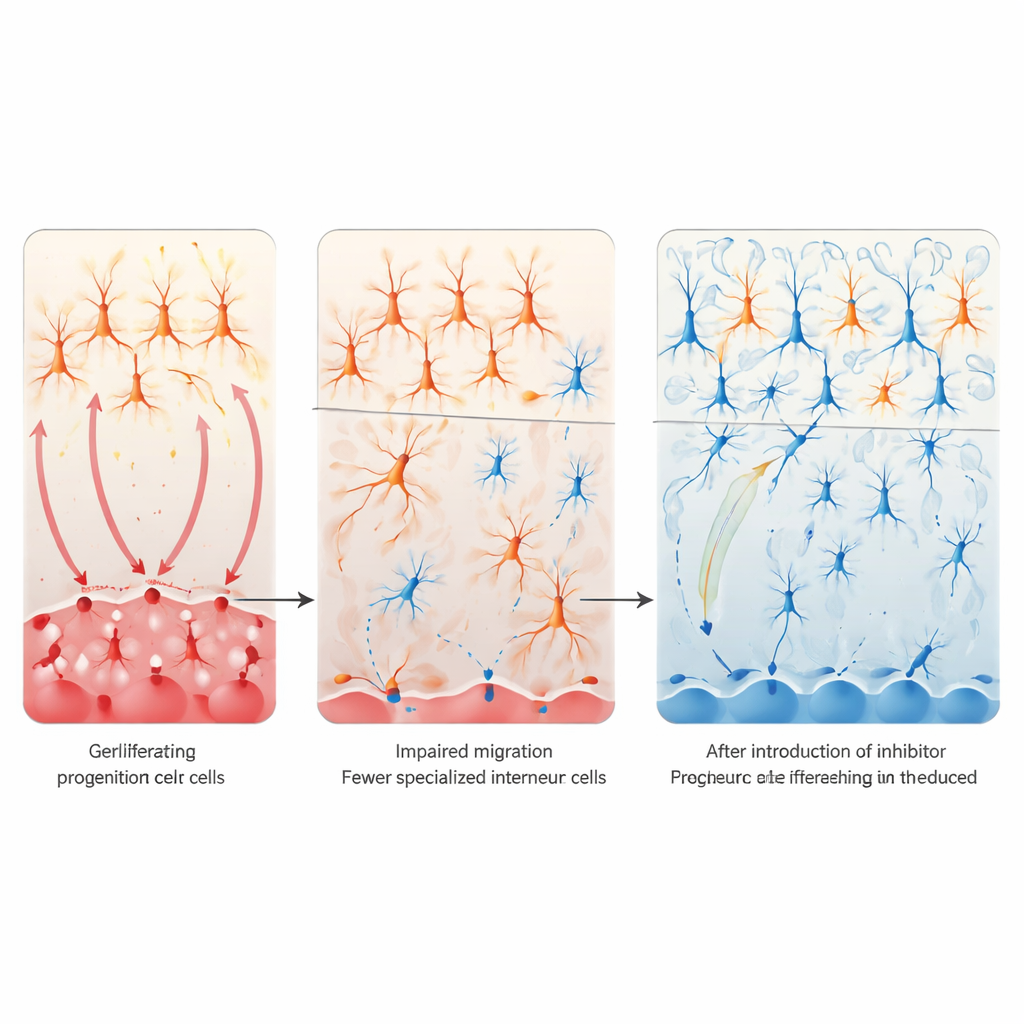
Dämpning av Notch för att rädda hjärnkretsar
Nästa fråga var om en lugnare Notch‑signalering kunde åtgärda dessa defekter. I cellkultur minskade införandet av den aktiva formen av Notch‑receptorn i utvecklande främre hjärnceller markörer för VIP‑interneuroner, medan genetisk blockering av Notch eller behandling med en γ‑sekretas‑hämmare gav motsatt effekt och kunde återställa VIP‑markörer även efter valproinsyraexponering. I levande möss selektivt raderade teamet Notch1 och Notch2 i celler härstammande från caudal ganglionic eminence. Denna lokala genetiska "broms" förhindrade förlusten av kortikala VIP‑interneuroner och normaliserade till stor del socialt interaktionsbeteende hos avkommor som exponerats för valproinsyra under dräktigheten. Transkriptomanalys av vuxna hjärnor visade att denna räddning också dämpade en onormal uppreglering av gener kopplade till excitatoriska glutamatsynapser, vilket tyder på att återställandet av inhibitoriska VIP‑kretsar bidrar till att återbalansera bredare kortikala nätverk.
En engångsdos prenatal medicin som omformar utvecklingen
Då genetiska ingrepp inte är praktiska hos människor testade forskarna en läkemedelsbaserad strategi. De använde Ro4929097, en potent γ‑sekretas‑hämmare som tidigare utvärderats i cancer‑ och Alzheimersstudier, och administrerade en singeldos till dräktiga möss tillsammans med valproinsyra. Denna korta prenatala behandling reducerade nivåerna av aktivt Notch‑protein, återställde i stort sett antalet VIP‑interneuroner i avkommornas cortex och förbättrade flera ASD‑lika beteenden, inklusive repetitiv putsning och sociala brister. Enkelcells‑RNA‑sekvensering av nyfödda hjärnor visade att läkemedlet inte bara normaliserade VIP‑linjen; det korrigerade också bredare störningar i neurala progenitorer, oligodendrocyter (myelinskapande celler) och andra cellpopulationer och sköt därigenom den övergripande cellulära sammansättningen mot den som sågs hos kontroll‑djur.
Vad detta betyder för förståelsen och behandlingen av autism
För en lekman är huvudbudskapet att olika autismrelaterade påverkningar kan konvergera på en gemensam "kopplingspanel" i den utvecklande hjärnan. När Notch‑vägen sitter fast i "på"‑läge under ett kritiskt fönster i fosterlivet misslyckas viktiga inhibitoriska nervceller att mogna och kortikala kretsar blir obalanserade, vilket bidrar till sociala och beteendemässiga problem. I möss kan tidsmässigt väl avvägd dämpning av denna väg — antingen i specifika celltyper eller med en enda prenatal läkemedelsdos — i stor utsträckning återställa normal utveckling och beteende. Att översätta en sådan strategi till människor kräver stor försiktighet, men dessa resultat pekar på Notch‑signalering, och i synnerhet utvecklingen av VIP‑interneuroner, som lovande mål för tidiga interventioner som syftar till att förebygga åtminstone vissa former av ASD‑relaterad hjärndysfunktion.
Citering: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Nyckelord: autismspektrumtillstånd, Notch‑signalering, VIP‑interneuroner, neuroutveckling, epigenetik