Clear Sky Science · de
Gezielte Beeinflussung der Notch-Signalgebung zur Wiederherstellung der neuronalen Entwicklung und des Verhaltens in Mausmodellen von ASD
Warum diese Forschung für Familien und die Gesellschaft wichtig ist
Die Autismus-Spektrum-Störung (ASD) beeinflusst, wie Menschen kommunizieren, sozial interagieren und auf ihre Umwelt reagieren — doch ihre biologischen Ursachen sind weiterhin rätselhaft. Diese Studie an Mäusen geht einer zentralen Frage nach: Stören sehr unterschiedliche Risikofaktoren für Autismus — Gene, Infektionen während der Schwangerschaft oder bestimmte Medikamente — letztlich denselben Hirnweg? Die Forschenden zeigen eine gemeinsame Fehlregulation in einem Entwicklungs-Signalweg namens Notch und belegen, dass ein gezieltes Herunterregeln dieses Weges vor der Geburt das Gehirnverdrahtungsmuster und soziales Verhalten in mehreren ASD-ähnlichen Mausmodellen weitgehend wiederherstellen kann.
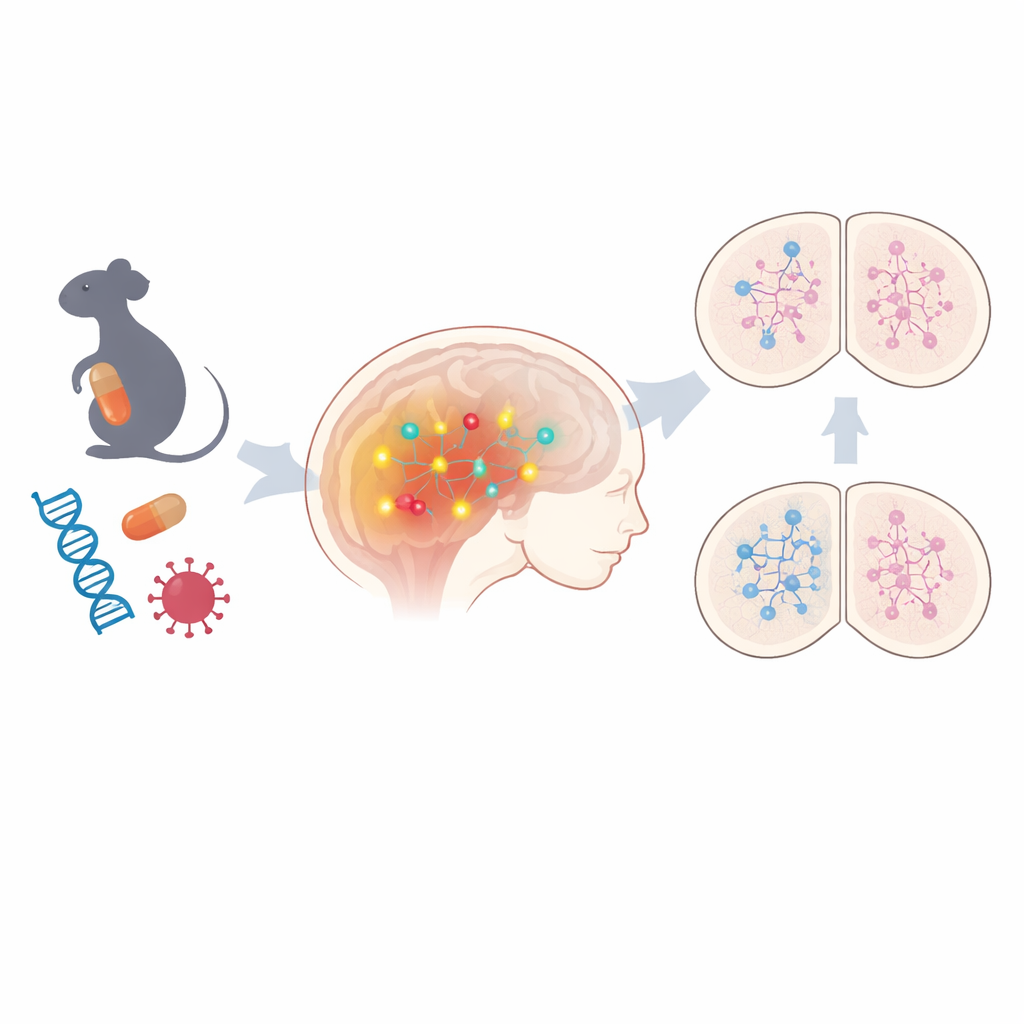
Ein gemeinsamer Weg hinter vielen unterschiedlichen Risiken
Das Team begann mit der Untersuchung fetaler Mäusehirne aus zwei nicht-genetischen ASD-Modellen: einem, bei dem trächtige Mäuse dem Antiepileptikum Valproinsäure ausgesetzt wurden, und einem anderen, das eine mütterliche Virusinfektion nachahmt. Durch umfassende Genaktivitätsprofile fanden sie, dass in beiden Modellen Hunderte Gene verändert waren, mit starken Hinweisen auf gestörte epigenetische Regulation — chemische Markierungen, die Gene an- oder ausschalten, ohne die DNA zu verändern. Unter den gemeinsamen Veränderungen stach ein Weg hervor: die Notch-Signalgebung, ein zentraler Regulator dafür, wie unreife Gehirnzellen entscheiden, welcher Neuronentyp sie werden. Komponenten dieses Weges, einschließlich Kernrezeptoren und nachgeschalteter Effektoren, waren durchweg erhöht. Als die Wissenschaftler menschliche, auf Stammzellen basierende Neuronenmodelle mit einigen autismus-assoziierten Genvarianten untersuchten, sahen sie in mehreren Fällen erneut eine verstärkte Notch-assoziierte Genaktivität, was darauf hindeutet, dass dieser Signalweg eine gemeinsame Verbindung zwischen umweltbedingten und erblichen Formen von ASD sein könnte.
Verwundbare Gehirnzellen, die die Aktivität feinabstimmen
Um die Folgen einer Notch-Überaktivität zu verstehen, konzentrierten sich die Forschenden auf das Gleichgewicht zwischen exzitatorischer und inhibitorischer Signalgebung im Kortex — das bei Autismus oft gestört ist. Sie richteten den Blick auf eine kleine Population inhibitorischer Nervenzellen, sogenannte VIP-Interneurone, die helfen zu regulieren, wie stark kortikale Schaltkreise auf Eingaben reagieren. In beiden Modellen — Valproinsäure und maternale Immunaktivierung — waren diese VIP-Zellen im Kortex dramatisch reduziert, während die meisten anderen Interneurontypen weitgehend verschont blieben. Zurückverfolgt bis zu einer fetalen Hirnregion, der kaudalen ganglionären Eminenz, zeigten die Untersuchungen, dass dortige Vorläuferzellen übermäßig proliferierten, aber nicht richtig in postmitotische VIP-Vorläufer übergingen und in den Kortex migrierten. Das Muster deutete darauf hin, dass eine überaktive Notch-Signalgebung diese Vorläufer in einem "niemals erwachsen werden"-Zustand festhält, was zu einem nachhaltigen Mangel an VIP-Interneuronen und einer Neigung zu übermäßiger Erregung führt.
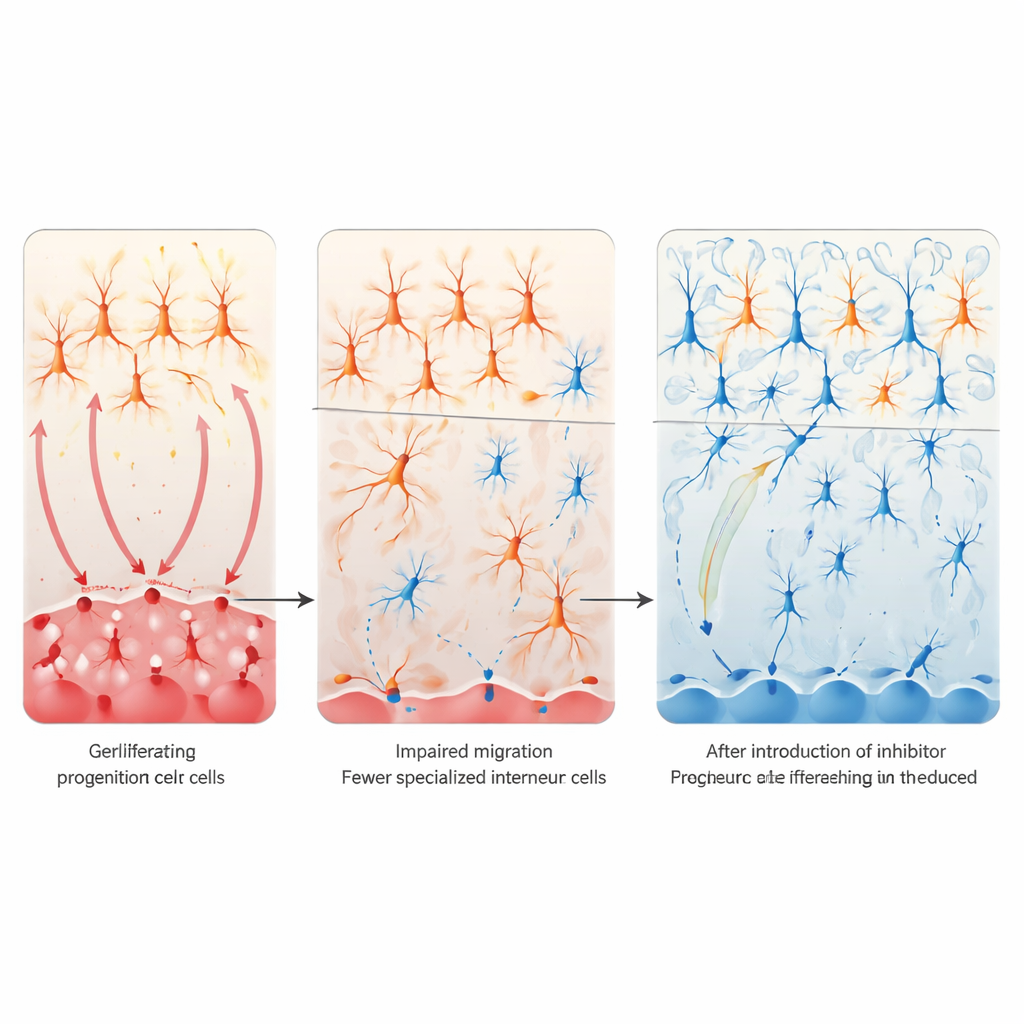
Notch drosseln, um Schaltkreise zu retten
Die nächste Frage war, ob eine Beruhigung der Notch-Signalgebung diese Defekte beheben kann. In Zellkultur reduzierte das erzwungene Einbringen der aktiven Form des Notch-Rezeptors in sich entwickelnde Vorderhirnzellen Marker für VIP-Interneurone, während das genetische Blockieren von Notch oder die Anwendung eines γ-Sekretase-Inhibitors den gegenteiligen Effekt hatte und VIP-Marker sogar nach Valproinsäure-Exposition wiederherstellen konnte. In lebenden Mäusen löschte das Team selektiv Notch1 und Notch2 in Zellen, die aus der kaudalen ganglionären Eminenz stammen. Diese lokale genetische "Bremse" verhinderte den Verlust kortikaler VIP-Interneurone und normalisierte weitgehend soziale Interaktionsverhalten bei Nachkommen, die während der Gestation Valproinsäure ausgesetzt waren. Eine Transkriptomanalyse erwachsener Gehirne zeigte, dass diese Rettung auch eine abnorme Hochregulierung von Genen, die mit exzitatorischen Glutamatsynapsen verknüpft sind, abschwächte, was darauf hindeutet, dass die Wiederherstellung inhibitorischer VIP-Schaltkreise hilft, breitere kortikale Netzwerke neu auszubalancieren.
Ein einmalig pränatal verabreichtes Medikament, das Entwicklung umgestaltet
Da genetische Interventionen beim Menschen nicht praktikabel sind, prüften die Forschenden eine medikamentöse Strategie. Sie verwendeten Ro4929097, einen potenten γ-Sekretase-Inhibitor, der zuvor in Krebs- und Alzheimer-Studien untersucht wurde, und verabreichten eine Einzelgabe an trächtige Mäuse zusammen mit Valproinsäure. Diese kurzzeitige pränatale Behandlung senkte die aktiven Notch-Proteinspiegel, stellte die Zahl der VIP-Interneurone im Kortex der Nachkommen weitgehend wieder her und verbesserte mehrere ASD-ähnliche Verhaltensweisen, einschließlich repetitiven Putzens und sozialer Defizite. Einzelzell-RNA-Sequenzierungen neugeborener Gehirne zeigten, dass das Medikament nicht nur die VIP-Linie normalisierte; es korrigierte auch breitere Störungen in neuralen Vorläuferzellen, Oligodendrozyten (myelinbildende Zellen) und anderen Zellpopulationen und rückte die gesamte Zellzusammensetzung wieder näher an die Kontrolle heran.
Was das für das Verständnis und die Behandlung von Autismus bedeutet
Für Laien lautet die Kernaussage, dass unterschiedliche autismusbezogene Einflüsse auf ein gemeinsames "Schaltzentrum" im sich entwickelnden Gehirn zulaufen können. Wenn der Notch-Weg während eines kritischen fetalen Zeitfensters im "An"-Zustand verharrt, reifen wichtige inhibitorische Nervenzellen nicht aus, und kortikale Schaltkreise geraten aus dem Gleichgewicht, was zu sozialen und verhaltensbezogenen Problemen beiträgt. Bei Mäusen kann ein sorgfältig getimtes Absenken dieses Weges — entweder in spezifischen Zelltypen oder durch eine einmalige pränatale Medikamentengabe — die normale Entwicklung und das Verhalten größtenteils wiederherstellen. Die Übertragung eines solchen Ansatzes auf Menschen erfordert zwar große Vorsicht, doch heben diese Befunde die Notch-Signalgebung und insbesondere die Entwicklung der VIP-Interneurone als vielversprechende Ziele für frühzeitige Interventionen hervor, die darauf abzielen, zumindest einige Formen der ASD-assoziierten Gehirnfehlfunktion zu verhindern.
Zitation: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Schlüsselwörter: Autismus-Spektrum-Störung, Notch-Signalgebung, VIP-Interneurone, Neuroentwicklung, Epigenetik