Clear Sky Science · ar
استهداف إشارات نوتش لاستعادة التطور العصبي والسلوك في نماذج الفأر للتوحد
لماذا يهم هذا البحث للعائلات والمجتمع
يؤثر اضطراب طيف التوحد (ASD) على كيفية تواصل الأشخاص وتفاعلهم اجتماعياً واستجابتهم للعالم من حولهم، ومع ذلك تظل جذوره البيولوجية محيرة. يتناول هذا البحث في الفئران سؤالاً كبيراً: هل تؤدي عوامل الخطر المختلفة جداً للتوحد—مثل الجينات، أو الالتهابات أثناء الحمل، أو بعض الأدوية—إلى اضطراب نفس المسار الدماغي؟ يكشف الباحثون عن اضطراب مشترك في نظام إشارات تطوري يُسمى نوتش ويظهرون أن خفض نشاط هذا المسار بعناية قبل الولادة يمكن أن يستعيد توصيل الدماغ وسلوكيات اجتماعية أقرب إلى الطبيعي في عدة نماذج فأرية تشبه التوحد.
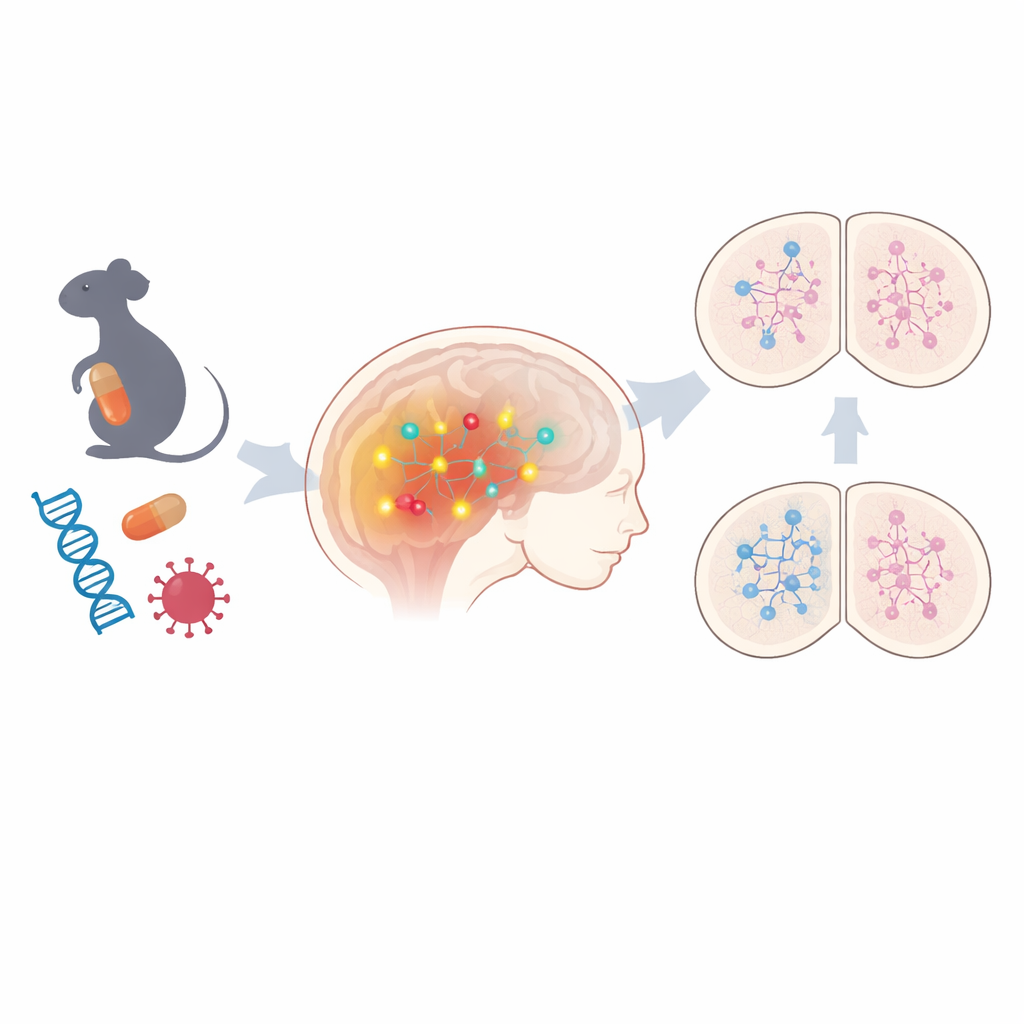
مسار مشترك وراء مخاطر مختلفة
بدأ الفريق بفحص أدمغة أجنة الفئران في نموذجين للتوحد غير وراثيين: أحدهما حيث تعرضت الفئران الحامل لدواء مضاد للاختلاجات يُدعى حمض الفالبرويك، والآخر يحاكي إصابة أمية فيروسية. باستخدام تصوير واسع لنشاط الجينات، وجدوا أن مئات الجينات تغيرت في كلا النموذجين، مع دلائل قوية على اضطراب في التنظيم فوق الجيني—وهي علامات كيميائية تُشغّل أو تُطفئ الجينات دون تغيير الحمض النووي نفسه. من بين التغيرات المشتركة، اِرتَقى مسار واحد للواجهة: إشارات نوتش، وهو متحكم أساسي في كيفية قرار الخلايا الدماغية غير الناضجة نوع الخلية العصبية التي ستصبحها. كانت مكونات هذا المسار، بما في ذلك المستقبلات الجوهرية والعوامل الفعالة لاحقاً، مرفوعة باستمرار. وعندما نظر العلماء إلى نماذج عصبية مشتقة من خلايا جذعية بشرية تحمل بعض الطفرات المرتبطة بالتوحد، رأوا مرة أخرى نشاطاً جينياً مرتفعاً متعلقاً بنوتش في عدة حالات، مما يوحي بأن هذا المسار قد يكون خيطاً مشتركاً عبر الأشكال البيئية والوراثية للتوحد.
خلايا دماغية عرضة تعبّر عن الدقة في الضبط
لفهم عواقب فرط نشاط نوتش، ركز الباحثون على التوازن بين الإشارات المثبطة والمثيرة في القشرة—الذي يتعطل غالباً في التوحد. توقفوا عند مجموعة صغيرة من الخلايا العصبية المثبطة تُسمى الخلايا البينية VIP، التي تساعد في ضبط مدى استجابة دوائر القشرة للمُدخلات. في كل من نموذجي حمض الفالبرويك وتفعيل المناعة الأمومية، كانت هذه الخلايا VIP منخفضة بشكل كبير في القشرة، بينما ظلت معظم أنواع الخلايا البينية الأخرى محفوظة إلى حد كبير. وبإرجاع أصل هذه الخلايا إلى منطقة جنينية جنوبية تُدعى الذروة العقدية الخلفية (caudal ganglionic eminence)، وجدوا أن الخلايا المُنزِعة هناك كانت تتكاثر بشكل مفرط لكنها تفشل في الانتقال بشكل صحيح إلى خلايا منشأ VIP بعد الانقسام والهجرة إلى القشرة. يشير النمط إلى أن فرط نشاط نوتش كان يحبس هذه الخلايا الجذعية في حالة «لا تكبر أبداً»، مما يؤدي إلى نقص دائم في خلايا VIP وانحراف نحو إثارة مفرطة.
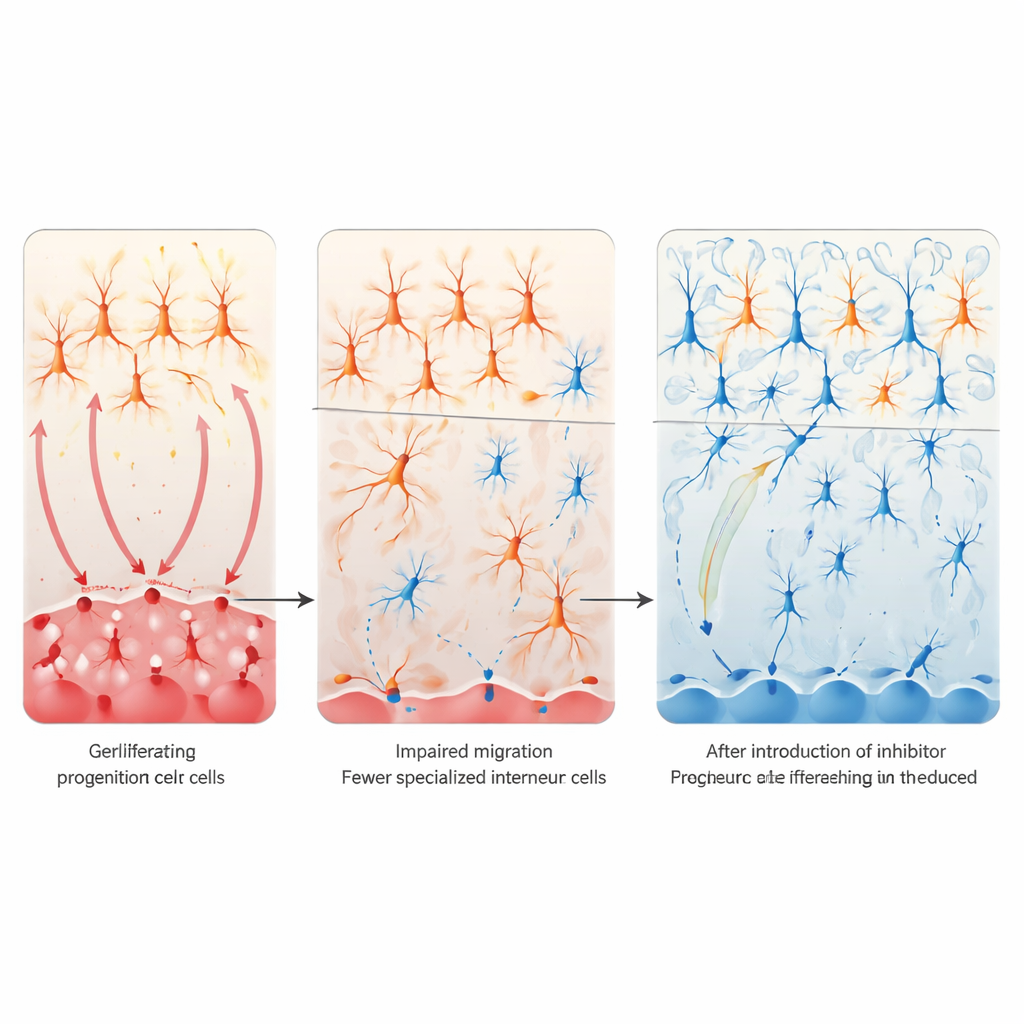
خفض نوتش لإنقاذ دوائر الدماغ
كان السؤال التالي ما إذا كان تهدئة إشارات نوتش يمكن أن يصلح هذه العيوب. في زراعة الخلايا، أدى إجبار الشكل النشط لمستقبل نوتش إلى الخلايا المتطورة في الدماغ الأمامي إلى تقليل علامات خلايا VIP، في حين أن حجب نوتش وراثياً أو باستخدام مثبط غاما-سِكرتاز أدى إلى العكس وكان بإمكانه استعادة علامات VIP حتى بعد التعرض لحمض الفالبرويك. في الفئران الحية، حَذَف الفريق بشكل انتقائي Notch1 و Notch2 في الخلايا المشتقة من الذروة العقدية الخلفية. منعت هذه «الكابح» الجيني المحلي فقدان خلايا VIP القشرية وقَطْعَتْ إلى حد كبير تَطَبُّع سلوكيات التفاعل الاجتماعي في النسل الذي تعرّض أثناء الحمل لحمض الفالبرويك. أظهر تحليل النصوص الجينية لأدمغة البالغين أن هذا الإنقاذ خفّض أيضاً زيادة غير طبيعية في التعبير عن جينات مرتبطة بمشابك الغلوتامات المثيرة، مما يشير إلى أن استعادة دوائر VIP المثبطة يساعد في إعادة توازن الشبكات القشرية الأوسع.
دواء واحد قبل الولادة يعيد تشكيل التطور
لأن التدخلات الجينية غير عملية للبشر، اختبر الباحثون استراتيجية دوائية. استخدموا Ro4929097، وهو مثبط قوي لغاما-سِكرتاز تمت تجربته سابقاً في تجارب السرطان ومرض ألزهايمر، وأعطوا جرعة واحدة للفئران الحامل مع حمض الفالبرويك. خفض هذا العلاج القصير قبل الولادة مستويات بروتين نوتش النشط، واستعاد إلى حد كبير أعداد خلايا VIP في قشرة ذراري الفئران، وحسّن عدة سلوكيات شبيهة بالتوحد، بما في ذلك التهيّج التكراري ونواقص التفاعل الاجتماعي. أظهرت تقنية تسلسل RNA لخلايا مفردة في أدمغة حديثي الولادة أن الدواء لم يطَبّع فقط سلالة VIP؛ بل صحح أيضاً اضطرابات أوسع في الخلايا الجذعية العصبية، والخلايا قليلة التغصن (الخلايا المكونة للمايلين)، وسكان خلوية أخرى، ما دفع التركيب الخلوي العام نحو ما يُرى في الحيوانات الضابطة.
ماذا يعني هذا لفهم وعلاج التوحد
للقارئ العام، الخلاصة هي أن تأثيرات مرتبطة بالتوحد ومتنوعة قد تتلاقى على «لوحة مفاتيح» مشتركة في الدماغ النامي. عندما يعلق مسار نوتش في وضعية «تشغيل» خلال نافذة جنينية حساسة، تفشل خلايا عصبية مثبطة رئيسية في النضوج، وتصبح الدوائر القشرية غير متوازنة، مما يسهم في مشاكل اجتماعية وسلوكية. في الفئران، يؤدي تهدئة هذا المسار في توقيت دقيق—سواء في أنواع خلوية محددة أو بجرعة دوائية واحدة قبل الولادة—إلى استعادة التطور والسلوك إلى حد كبير. وبينما سيتطلب نقل مثل هذا النهج إلى البشر حذراً بالغاً، تبرز هذه النتائج إشارات نوتش، وبشكل خاص تطور خلايا VIP البينية، كأهداف واعدة لتدخلات مبكرة تهدف إلى منع بعض أشكال خلل الدماغ المرتبط بالتوحد.
الاستشهاد: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
الكلمات المفتاحية: اضطراب طيف التوحد, إشارات نوتش, خلية القشرة الحاجبة VIP, التطور العصبي, علم فوق الجينات (الإيبيجنتيك)