Clear Sky Science · ja
ノッチシグナル伝達を標的にしてマウスASDモデルの神経発達と行動を回復する
家族と社会にとってこの研究が重要な理由
自閉スペクトラム症(ASD)は、人々のコミュニケーションや社会的相互作用、周囲への反応の仕方に影響を与えますが、その生物学的な根底はまだ完全には解明されていません。本論文はマウスを用いて大きな問いに取り組みます:遺伝的要因、妊娠中の感染、あるいは特定の薬剤のような非常に異なるリスク因子が、最終的に同じ脳回路を乱すのか?研究者たちは、ノッチと呼ばれる発生期のシグナル伝達系に共通の乱れを見いだし、出生前にこの経路の活動を慎重に抑えることで、いくつかのASD様マウスモデルにおいてより正常な脳配線と社会的行動を回復できることを示しました。
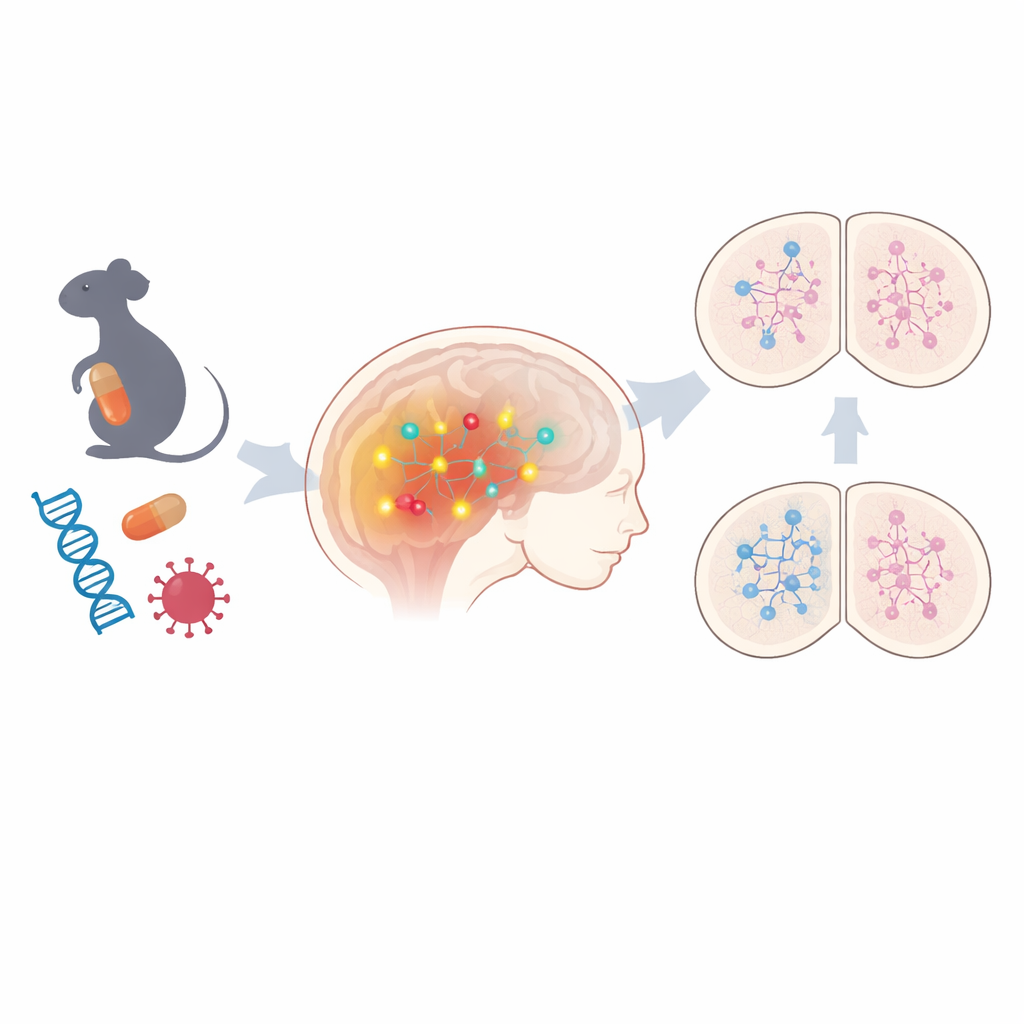
さまざまなリスクに共通する経路
研究チームはまず、非遺伝性のASDモデルである二つの胎児マウス脳を調べました:妊娠マウスが抗けいれん薬バルプロ酸にさらされたモデルと、母体のウイルス感染を模したモデルです。広範な遺伝子発現プロファイリングにより、両モデルで数百の遺伝子が変動し、DNAそのものを変えずに遺伝子のオン・オフを制御する化学的マーキングであるエピジェネティックな調節の乱れの強いシグネチャーが見られました。共通の変化の中で際立っていたのがノッチシグナル伝達でした。これは未熟な脳細胞がどの神経細胞タイプになるかを決める主要な制御系です。この経路の構成要素、コアとなる受容体や下流のエフェクターが一貫して活性化されていました。研究者らが一部の自閉関連遺伝子変異を持つヒト幹細胞由来ニューロンモデルを調べたところでも、いくつかの場合にノッチ関連遺伝子の活動亢進が見られ、環境因子と遺伝因子の双方にまたがってこの経路が共通の糸である可能性を示唆しました。
活動を微調整する脆弱な脳細胞
ノッチ過活動の結果を理解するために、研究者たちは皮質における興奮性と抑制性のシグナルバランスに注目しました—このバランスはしばしば自閉症で乱れます。彼らは、皮質回路の応答の強さを調節するVIPと呼ばれる小集団の抑制性ニューロンに着目しました。バルプロ酸と母体免疫活性化の両モデルで、これらのVIP細胞は皮質で著しく減少しており、他の多くの種類の介在ニューロンは概ね保たれていました。これらの細胞の起源を尾側神経節隆起(caudal ganglionic eminence)という胎児脳領域にさかのぼると、そこにある前駆細胞は過剰に増殖している一方で、適切に分化してポストミトーシスなVIP前駆細胞に切り替わり皮質へ移動することができていませんでした。このパターンは、ノッチシグナル伝達の過活動がこれらの前駆細胞を「成長しないまま」の状態に閉じ込め、持続的なVIP介在ニューロンの不足と過剰な興奮への傾きをもたらしていることを示唆していました。
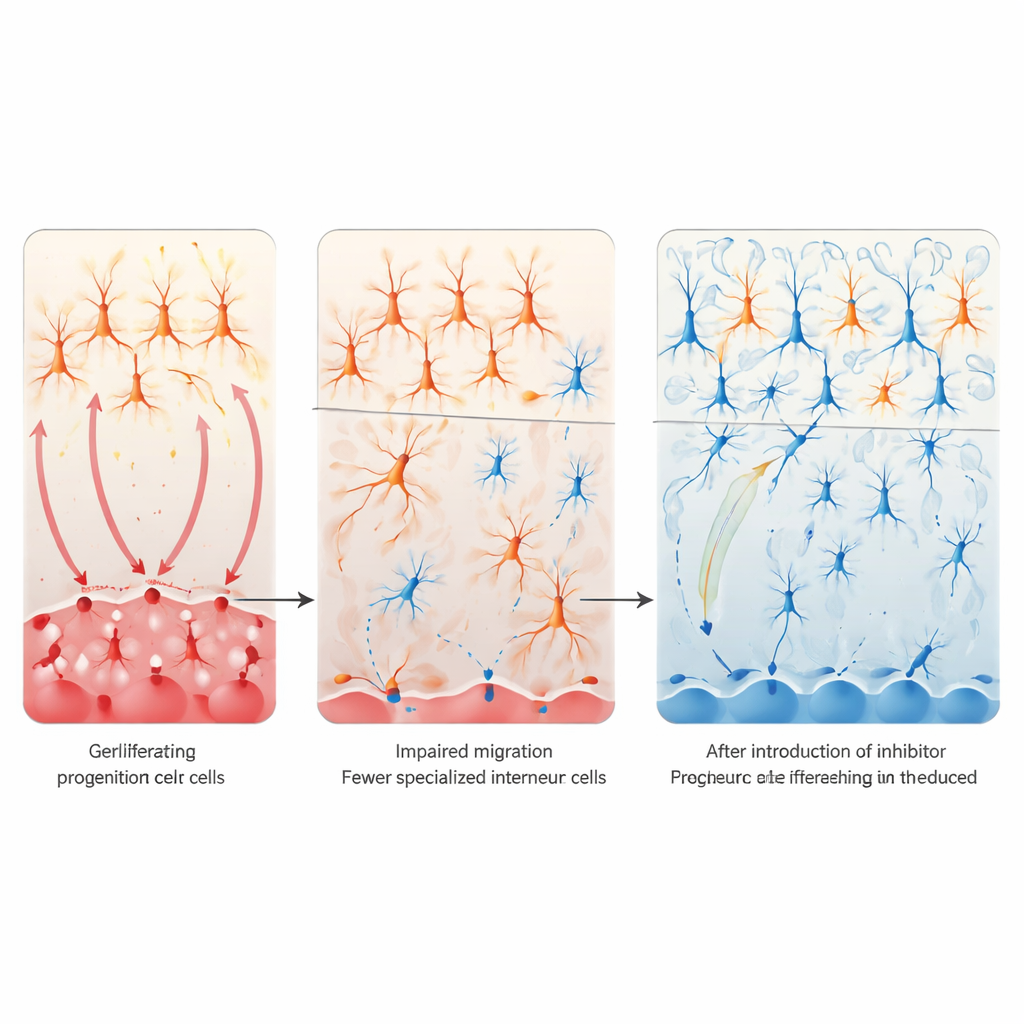
ノッチを抑えることで回路を救う
次の疑問は、ノッチシグナル伝達を穏やかにすることでこれらの欠陥を救えるかどうかでした。細胞培養では、ノッチ受容体の活性型を発達中の前脳細胞に強制発現させるとVIP介在ニューロンのマーカーが低下しました。一方、遺伝的にノッチを遮断するかγ-セクレターゼ阻害剤で抑えると逆の効果が現れ、バルプロ酸曝露後でもVIPマーカーを回復することができました。生体マウスでは、研究チームは尾側神経節隆起由来の細胞においてNotch1とNotch2を選択的に欠失させました。この局所的な遺伝的“ブレーキ”により、皮質VIP介在ニューロンの消失が防がれ、妊娠中にバルプロ酸に曝露された子孫の社会的相互作用行動は大部分で正常化しました。成体脳のトランスクリプトーム解析は、この回復が興奮性グルタミン酸シナプスに関連する遺伝子の異常な上方制御も抑えることを示しており、抑制的なVIP回路の回復がより広範な皮質ネットワークの再バランスに寄与することを示唆しています。
発達を形作る一回の出生前投与薬
遺伝子操作はヒトには実用的でないため、研究者たちは薬物ベースの戦略を試しました。彼らはRo4929097という強力なγ-セクレターゼ阻害剤(がんやアルツハイマーの試験で評価されたことがある)を用い、妊娠マウスにバルプロ酸と同時に単回投与しました。この短時間の出生前治療により、活性化されたノッチタンパク質レベルが低下し、子孫の皮質におけるVIP介在ニューロン数は概ね回復し、反復的なグルーミングや社会性欠損を含む複数のASD様行動が改善しました。新生児脳の単一細胞RNAシーケンスは、この薬がVIP系譜を正常化するだけでなく、神経前駆細胞、オリゴデンドロサイト(髄鞘形成細胞)、その他の細胞集団におけるより広範な乱れも是正し、全体の細胞組成を対照動物に近い状態へと押し戻したことを明らかにしました。
自閉症の理解と治療にとっての意義
一般向けの要点は、多様な自閉症関連影響が発達中の脳における共通の“スイッチボード”に収束する可能性があるということです。重要な胎児の時期にノッチ経路が「入りっぱなし」になると、主要な抑制性神経細胞が成熟できず、皮質回路のバランスが崩れて社会的および行動上の問題に寄与します。マウスでは、特定の細胞型での局所的な制御であれ単回の出生前薬物投与であれ、この経路を適切なタイミングで抑えることで発達と行動を大部分回復させることができます。こうしたアプローチをヒトに移すには慎重さが不可欠ですが、これらの発見はノッチシグナル伝達、特にVIP介在ニューロンの発達を、出生前の早期介入で少なくとも一部のASD関連脳機能障害を予防するための有望な標的として強調しています。
引用: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
キーワード: 自閉スペクトラム症, ノッチシグナル伝達, VIP抑制性介在ニューロン, 神経発達, エピジェネティクス