Clear Sky Science · it
Mirare la segnalazione Notch per ripristinare lo sviluppo neurale e il comportamento in modelli murini di ASD
Perché questa ricerca è importante per le famiglie e la società
Il disturbo dello spettro autistico (ASD) influisce su come le persone comunicano, socializzano e rispondono al mondo circostante, ma le sue radici biologiche restano enigmatiche. Questo studio nel topo affronta una grande domanda: fattori di rischio molto diversi per l’autismo — genetici, infezioni durante la gravidanza o alcuni farmaci — finiscono per perturbare lo stesso percorso cerebrale? I ricercatori rivelano una perturbazione condivisa in un sistema di segnalazione dello sviluppo chiamato Notch e mostrano che ridurre con attenzione questa via prima della nascita può ripristinare un wiring cerebrale e comportamenti sociali più normali in diversi modelli murini che imitano l’ASD.
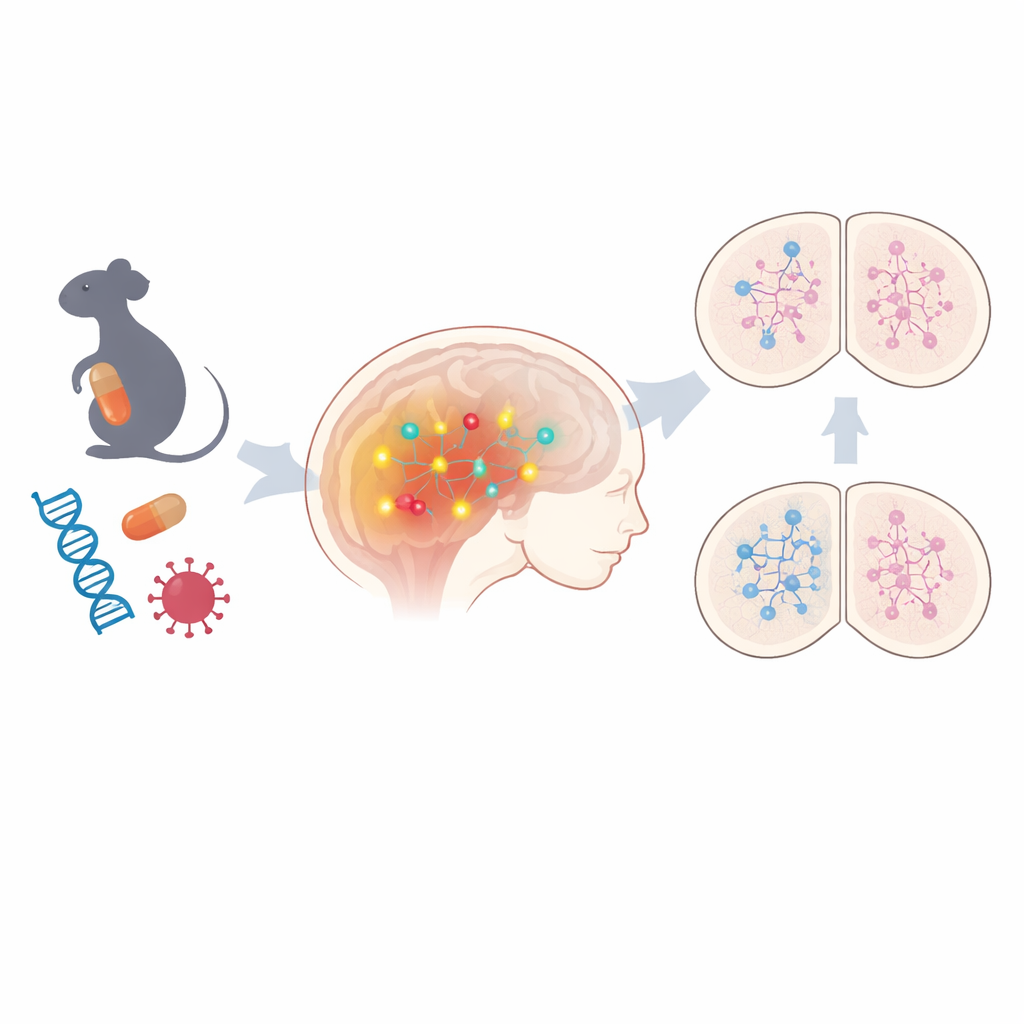
Una via comune dietro rischi molto diversi
Il gruppo ha iniziato esaminando cervelli fetali di topo in due modelli non genetici di ASD: uno in cui le femmine gravide erano esposte al farmaco anti-convulsivante acido valproico e un altro che imitava un’infezione materna virale. Tramite profilazione ampia dell’attività genica, hanno trovato che centinaia di geni risultavano alterati in entrambi i modelli, con marcati segnali di disfunzione dell’epigenetica — marchi chimici che accendono o spengono i geni senza cambiare il DNA. Tra i cambiamenti condivisi è emersa una via dominante: la segnalazione Notch, un controllore chiave di come le cellule cerebrali immature decidono quale tipo di neurone diventare. Componenti di questa via, inclusi recettori centrali ed effettori a valle, risultavano costantemente up-regolati. Quando gli scienziati hanno osservato modelli neuronali umani derivati da cellule staminali portatrici di varianti genetiche associate all’autismo, hanno di nuovo riscontrato un’attivazione aumentata di geni legati a Notch in diversi casi, suggerendo che questa via potrebbe essere un filo comune sia nelle forme ambientali che ereditarie di ASD.
Cellule cerebrali vulnerabili che modulano l’attività
Per comprendere le conseguenze di un’eccessiva attività di Notch, i ricercatori si sono concentrati sull’equilibrio tra segnali eccitatori e inibitori nella corteccia — spesso alterato nell’autismo. Hanno focalizzato l’attenzione su una piccola popolazione di neuroni inibitori chiamati interneuroni VIP, che aiutano a regolare quanto intensamente i circuiti corticali rispondono agli input. In entrambi i modelli murini, acido valproico e attivazione immunitaria materna, queste cellule VIP risultavano drasticamente ridotte nella corteccia, mentre la maggior parte degli altri tipi di interneuroni era in gran parte preservata. Tracciando l’origine di queste cellule fino a una regione fetale chiamata eminence gangliare caudale, hanno scoperto che le cellule progenitrici lì proliferavano eccessivamente ma non riuscivano a convertire correttamente in precursori VIP post-mitotici e a migrare nella corteccia. Il quadro suggeriva che la segnalazione Notch iperattiva intrappolava questi progenitori in uno stato di “mai maturare”, causando una carenza duratura di interneuroni VIP e un’inclinazione verso un’eccessiva eccitazione.
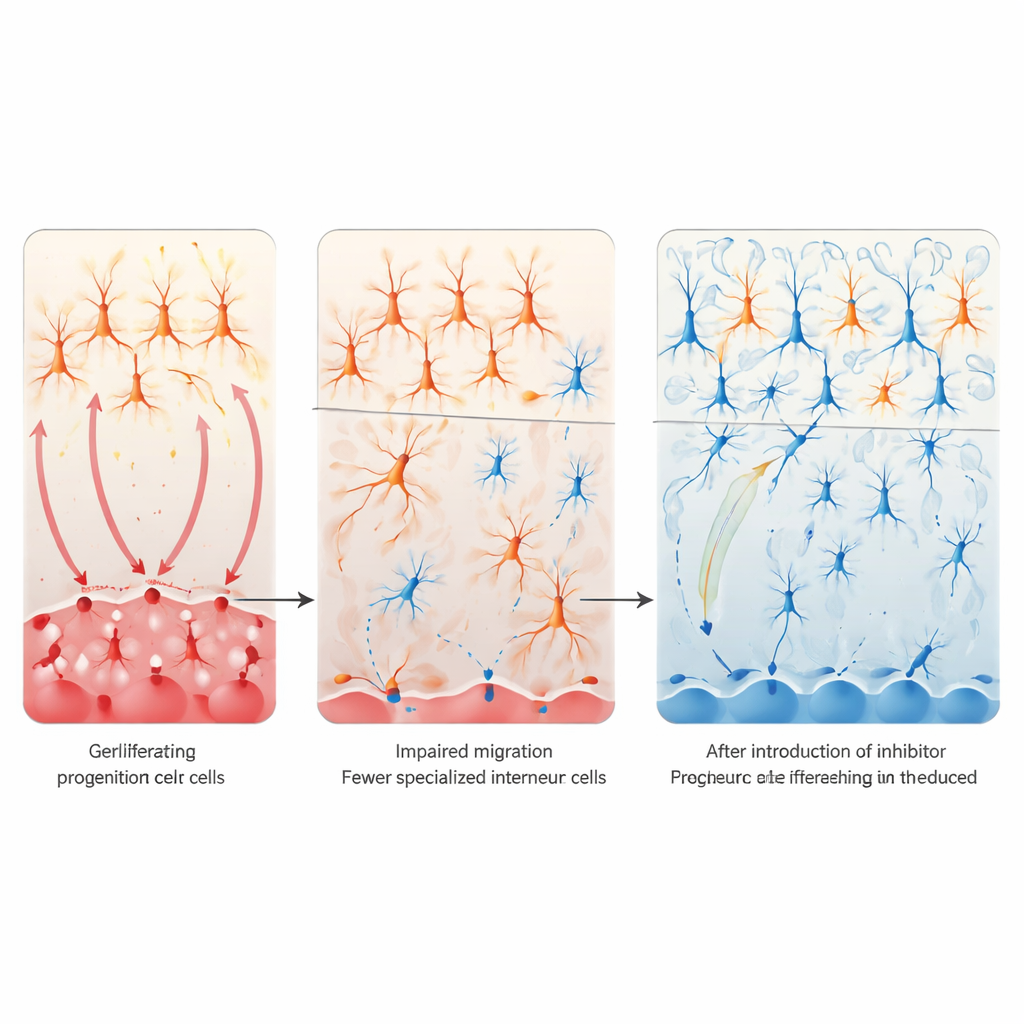
Abbassare Notch per recuperare i circuiti cerebrali
La domanda successiva era se calmare la segnalazione Notch potesse correggere questi difetti. in coltura cellulare, forzare la forma attiva del recettore Notch nelle cellule del proencefalo in sviluppo riduceva i marcatori degli interneuroni VIP, mentre bloccare Notch geneticamente o con un inibitore della γ‑secretasi produceva l’effetto opposto e poteva ripristinare i marcatori VIP anche dopo l’esposizione all’acido valproico. In topi vivi, il team ha eliminato selettivamente Notch1 e Notch2 nelle cellule derivate dall’eminence gangliare caudale. Questo “freno” genetico locale ha prevenuto la perdita di interneuroni VIP corticali e ha in gran parte normalizzato i comportamenti di interazione sociale nei cuccioli esposti all’acido valproico durante la gestazione. L’analisi trascrittomica di cervelli adulti ha mostrato che questo recupero ha anche attenuato un’anomala up‑regolazione di geni collegati alle sinapsi eccitatorie a base di glutammato, suggerendo che il ripristino dei circuiti inibitori VIP contribuisce a riequilibrare reti corticali più ampie.
Un singolo trattamento prenatale che rimodella lo sviluppo
Poiché interventi genetici non sono praticabili nell’uomo, i ricercatori hanno testato una strategia farmacologica. Hanno usato Ro4929097, un potente inibitore della γ‑secretasi già valutato in trial per il cancro e l’Alzheimer, e hanno somministrato una singola dose a topi gravidi insieme all’acido valproico. Questo breve trattamento prenatale ha ridotto i livelli di proteina Notch attiva, ha in gran parte ripristinato il numero di interneuroni VIP nella corteccia dei discendenti e ha migliorato molteplici comportamenti simili all’ASD, inclusi il grooming ripetitivo e i deficit sociali. Il sequenziamento dell’RNA a singola cellula nei cervelli neonatali ha rivelato che il farmaco non ha normalizzato solo la linea VIP; ha anche corretto più ampi disturbi nei progenitori neurali, negli oligodendrociti (cellule che formano la mielina) e in altre popolazioni cellulari, spingendo la composizione cellulare complessiva verso quella osservata negli animali di controllo.
Cosa significa per la comprensione e il trattamento dell’autismo
Per un non addetto ai lavori, il messaggio principale è che influenze diverse legate all’autismo possono convergere su un “quadro di comando” condiviso nel cervello in sviluppo. Quando la via Notch resta bloccata nella posizione “acceso” durante una finestra fetale critica, cellule nervose inibitorie chiave non maturano e i circuiti corticali si sbilanciano, contribuendo a problemi sociali e comportamentali. Nei topi, un’attenuazione temporizzata di questa via — sia in tipi cellulari specifici sia con una singola dose prenatale di farmaco — può in larga misura ripristinare uno sviluppo e un comportamento più normali. Sebbene tradurre tale approccio nell’uomo richiederà estrema cautela, questi risultati mettono in luce la segnalazione Notch, e in particolare lo sviluppo degli interneuroni VIP, come bersagli promettenti per interventi precoci volti a prevenire almeno alcune forme di disfunzione cerebrale correlate all’ASD.
Citazione: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Parole chiave: disturbo dello spettro autistico, segnalazione Notch, interneuroni VIP, neuro sviluppo, epigenetica