Clear Sky Science · pt
Direcionando a sinalização Notch para restaurar o desenvolvimento neural e o comportamento em modelos murinos de TEA
Por que esta pesquisa importa para famílias e para a sociedade
O transtorno do espectro autista (TEA) afeta a forma como as pessoas se comunicam, socializam e reagem ao mundo ao seu redor, mas suas raízes biológicas continuam enigmáticas. Este estudo em camundongos aborda uma pergunta importante: fatores de risco muito diferentes para o autismo — genes, infecções durante a gravidez ou certos medicamentos — acabam perturbando a mesma via cerebral? Os pesquisadores revelam uma perturbação comum em um sistema de sinalização do desenvolvimento chamado Notch e mostram que reduzir cuidadosamente essa via antes do nascimento pode restaurar uma conexão cerebral e comportamentos sociais mais normais em vários modelos murinos com traços semelhantes ao TEA.
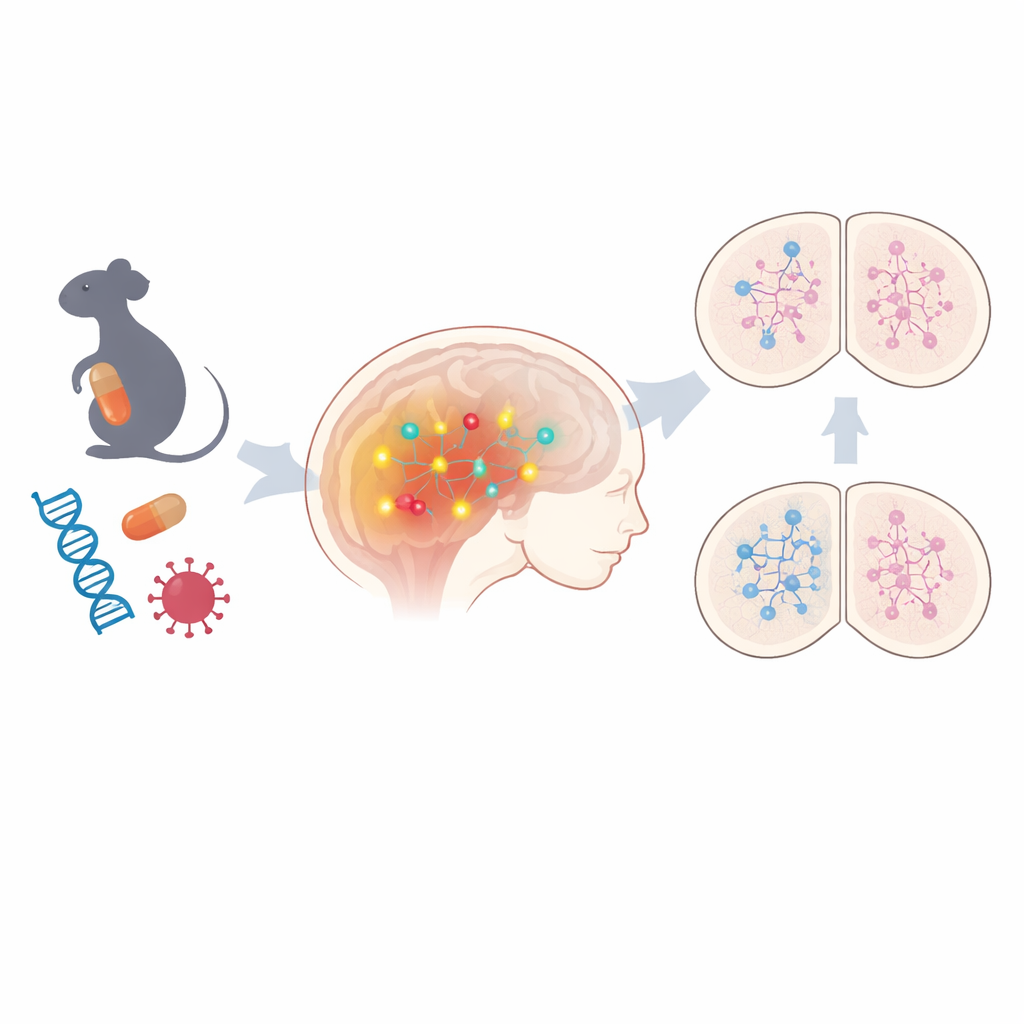
Uma via comum por trás de muitos riscos diferentes
A equipe começou examinando cérebros fetais de camundongos em dois modelos não genéticos de TEA: um em que fêmeas grávidas foram expostas ao medicamento anticonvulsivante valproato, e outro que imita infecção viral materna. Usando um perfil amplo de atividade gênica, eles descobriram que centenas de genes eram alterados em ambos os modelos, com fortes sinais de desregulação epigenética — marcas químicas que ligam ou desligam genes sem alterar o DNA em si. Entre as mudanças compartilhadas, uma via se destacou: a sinalização Notch, um controlador central de como células cerebrais imaturas decidem que tipo de neurônio se tornar. Componentes dessa via, incluindo receptores principais e efetores a jusante, foram consistentemente aumentados. Quando os cientistas analisaram modelos neuronais humanos derivados de células-tronco que carregavam algumas variantes genéticas associadas ao autismo, novamente observaram atividade gênica relacionada à Notch elevada em vários casos, sugerindo que essa via pode ser um fio comum entre formas ambientais e hereditárias do TEA.
Células cerebrais vulneráveis que ajustam a atividade
Para entender as consequências da hiperatividade da Notch, os pesquisadores se concentraram no equilíbrio entre sinalizações excitatórias e inibitórias no córtex — frequentemente perturbado no autismo. Eles focalizaram uma pequena população de células nervosas inibitórias chamadas interneurônios VIP, que ajudam a regular a intensidade com que os circuitos corticais respondem a estímulos. Em ambos os modelos, valproato e ativação imune materna, essas células VIP foram dramaticamente reduzidas no córtex, enquanto a maioria dos outros tipos de interneurônios foi em grande parte preservada. Ao traçar a origem dessas células até uma região fetal chamada eminência ganglionar caudal, descobriram que progenitores nessa região proliferavam excessivamente, mas falhavam em fazer a transição adequada para precursores VIP pós-mitóticos e migrar para o córtex. O padrão sugeriu que a sinalização Notch hiperativa estava prendendo esses progenitores em um estado de “nunca amadurecer”, levando a uma escassez duradoura de interneurônios VIP e a um viés em direção à excitação excessiva.
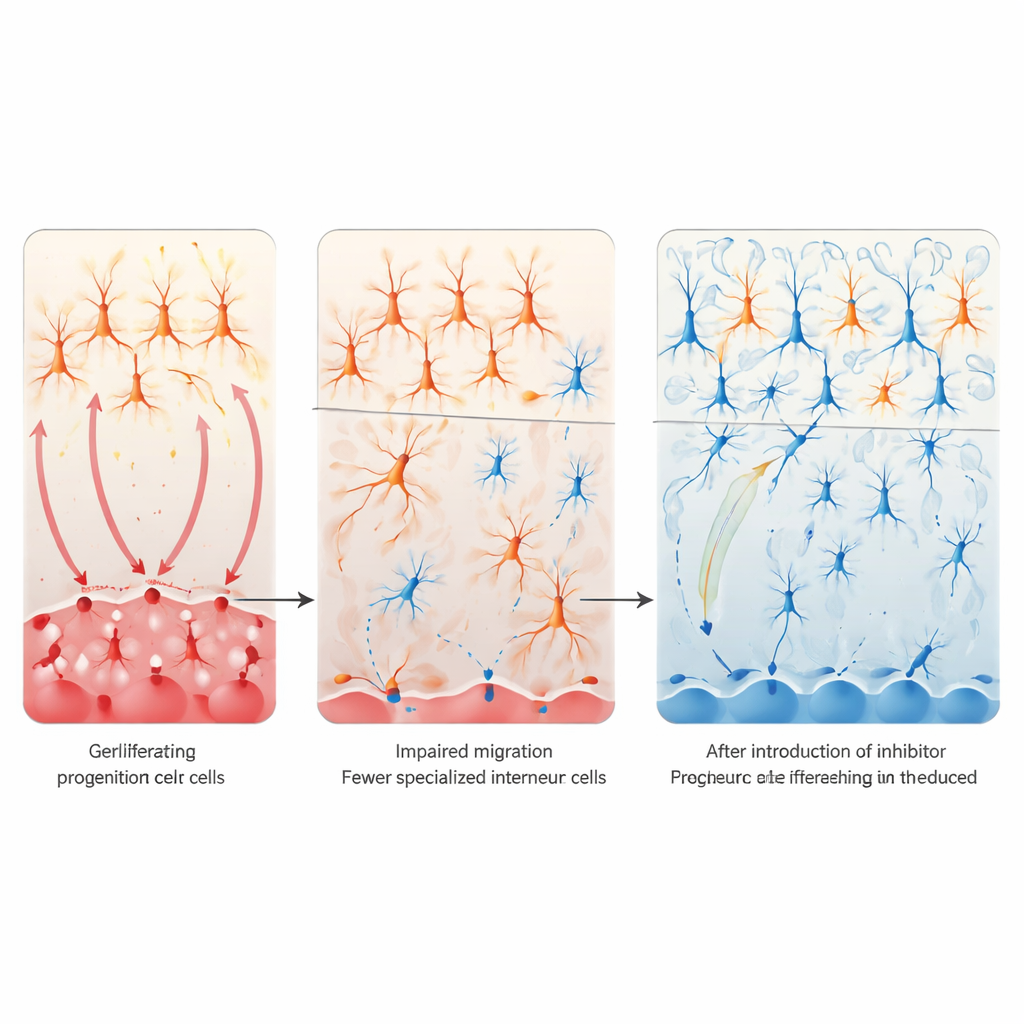
Reduzir a Notch para resgatar circuitos cerebrais
A próxima questão foi se acalmar a sinalização Notch poderia reparar esses defeitos. Em cultura celular, forçar a forma ativa do receptor Notch em células do prosencéfalo em desenvolvimento reduziu marcadores de interneurônios VIP, enquanto bloquear Notch geneticamente ou com um inibidor de γ-secretase teve o efeito oposto e pôde restaurar marcadores VIP mesmo após exposição ao valproato. Em camundongos vivos, a equipe deletou seletivamente Notch1 e Notch2 em células derivadas da eminência ganglionar caudal. Esse “freio” genético local evitou a perda de interneurônios VIP corticais e, em grande parte, normalizou comportamentos de interação social em descendentes expostos ao valproato durante a gestação. A análise transcriptômica de cérebros adultos mostrou que esse resgate também atenuou uma regulação anormal para cima de genes ligados a sinapses excitatórias de glutamato, sugerindo que restaurar os circuitos inibitórios VIP ajuda a reequilibrar redes corticais mais amplas.
Um medicamento pré-natal único que remodela o desenvolvimento
Como intervenções genéticas não são práticas em humanos, os pesquisadores testaram uma estratégia baseada em fármaco. Eles usaram Ro4929097, um potente inibidor de γ-secretase anteriormente avaliado em ensaios para câncer e Alzheimer, e administraram uma dose única a camundongos grávidos junto com valproato. Esse tratamento pré-natal breve reduziu os níveis de proteína Notch ativa, restaurou em grande parte o número de interneurônios VIP no córtex dos descendentes e melhorou múltiplos comportamentos semelhantes ao TEA, incluindo limpeza repetitiva e déficits sociais. Sequenciamento de RNA de célula única de cérebros neonatais revelou que o fármaco não apenas normalizou a linhagem VIP; ele também corrigiu perturbações mais amplas em progenitores neurais, oligodendrócitos (células formadoras de mielina) e outras populações celulares, direcionando a composição celular geral de volta àquela observada em animais controle.
O que isso significa para entender e tratar o autismo
Para leigos, a mensagem principal é que influências diversas relacionadas ao autismo podem convergir em um “quadro de distribuição” compartilhado no cérebro em desenvolvimento. Quando a via Notch fica presa na posição “ligada” durante uma janela fetal crítica, células nervosas inibitórias chave deixam de amadurecer e os circuitos corticais se tornam desequilibrados, contribuindo para problemas sociais e comportamentais. Em camundongos, reduzir cuidadosamente essa via — seja em tipos celulares específicos ou com uma dose pré-natal única de medicamento — pode, em grande parte, restaurar o desenvolvimento e o comportamento normais. Embora a tradução dessa abordagem para humanos exija extrema cautela, esses achados destacam a sinalização Notch, e especialmente o desenvolvimento dos interneurônios VIP, como alvos promissores para intervenções na vida precoce destinadas a prevenir ao menos algumas formas de disfunção cerebral associada ao TEA.
Citação: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Palavras-chave: transtorno do espectro autista, sinalização Notch, interneurônios VIP, neurodesenvolvimento, epigenética