Clear Sky Science · pl
Ukierunkowanie sygnalizacji Notch w celu przywrócenia rozwoju nerwowego i zachowania w modelach mysich ASD
Dlaczego te badania są ważne dla rodzin i społeczeństwa
Zaburzenia ze spektrum autyzmu (ASD) wpływają na sposób komunikowania się, nawiązywania relacji i reagowania na otoczenie, a ich biologiczne przyczyny pozostają zagadką. To badanie na myszach zajmuje się istotnym pytaniem: czy bardzo różne czynniki ryzyka autyzmu — geny, infekcje w czasie ciąży czy niektóre leki — prowadzą do zaburzenia tej samej ścieżki molekularnej w mózgu? Badacze wykryli wspólne zaburzenie w rozwojowym systemie sygnałowym zwanym Notch i pokazali, że ostrożne przytłumienie tej ścieżki przed narodzinami może przywrócić bardziej normalne okablowanie mózgu i zachowania społeczne w kilku mysich modelach przypominających ASD.
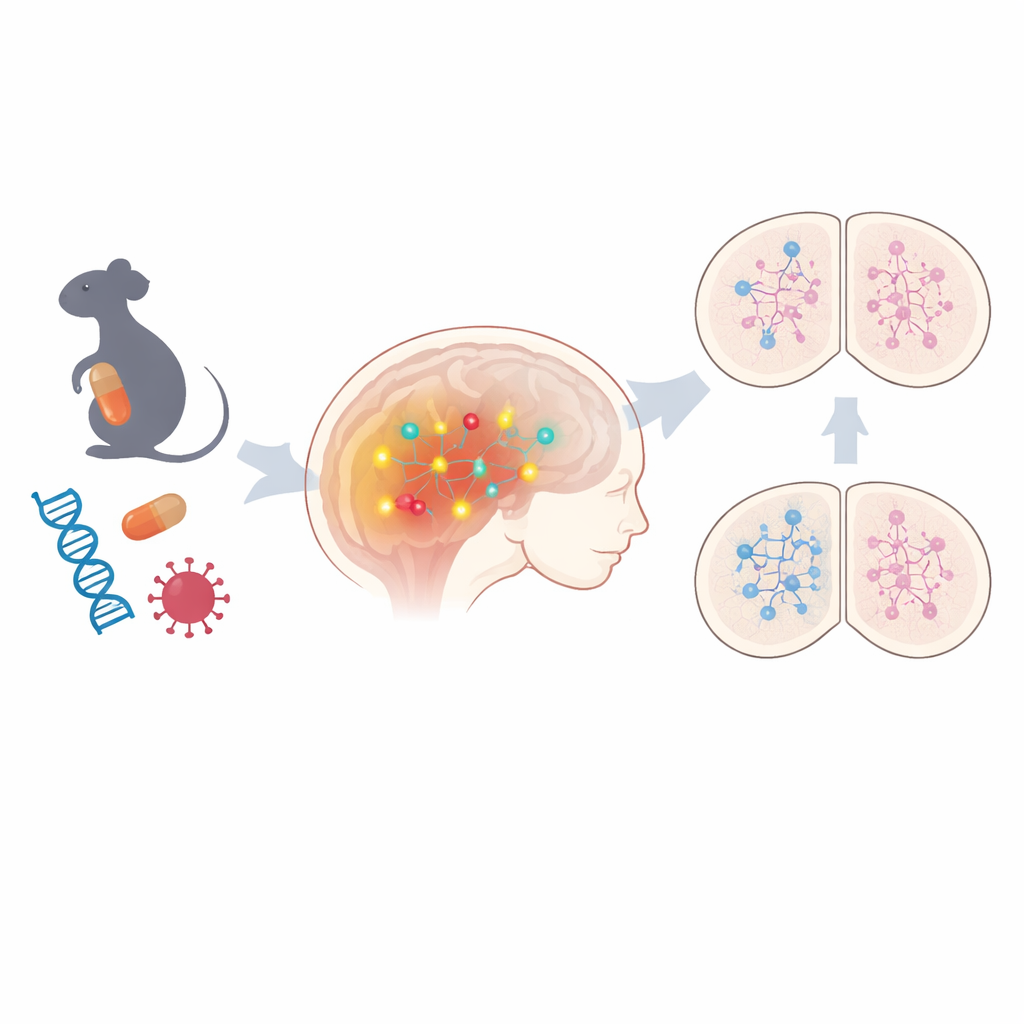
Wspólna ścieżka odpowiadająca za różne czynniki ryzyka
Zespół rozpoczął od analizy mózgów płodowych myszy w dwóch niegenetycznych modelach ASD: w jednym ciężarne samice były narażone na lek przeciwpadaczkowy kwas walproinowy, w drugim odtwarzano infekcję wirusową matki. Przy użyciu szerokiego profilowania aktywności genów stwierdzono, że setki genów były zmienione w obu modelach, z wyraźnymi sygnaturami zaburzonej regulacji epigenetycznej — chemicznych oznaczeń, które włączają lub wyłączają geny bez zmiany samego DNA. Wśród wspólnych zmian wyróżniała się jedna ścieżka: sygnalizacja Notch, kluczowy regulator tego, jak niedojrzałe komórki mózgu decydują, jakiego typu neuronem się staną. Składniki tej ścieżki, w tym receptory i dalsze efektory, były konsekwentnie nadaktywne. Gdy naukowcy przeanalizowali modele neuronów pochodzących z ludzkich komórek macierzystych noszące niektóre warianty genetyczne związane z autyzmem, ponownie obserwowali zwiększoną aktywność genów związanych z Notch w kilku przypadkach, co sugeruje, że ta ścieżka może łączyć zarówno środowiskowe, jak i dziedziczne formy ASD.
Wrażliwe komórki mózgowe, które dopracowują aktywność
Aby zrozumieć konsekwencje nadaktywności Notch, badacze skupili się na równowadze między sygnalizacją pobudzającą i hamującą w korze — często zaburzoną w autyzmie. Skoncentrowali się na niewielkiej populacji komórek hamujących zwanych interneuronami VIP, które regulują, jak silnie obwody korowe reagują na sygnały. W obu modelach — po ekspozycji na kwas walproinowy i po aktywacji odpornościowej matki — liczba tych komórek VIP w korze była dramatycznie zmniejszona, podczas gdy większość innych typów interneuronów była w dużej mierze nietknięta. Śledząc pochodzenie tych komórek do tkanki płodowej zwanej ogonowym wzgórzem zwojowym (caudal ganglionic eminence), odkryli, że komórki progenitorowe tam nadmiernie się proliferowały, lecz nie przełączały się prawidłowo w postmitotyczne prekursorowe komórki VIP i nie migrowały do kory. Wzorzec ten sugerował, że nadmierna sygnalizacja Notch utrzymuje te progenitory w stanie „nigdy nie dorosnąć”, co prowadzi do trwałego niedoboru interneuronów VIP i przesunięcia równowagi ku nadmiernej pobudliwości.
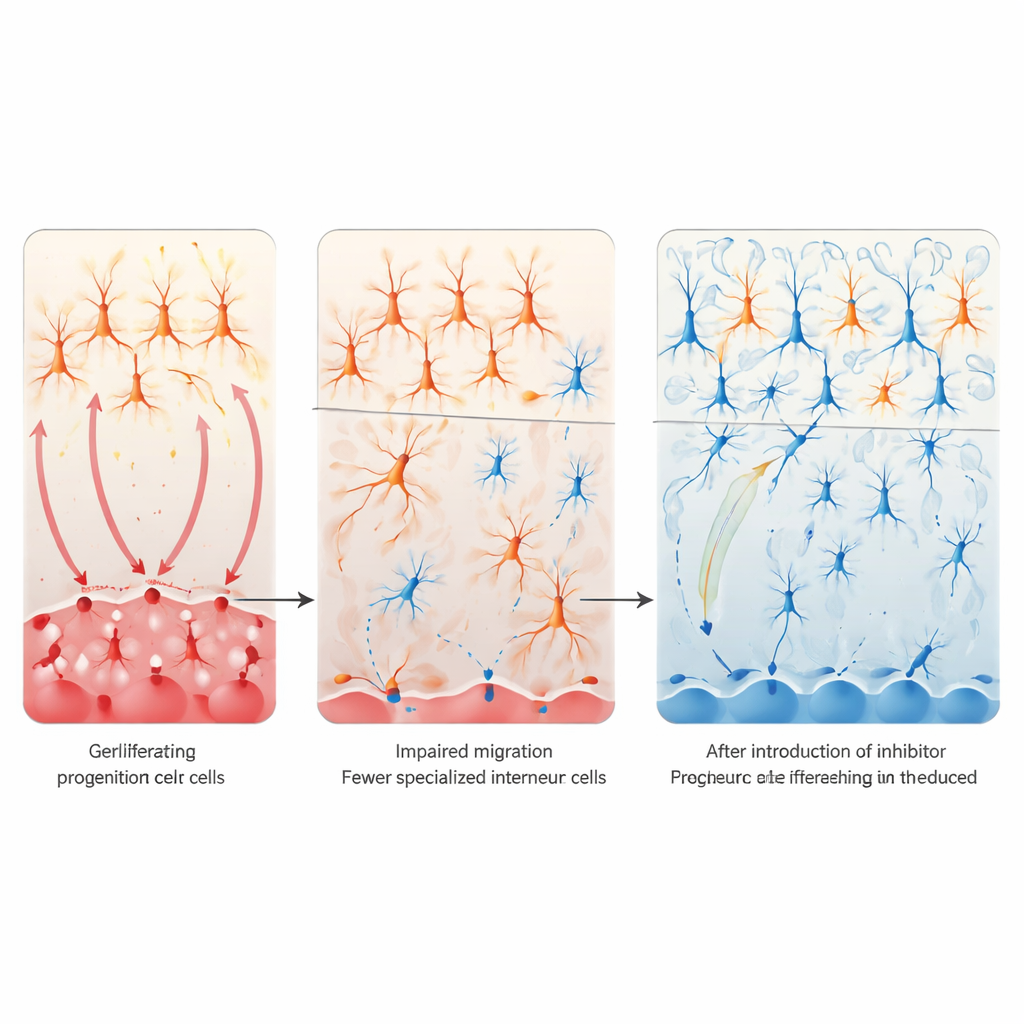
Przyciszenie Notch przywraca obwody mózgowe
Następne pytanie brzmiało, czy uspokojenie sygnalizacji Notch może naprawić te defekty. W hodowlach komórkowych wymuszenie aktywnej formy receptora Notch w rozwijających się komórkach przedniego mózgu zmniejszało markery interneuronów VIP, podczas gdy genetyczne zablokowanie Notch lub zastosowanie inhibitora γ-sekretazy dawało efekt przeciwny i mogło przywrócić markery VIP nawet po ekspozycji na kwas walproinowy. U żywych myszy zespół selektywnie usunął Notch1 i Notch2 w komórkach pochodzących z ogonowego wzgórza zwojowego. Ten lokalny genetyczny „hamulec” zapobiegł utracie interneuronów VIP w korze i w dużej mierze znormalizował zachowania społeczne potomstwa narażonego na kwas walproinowy w ciąży. Analiza transkryptomiczna dorosłych mózgów wykazała, że ta interwencja osłabiła również nieprawidłową nadaktywację genów związanych z pobudzającymi synapsami glutaminergicznymi, co sugeruje, że przywrócenie hamujących obwodów VIP pomaga zrównoważyć szersze sieci korowe.
Jednorazowy prenatalny lek, który przekształca rozwój
Ponieważ interwencje genetyczne nie są praktyczne u ludzi, badacze przetestowali strategię farmakologiczną. Użyli Ro4929097, silnego inhibitora γ-sekretazy wcześniej ocenianego w badaniach nad rakiem i chorobą Alzheimera, i podali pojedynczą dawkę ciężarnym myszom razem z kwasem walproinowym. Krótkie prenatalne leczenie obniżyło poziomy aktywnego białka Notch, w dużej mierze przywróciło liczbę interneuronów VIP w korze potomstwa i poprawiło wiele zachowań przypominających ASD, w tym powtarzalne pielęgnowanie i deficyty społeczne. Sekwencjonowanie RNA pojedynczych komórek w mózgach noworodków wykazało, że lek nie tylko normalizował linię VIP; skorygował także szersze zaburzenia w progenitorach nerwowych, oligodendrocytach (komórkach tworzących osłonkę mielinową) i innych populacjach komórkowych, przesuwając ogólny skład komórkowy z powrotem w kierunku obserwowanego u zwierząt kontrolnych.
Co to oznacza dla zrozumienia i leczenia autyzmu
Dla laika główny wniosek jest taki, że różnorodne wpływy związane z autyzmem mogą zbiegać się na wspólnym „centrali” w rozwijającym się mózgu. Gdy ścieżka Notch jest zakleszczona w pozycji „włączonej” podczas krytycznego płodowego okna, kluczowe komórki hamujące nie dojrzewają i obwody korowe stają się niezrównoważone, co przyczynia się do problemów społecznych i behawioralnych. U myszy ostrożnie czasowe przytłumienie tej ścieżki — albo w określonych typach komórek, albo jednorazową prenatalną dawką leku — może w dużej mierze przywrócić prawidłowy rozwój i zachowanie. Choć przeniesienie takiego podejścia na ludzi wymaga wielkiej ostrożności, te wyniki wskazują na sygnalizację Notch, a szczególnie rozwój interneuronów VIP, jako obiecujące cele dla interwencji we wczesnym życiu mających na celu zapobieganie przynajmniej niektórym formom dysfunkcji mózgowej związanej z ASD.
Cytowanie: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Słowa kluczowe: zaburzenia ze spektrum autyzmu, sygnalizacja Notch, neuron interneuronów VIP, neurogeneza, epigenetyka