Clear Sky Science · fr
Cibler la signalisation Notch pour restaurer le développement neural et le comportement dans des modèles murins du TSA
Pourquoi ces recherches comptent pour les familles et la société
Le trouble du spectre autistique (TSA) affecte la manière dont les personnes communiquent, socialisent et réagissent au monde qui les entoure, mais ses origines biologiques restent énigmatiques. Cette étude chez la souris aborde une grande question : des facteurs de risque très différents pour l’autisme — gènes, infections pendant la grossesse ou certains médicaments — perturbent-ils finalement la même voie cérébrale ? Les chercheurs mettent en évidence une perturbation commune d’un système de signalisation développemental appelé Notch et montrent qu’abaisser soigneusement cette voie avant la naissance peut rétablir une architecture cérébrale et un comportement social plus normaux dans plusieurs modèles murins présentant des traits de TSA.
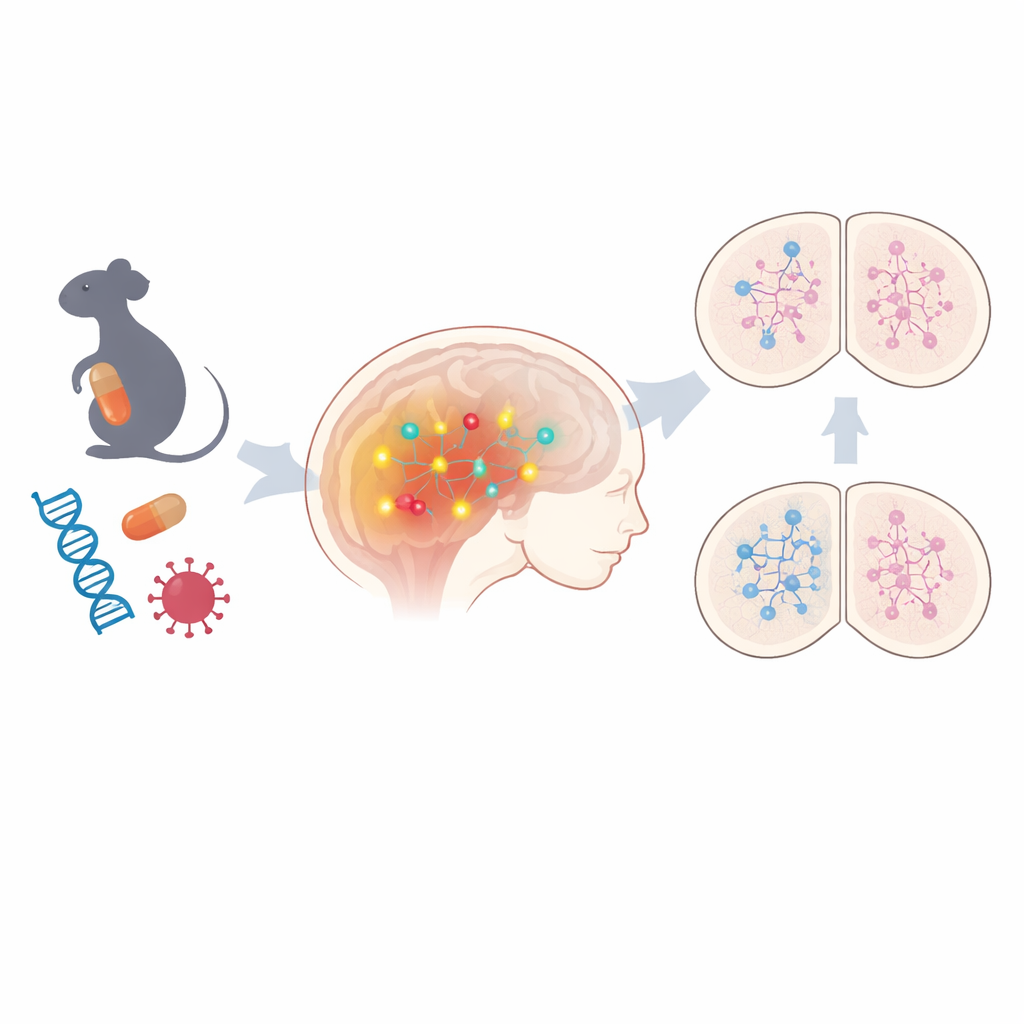
Une voie commune derrière de nombreux risques différents
L’équipe a commencé par examiner des cerveaux fœtaux de souris issus de deux modèles non génétiques de TSA : l’un où des femelles enceintes ont été exposées à l’anticonvulsivant acide valproïque, et l’autre reproduisant une infection virale maternelle. Grâce à des profils larges d’activité génique, ils ont constaté que des centaines de gènes étaient modifiés dans les deux modèles, avec des signatures nettes de dérèglement épigénétique — des marques chimiques qui activent ou désactivent des gènes sans changer l’ADN lui‑même. Parmi les changements partagés, une voie s’est démarquée : la signalisation Notch, un contrôleur clé de la façon dont les cellules cérébrales immatures décident quel type de neurone devenir. Des composants de cette voie, y compris les récepteurs centraux et les effecteurs en aval, étaient systématiquement surexprimés. Lorsque les scientifiques ont examiné des modèles neuronaux dérivés de cellules souches humaines portant certaines variantes génétiques liées à l’autisme, ils ont de nouveau observé une activité génique liée à Notch accrue dans plusieurs cas, suggérant que cette voie pourrait être un fil commun aux formes environnementales et héréditaires du TSA.
Des cellules cérébrales vulnérables qui ajustent l’activité
Pour comprendre les conséquences d’une suractivité de Notch, les chercheurs se sont concentrés sur l’équilibre entre la signalisation excitrice et inhibitrice dans le cortex — souvent perturbé dans l’autisme. Ils ont ciblé une petite population de cellules nerveuses inhibitrices appelées interneurones VIP, qui contribuent à réguler la force de la réponse des circuits corticaux aux stimuli. Dans les modèles murins d’exposition à l’acide valproïque et d’activation immune maternelle, ces cellules VIP étaient fortement réduites dans le cortex, alors que la plupart des autres types d’interneurones étaient pour l’essentiel préservés. En retraçant l’origine de ces cellules jusqu’à une région fœtale appelée l’éminence ganglionnaire caudale, ils ont constaté que les cellules progénitrices y proliféraient de manière excessive mais ne parvenaient pas à se convertir correctement en précurseurs VIP post‑mitotiques et à migrer vers le cortex. Le schéma suggérait qu’une signalisation Notch hyperactive maintenait ces progéniteurs dans un état de « jamais mûrir », conduisant à une pénurie durable d’interneurones VIP et à une bascule vers une excitation excessive.
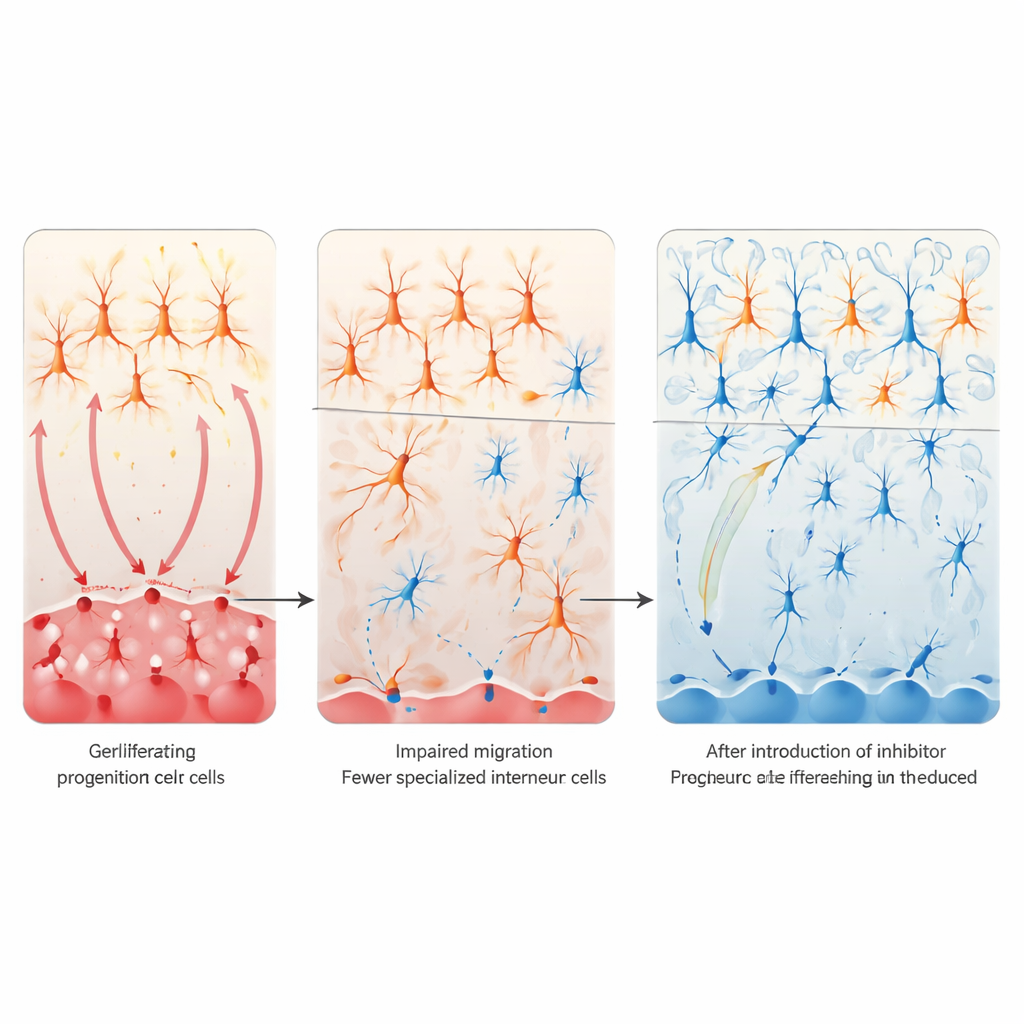
Réduire Notch pour réparer les circuits cérébraux
La question suivante était de savoir si calmer la signalisation Notch pouvait corriger ces défauts. En culture cellulaire, forcer la forme active du récepteur Notch dans des cellules du cerveau antérieur en développement réduisait les marqueurs des interneurones VIP, tandis que bloquer Notch génétiquement ou avec un inhibiteur de γ‑sécrétase avait l’effet inverse et pouvait restaurer les marqueurs VIP même après exposition à l’acide valproïque. Chez la souris vivante, l’équipe a supprimé sélectivement Notch1 et Notch2 dans des cellules dérivées de l’éminence ganglionnaire caudale. Cette « frein » génétique local a empêché la perte des interneurones VIP corticaux et a en grande partie normalisé les comportements d’interaction sociale chez les descendants exposés à l’acide valproïque pendant la gestation. L’analyse transcriptomique des cerveaux adultes a montré que ce sauvetage atténuait également une surexpression anormale de gènes liés aux synapses glutamatergiques excitratrices, suggérant que la restauration des circuits inhibiteurs VIP contribue à rééquilibrer des réseaux corticaux plus larges.
Un médicament prénatal unique qui remodelle le développement
Parce que les interventions génétiques ne sont pas pratiques chez l’humain, les chercheurs ont testé une stratégie médicamenteuse. Ils ont utilisé Ro4929097, un inhibiteur puissant de la γ‑sécrétase précédemment évalué dans des essais contre le cancer et la maladie d’Alzheimer, et ont administré une dose unique à des femelles enceintes en même temps que l’acide valproïque. Ce bref traitement prénatal a réduit les niveaux de protéine Notch active, a en grande partie restauré le nombre d’interneurones VIP dans le cortex des descendants et a amélioré plusieurs comportements de type TSA, y compris le toilettage répétitif et les déficits sociaux. Le séquençage ARN unicellulaire des cerveaux de nouveau‑nés a révélé que le médicament ne normalisait pas seulement la lignée VIP ; il corrigeait aussi des perturbations plus larges dans les progéniteurs neuronaux, les oligodendrocytes (cellules formant la myéline) et d’autres populations cellulaires, rapprochant la composition cellulaire globale de celle observée chez les animaux témoins.
Ce que cela signifie pour la compréhension et le traitement de l’autisme
Pour un non‑spécialiste, la conclusion principale est que des influences liées à l’autisme, très diverses, peuvent converger vers un « panneau de contrôle » partagé du cerveau en développement. Lorsque la voie Notch reste bloquée en position « on » pendant une fenêtre fœtale critique, des neurones inhibiteurs clés n’arrivent pas à maturité et les circuits corticaux se déséquilibrent, contribuant à des troubles sociaux et comportementaux. Chez la souris, un affaiblissement soigneusement chronométré de cette voie — soit dans des types cellulaires spécifiques, soit par une dose prénatale unique de médicament — peut largement restaurer le développement et le comportement normaux. La traduction d’une telle approche à l’homme exigera une extrême prudence, mais ces résultats mettent en lumière la signalisation Notch, et en particulier le développement des interneurones VIP, comme des cibles prometteuses pour des interventions en début de vie visant à prévenir au moins certaines formes de dysfonctionnement cérébral associé au TSA.
Citation: Hanno, Y., Nakanishi, M., Takase, A. et al. Targeting notch signaling to restore neural development and behavior in mouse models of ASD. Nat Commun 17, 2587 (2026). https://doi.org/10.1038/s41467-026-70321-6
Mots-clés: trouble du spectre autistique, signalisation Notch, interneurones VIP, neurodéveloppement, épigénétique