Clear Sky Science · tr
Hücresel düzeyde bozulmuş $$\alpha$$-Sİnüklein agregat temizliği, tünelleşen nanotüpler aracılığıyla bunların mikroglialara yayılmasını tetikliyor
Beyin sağlığı için küçük protein kümeleri neden önemli
Parkinson hastalığı ve ilgili bozukluklar, alfa-sinüklein adlı bir proteinin beyin hücreleri içinde yavaşça birikmesiyle karakterizedir. Bu kümeler hücrelere zarar verebilir, ancak beyin savunmasız değildir: kendi temizleme ekipleri ve destek hücreleri vardır. Bu çalışma, sinir hücreleri ile beyin bağışıklık hücrelerinin bu kümeleri temizleme yükünü nasıl paylaştığını ve tünelleşen nanotüp olarak adlandırılan, hücreler arası az bilinen bir köprünün, toksik maddeyi zorlanan nöronlardan daha dayanıklı mikroglialara aktarmada nasıl bir otoyol haline geldiğini araştırıyor.
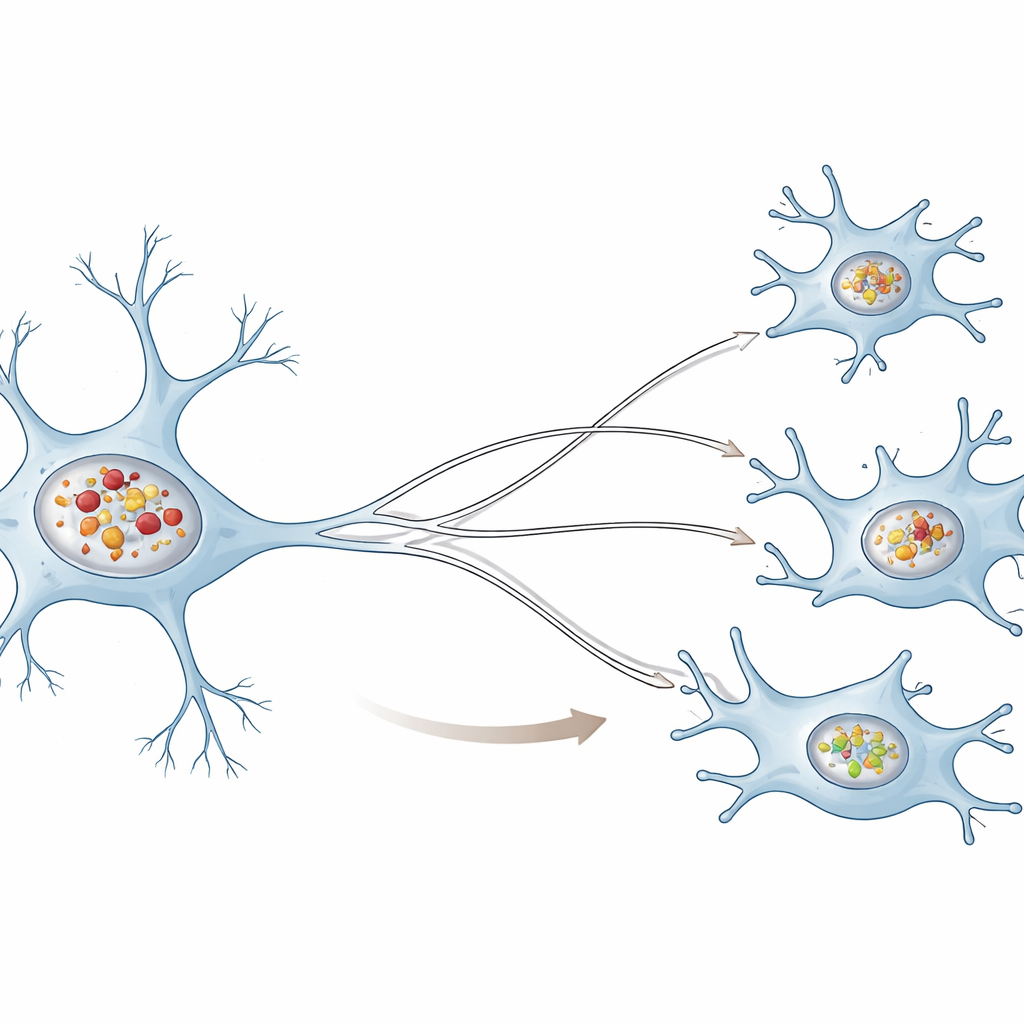
İki çok farklı temizlik ekibi
Yazarlar insan nöron-benzeri hücreleri beyin dokusunun yerleşik bağışıklık hücreleri olan insan mikrogliaları ile karşılaştırdı ve her iki hücre tipini de laboratuvarda hazırlanan, hastalıkta görülen zararlı kümelerin bir versiyonu olan önceden oluşturulmuş alfa-sinüklein fibrillerine maruz bıraktı. Her iki hücre tipinde de gelen kümeler alınıp lizozom adı verilen küçük geri dönüşüm bölmelerine gönderildi. Bununla birlikte, nöronlar lizozomlarında mikroglialardan çok daha fazla küme biriktirdi. Zamanla nöronal lizozomlar daha az asidik hale geldi ve bir test proteini parçalayıp yok etme kapasitesi azaldı; bu, temel geri dönüşüm işlevlerinin aksadığını gösterdi. Buna karşılık mikrogliaların lizozomları, alfa-sinüklein içeriyor olsalar bile büyük ölçüde asidite ve parçalama kapasitelerini korudu.
Geri dönüşüm başarısız olduğunda hasar yayılır
Hasarlı lizozomlar sızıntı yapabilir veya yırtılabilir. Zar kırılmalarının belirteçleri ve onarım proteinlerini kullanarak araştırmacılar, alfa-sinükleine maruz kaldıktan sonra nöronların mikroglialara kıyasla çok daha fazla lizozomal hasar yaşadığını buldu. Etkilenen nöronal lizozomlar hareket kabiliyetini yitirdi ve kümelenme gösterdi; bu da işlev bozukluğunun bir başka işareti. Mikroglia farklı yanıt verdi: hasarlı lizozomların hedeflenmiş uzaklaştırılması olan lizofaji sürecini başlattı ve aynı zamanda yeni lizozomların oluşumunu artırdı. Lizozom ve temizleme gen programlarını yöneten ana kontrol proteini her iki hücre tipinin çekirdeğine geçti, fakat yalnızca mikroglialarda aşağı akış genler güçlü bir şekilde açıldı. Bu asimetri, nöronların geri dönüşüm sistemlerini onarmakta zorlandığı, mikrogliaların ise kendi sistemlerini yenileyebildiği anlamına gelir.
Otofaji: nöronlarda tıkalı, mikroglialarda artırılmış
Protein kümeleri normalde istenmeyen maddeleri sarıp lizozomlara teslim eden otofaji yolu ile işlenir. Ekip otofaji “akışını” ölçtü ve alfa-sinükleinin bu akışı büyük ölçüde nöronlarda bloke ettiğini, mikroglialarda ise etkilemediğini buldu. Kümelere maruz kalan nöronlar, yolun son adımı kimyasal olarak engellendiğinde daha fazla artış göstermeyen bir yük-adaptör proteini (p62) birikimi gösterdi; bu, bant konveyörün tıkandığı ile tutarlı. Buna karşılık mikroglia daha fazla p62 üretti ve son adım engellendiğinde güçlü bir artış gösterdi; bu da yolun hala çalıştığını, hatta yükseltildiğini gösteriyor. Mikroskopi, mikroglialarda alfa-sinüklein, otofaji belirteçleri ve lizozomların bir araya geldiği çok daha fazla nokta ortaya koydu; bu da mikrogliaların kümeleri tanıma ve yok edilmek üzere yönlendirme konusunda çok daha iyi olduğunu düşündürüyor.
Toksik yük için nanotüp otoyolları
Nöronlar çöplerle baş edemediğinde ne olur? Çalışma, sorunu mikroglialara aktardıklarını gösteriyor. Alfa-sinüklein yüklü nöronlarda otofaji kimyasal olarak engellendiğinde, daha fazla küme komşu mikroglialara aktarıldı; otofaji uyarıldığında ise aktarım düştü. Bu alışverişler kültür ortamına salınan materyale bağlı değildi, bunun yerine doğrudan hücreler arası bağlantılara işaret etti. Yazarlar tünelleşen nanotüplere—hücreler arasında ince, aktin temelli köprülere—odaklandı ve nöronlarda ya da mikroglialarda otofajiyi engellemenin hem bu bağlantıların sayısını hem de bunlardan geçen genel yük miktarını artırdığını buldu. Mikroglia verici konumunda olduğunda bile, onların otofajilerini bozmak nöronlara transferi artırdı; bu, kusurlu kendi kendini temizlemenin hücreleri bağlanmaya ve agregatları aktarmaya teşvik eden bir sinyal olduğunu öne sürüyor.
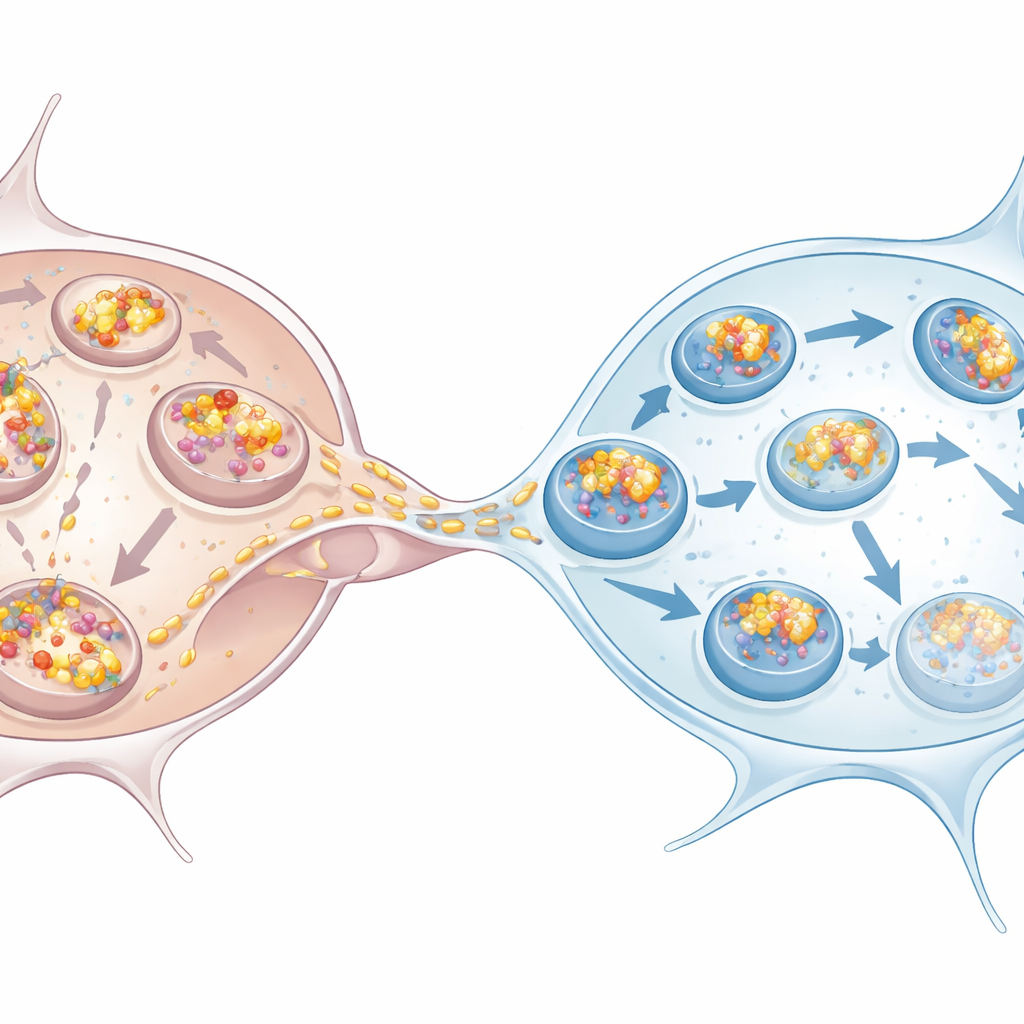
Mikroglia zorluğa karşı koyuyor
Çalışma ayrıca Parkinson hastalığında etkilenen hücrelere daha benzer olan insan kök hücre kaynaklı dopaminerjik nöronlar ve mikrogliaları inceledi. Aynı desen ortaya çıktı: nöronlar daha fazla alfa-sinüklein biriktirdi, otofajide bozulma belirtileri gösterdi ve atıkları devralmak için mikroglialara güvendiler. Aşırı yüklenmiş nöronlarla birlikte büyütülen veya yalnızca bunların koşullandırılmış ortamına maruz kalan mikroglialar kendi otofajilerini artırdı. Nanotüpler aracılığıyla alfa-sinüklein aldıklarında, gelen kümelerin büyük bir kısmı p62 işaretli yapılarda sonlandı; bu, parçalanmaya doğru bir rota ile uyumlu. Nöronları mikroglialarla birlikte kültürlemek, nöronlar içindeki kümelerin sayısını ve toplam yükünü azalttı; bu da mikrogliaların toksik agregatlar için etkili emici görevi gördüğünü doğruluyor.
Parkinson ve ötesi için bunun anlamı
Uzman olmayan biri için ana mesaj, tüm beyin hücrelerinin protein atıklarıyla başa çıkma konusunda eşit donanıma sahip olmadığıdır. Özellikle Parkinson’da hassas olan nöronların geri dönüşüm sistemleri kırılgandır ve alfa-sinüklein kümeleriyle kolayca bunaltılabilir. Mikroglia ise daha dayanıklı temizleyicilerdir ve küçük nanotüp köprüleri aracılığıyla nöronların fazla agregatlarını alıp parçalayarak nöronları kurtarmaya yardımcı olabilir. Ancak bu yardım bir bedelle gelir: aynı süreç hastalıkla ilişkili proteinlerin beyin genelinde yayılmasına da katkıda bulunabilir. Nöronal otofajiyi geri kazandıran veya mikroglial temizliği ince ayarlayan terapiler, sadece bireysel hücrelerin içindeki toksik yükü azaltmakla kalmayıp, zararlı protein kümelerinin hücreden hücreye yayılmasını da yavaşlatabilir.
Atıf: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Anahtar kelimeler: Parkinson hastalığı, alfa-sinüklein, mikroglia, otofaji, tünelleşen nanotüpler