Clear Sky Science · fr
Élimination altérée des agrégats de $$\alpha$$-synucléine dans les cellules neuronales favorise leur propagation vers les microglies via des nanotubes de tunnellisation
Pourquoi de petites agrégations protéiques comptent pour la santé cérébrale
La maladie de Parkinson et les troubles apparentés se caractérisent par l’accumulation progressive d’amas d’une protéine appelée alpha‑synucléine à l’intérieur des cellules cérébrales. Ces agrégats peuvent endommager les cellules, mais le cerveau n’est pas sans défense : il dispose de ses propres équipes de nettoyage et de cellules de soutien. Cette étude examine comment les neurones et les cellules immunitaires du cerveau se partagent la charge d’élimination de ces amas, et comment un type de pont cellulaire peu connu, appelé nanotube de tunnellisation, devient une voie pour évacuer du matériau toxique des neurones affaiblis vers des microglies plus résistantes.
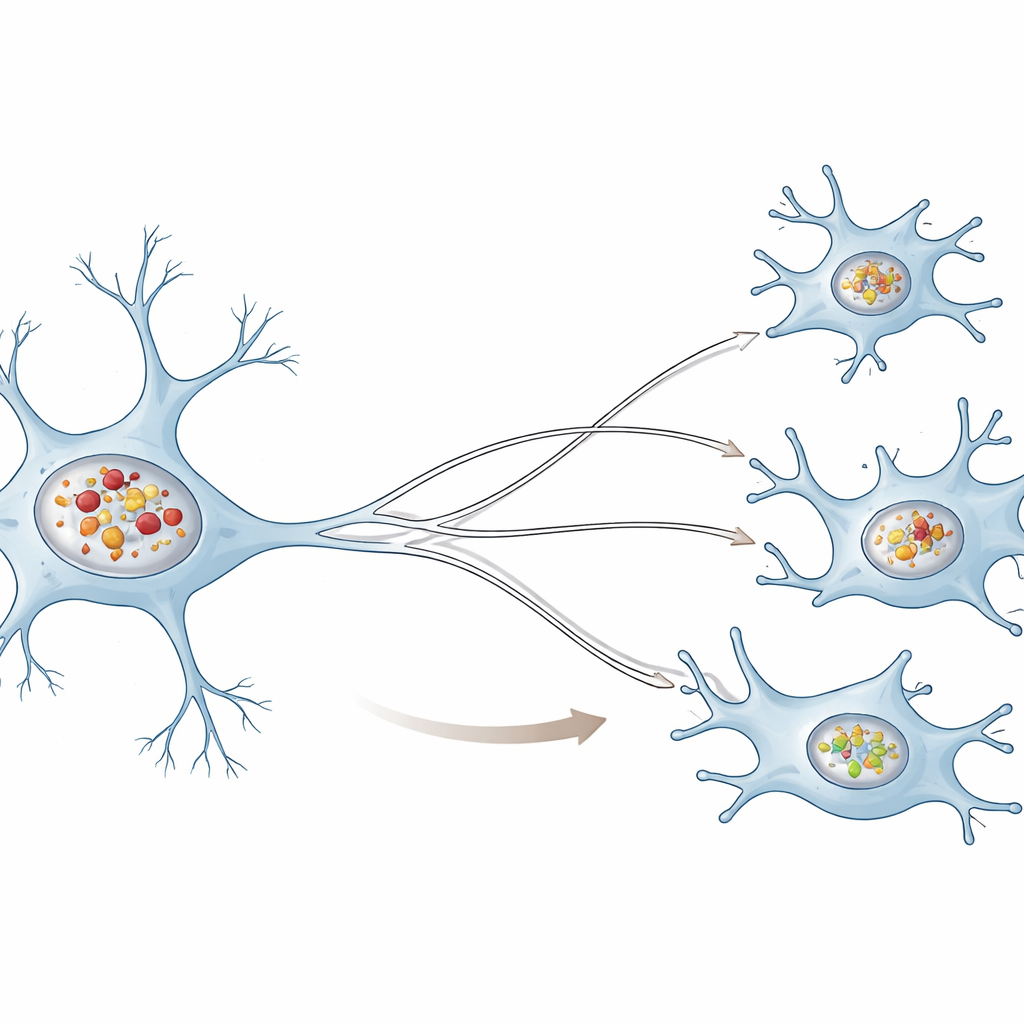
Deux équipes de nettoyage très différentes
Les auteurs ont comparé des cellules de type neuronal humain à des microglies humaines, les cellules immunitaires résidentes du cerveau, et ont exposé les deux types à des fibrilles d’alpha‑synucléine préformées, une version en laboratoire des amas nocifs observés en pathologie. Dans les deux types cellulaires, les agrégats entrants étaient internalisés et envoyés vers de petits compartiments de recyclage appelés lysosomes. Cependant, les neurones accumulaient beaucoup plus d’amas dans leurs lysosomes que les microglies. Au fil du temps, les lysosomes neuronaux devenaient moins acides et moins aptes à dégrader une protéine test, montrant que leur fonction de recyclage centrale déclinait. Les lysosomes des microglies, en revanche, préservaient en grande partie leur acidité et leur capacité de dégradation même lorsqu’ils contenaient de l’alpha‑synucléine.
Quand le recyclage échoue, les dégâts se propagent
Les lysosomes endommagés peuvent fuir et se rompre. En utilisant des marqueurs de ruptures membranaires et des protéines de réparation, les chercheurs ont constaté que les neurones subissaient bien plus de lésions lysosomales que les microglies après exposition à l’alpha‑synucléine. Les lysosomes affectés dans les neurones perdaient en mobilité et se regroupaient, un autre signe de dysfonctionnement. Les microglies réagissaient différemment : elles activaient la lysophagie, une élimination ciblée des lysosomes endommagés, et simultanément stimulaient la biogenèse de nouveaux lysosomes. Une protéine de contrôle maître qui dirige les programmes géniques liés aux lysosomes et au nettoyage migra dans le noyau des deux types cellulaires, mais seules les microglies déclenchaient de façon robuste l’expression en aval de ces gènes. Cette asymétrie signifie que les neurones peinent à restaurer leur système de recyclage, tandis que les microglies peuvent renouveler le leur.
Autophagie : bouchée dans les neurones, stimulée dans les microglies
Les agrégats protéiques sont normalement pris en charge par l’autophagie, une voie qui entoure le matériel indésirable et le livre aux lysosomes. L’équipe a mesuré le « flux » autophagique et a constaté que l’alpha‑synucléine bloquait largement ce flux dans les neurones mais pas dans les microglies. Les neurones exposés aux amas montraient une accumulation d’une protéine adaptatrice de cargaison (p62) sans augmentation supplémentaire lorsque l’étape finale de la voie était chimiquement bloquée, ce qui correspond à un tapis roulant arrêté. Les microglies, en revanche, produisaient plus de p62 et présentaient une forte augmentation lorsque la dernière étape était bloquée, indiquant une voie encore active, voire suractivée. La microscopie révélait beaucoup plus de sites dans les microglies où l’alpha‑synucléine, les marqueurs de l’autophagie et les lysosomes se rencontraient, suggérant que les microglies sont bien meilleures pour reconnaître et orienter les agrégats vers la destruction.
Nanotubes : autoroutes pour les cargaisons toxiques
Que se passe‑t‑il lorsque les neurones ne peuvent plus suivre le déchet ? L’étude montre qu’ils transfèrent le problème aux microglies. Lorsque l’autophagie était chimiquement inhibée dans des neurones chargés d’alpha‑synucléine, davantage d’amas étaient transférés aux microglies voisines, et lorsque l’autophagie était stimulée, le transfert diminuait. Ces échanges ne dépendaient pas de matière libérée dans le milieu de culture, mais plutôt de connexions directes entre cellules. Les auteurs se sont concentrés sur les nanotubes de tunnellisation — de fins ponts à base d’actine entre cellules — et ont trouvé que bloquer l’autophagie chez les neurones ou les microglies augmentait à la fois le nombre de ces connexions et la quantité de cargaisons générales transitant par elles. Même lorsque les microglies étaient donneuses plutôt que réceptrices, l’altération de leur autophagie augmentait le transfert vers les neurones, ce qui suggère qu’un défaut d’auto‑nettoyage est un signal encourageant les cellules à se connecter et à passer les agrégats.
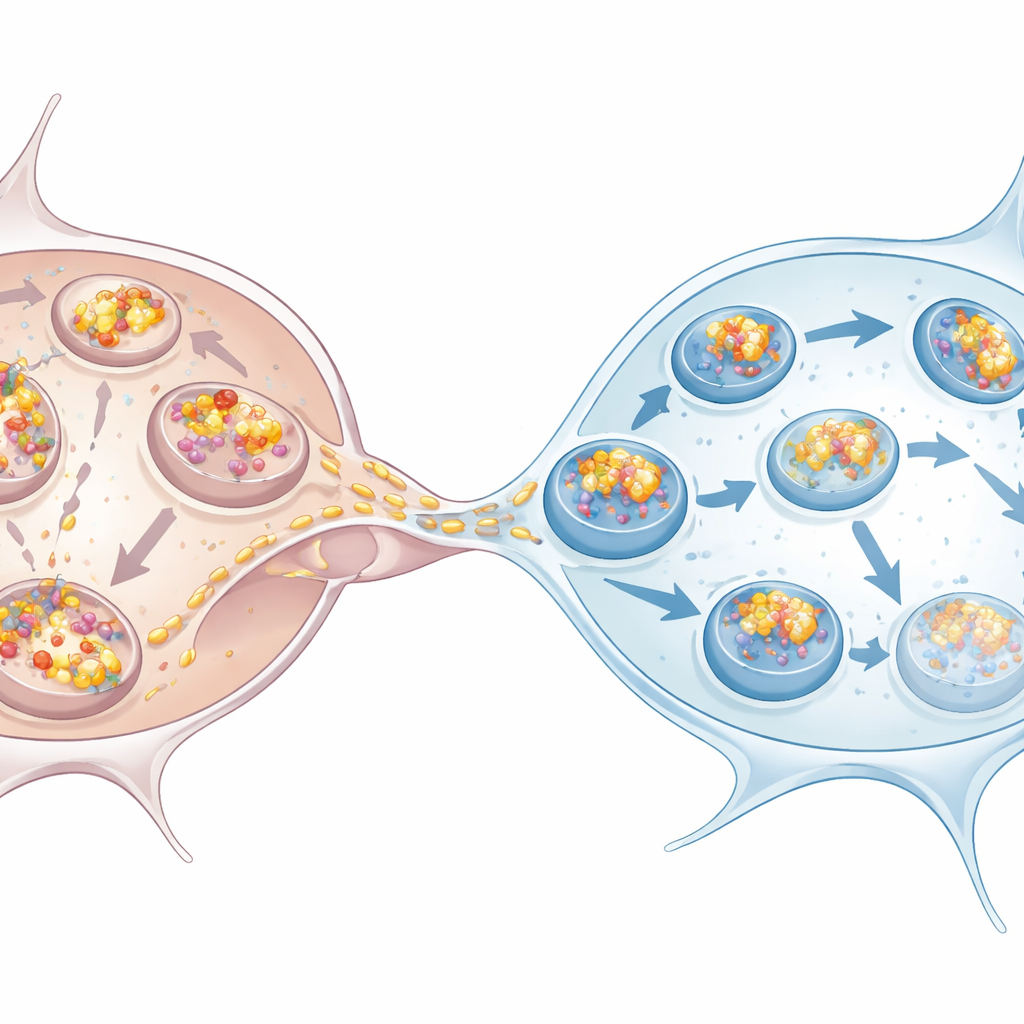
Les microglies relèvent le défi
Le travail a également examiné des neurones dopaminergiques et des microglies dérivés de cellules souches humaines, qui ressemblent davantage aux cellules affectées dans la maladie de Parkinson. Le même schéma est apparu : les neurones accumulaient davantage d’alpha‑synucléine, montraient des signes d’autophagie altérée, et dépendaient des microglies pour prendre en charge l’élimination. Les microglies cultivées à côté de neurones surchargés, ou même simplement exposées à leur milieu conditionné, ont renforcé leur propre autophagie. Une fois qu’elles recevaient de l’alpha‑synucléine via des nanotubes, une large fraction des agrégats entrants se retrouvait dans des structures marquées par p62, cohérentes avec une voie menant à la dégradation. La coculture de neurones avec des microglies réduisait le nombre et la charge globale d’agrégats à l’intérieur des neurones, confirmant que les microglies agissent comme des puits efficaces pour ces agrégats toxiques.
Ce que cela signifie pour la maladie de Parkinson et au-delà
Pour un non‑spécialiste, le message principal est que toutes les cellules cérébrales ne sont pas également équipées pour gérer les déchets protéiques. Les neurones, en particulier ceux vulnérables dans la maladie de Parkinson, possèdent des systèmes de recyclage fragiles qui peuvent être submergés par les amas d’alpha‑synucléine. Les microglies, en revanche, sont des nettoyeurs plus robustes et peuvent aider à sauver les neurones en absorbant et en dégradant leurs agrégats excédentaires via de minuscules ponts nanotubulaires. Mais cette aide a un coût : le même processus peut aussi faciliter la propagation des protéines liées à la maladie dans le cerveau. Des thérapies qui restaurent l’autophagie neuronale ou ajustent le nettoyage microglial pourraient non seulement réduire la charge toxique à l’intérieur des cellules individuelles, mais aussi ralentir la propagation intercellulaire des amas protéiques nocifs.
Citation: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Mots-clés: Maladie de Parkinson, alpha-synucléine, microglie, autophagie, nanotubes de tunnellisation