Clear Sky Science · sv
Försämrad rensning av $$\alpha$$-synuklein‑aggregat i neuronala celler driver deras spridning till mikroglia via tunneling‑nanotuber
Varför små proteinklumpar spelar roll för hjärnhälsan
Parkinsons sjukdom och närliggande störningar kännetecknas av en långsam uppbyggnad av klumpar av proteinet alfa‑synuklein inne i hjärnceller. Dessa klumpar kan skada celler, men hjärnan är inte obeväpnad: den har sina egna städteam och stödjeceller. Denna studie undersöker hur nervceller och hjärnans immunceller delar på ansvaret att rensa bort dessa klumpar, och hur en relativt okänd typ av cell‑till‑cell‑bro, kallad tunneling‑nanotub, blir en motorväg för att föra toxisk materia ut ur kämpande neuroner och in i tåligare mikroglia.
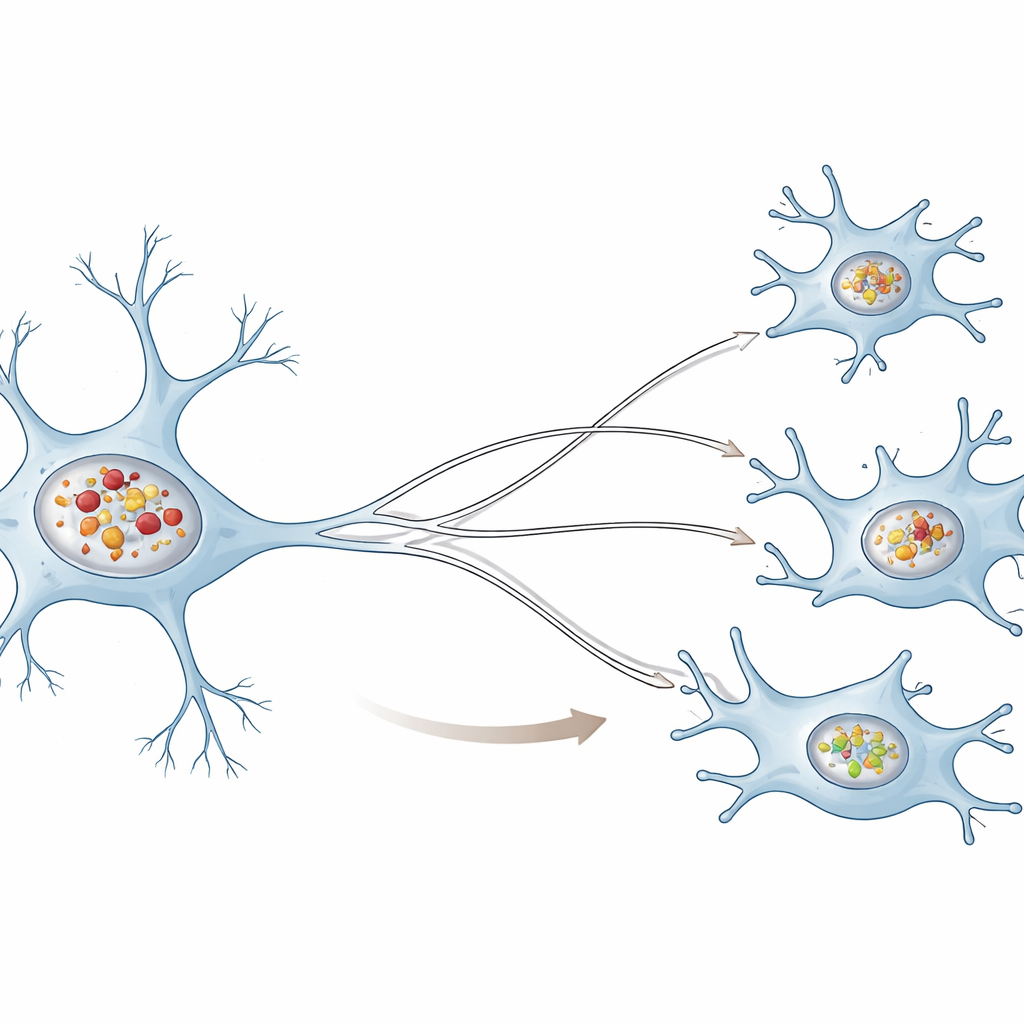
Två väldigt olika städteam
Författarna jämförde människoliknande neuronala celler med mänskliga mikroglia, hjärnans residenta immunceller, och exponerade båda för förbildade alfa‑synuklein‑fibriller, en laboratorieversion av de skadliga klumpar som ses vid sjukdom. I båda celltyperna togs de inkommande klumparna upp och skickades till små återvinningskompartment kallade lysosomer. Neuroner ackumulerade dock betydligt fler klumpar i sina lysosomer än mikroglia. Med tiden blev neuronernas lysosomer mindre sura och mindre kapabla att bryta ner ett testprotein, vilket visar att deras grundläggande återvinningsfunktion försämrades. Mikrogliala lysosomer, däremot, bevarade i stort sett sin surhet och nedbrytningskapacitet även när de innehöll alfa‑synuklein.
När återvinningen misslyckas sprids skadan
Skadade lysosomer kan läcka och brista. Genom att använda markörer för membranskador och reparationsproteiner fann forskarna att neuroner upplevde mycket mer lysosomal skada än mikroglia efter exponering för alfa‑synuklein. De påverkade lysosomerna i neuroner förlorade rörlighet och klumpade ihop sig, ett annat tecken på dysfunktion. Mikroglia svarade annorlunda: de aktiverade en process kallad lysofagi, en riktad borttagning av skadade lysosomer, samtidigt som de ökade bildningen av nya lysosomer. Ett huvudreglerande protein som driver genprogram för lysosomer och städning flyttade in i kärnan i båda celltyperna, men endast i mikroglia slog de efterföljande gener på kraftfullt. Denna asymmetri innebär att neuroner har svårt att återställa sitt återvinningssystem, medan mikroglia kan förnya sitt.
Autofagi: igentäppt i neuroner, ökad i mikroglia
Proteinklumpers hanteras normalt av autofagi, en väg som omsluter oönskat material och levererar det till lysosomer. Teamet mätte autofagiskt ”flöde” och fann att alfa‑synuklein i hög grad blockerade detta flöde i neuroner men inte i mikroglia. Neuroner exponerade för klumpar visade en uppbyggnad av ett cargo‑adapterprotein (p62) utan ytterligare ökning när vägarnas slutsteg kemiskt blockerades, vilket är förenligt med ett stannat transportband. Mikroglia, däremot, producerade mer p62 och visade en stark ökning när slutsteget blockerades, vilket indikerar en fortfarande fungerande, till och med uppreglerad, väg. Mikroskopi visade många fler platser i mikroglia där alfa‑synuklein, autofagimarkörer och lysosomer möttes, vilket tyder på att mikroglia är mycket bättre på att känna igen och dirigera klumpar för nedbrytning.
Nanotub‑motorvägar för giftigt gods
Vad händer när neuroner inte hinner med sopningen? Studien visar att de skickar problemet vidare till mikroglia. När autofagin i alfa‑synuklein‑belastade neuroner kemiskt hämmades överfördes fler klumpar till närliggande mikroglia, och när autofagin stimulerades minskade överföringen. Dessa utbyten berodde inte på material som släpptes ut i odlingsmediet, utan på direkta cell‑till‑cell‑förbindelser. Författarna fokuserade på tunneling‑nanotuber — tunna, aktinbaserade broar mellan celler — och fann att blockering av autofagi i antingen neuroner eller mikroglia ökade både antalet sådana förbindelser och mängden generellt gods som rörde sig genom dem. Även när mikroglia var givare snarare än mottagare ökade överföringen till neuroner vid försämrad autofagi i mikroglia, vilket antyder att bristfällig självrensning är en signal som uppmuntrar celler att koppla upp sig och föra vidare aggregat.
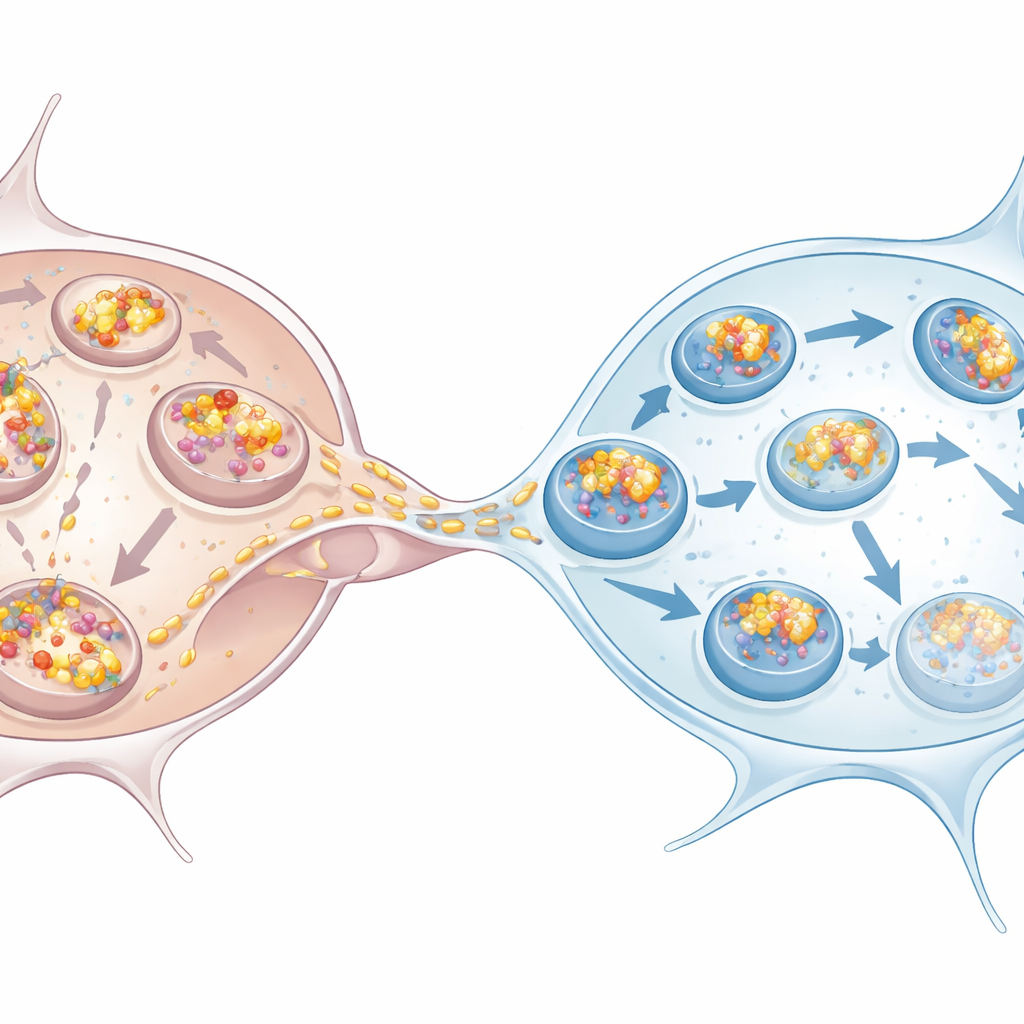
Mikroglia ställer upp
Arbetet granskade också dopaminerga neuroner och mikroglia härledda från mänskliga stamceller, som bättre liknar de celler som påverkas i Parkinsons sjukdom. Samma mönster framträdde: neuroner byggde upp mer alfa‑synuklein, visade tecken på försämrad autofagi och var beroende av mikroglia för att ta över bortforslingen. Mikroglia som växte tillsammans med överbelastade neuroner, eller till och med bara exponerades för deras betingade medium, ökade sin egen autofagi. När de mottog alfa‑synuklein via nanotuber hamnade en stor andel av de inkommande klumparna i p62‑markerade strukturer, förenligt med en väg mot nedbrytning. Samkultivering av neuroner med mikroglia minskade antalet och den totala lasten av klumpar inne i neuroner, vilket bekräftar att mikroglia fungerar som effektiva sänkor för giftiga aggregat.
Vad detta betyder för Parkinsons och vidare
För en icke‑specialist är huvudbudskapet att inte alla hjärnceller är lika rustade att hantera proteinavfall. Neuroner, särskilt de som är sårbara vid Parkinsons sjukdom, har sköra återvinningssystem som kan överväldigas av alfa‑synuklein‑klumpar. Mikroglia är däremot mer robusta städare och kan hjälpa neuroner genom att ta upp och bryta ner deras överskott av aggregat via små nanotub‑broar. Men denna hjälp kommer till priset av att samma process också kan underlätta spridningen av sjukdomsrelaterade proteiner genom hjärnan. Terapi som återställer neuronal autofagi eller finjusterar mikroglials rensningsfunktion skulle kunna minska den giftiga lasten inne i enskilda celler och samtidigt bromsa cell‑till‑cell‑spridningen av skadliga proteinklumpar.
Citering: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Nyckelord: Parkinsons sjukdom, alfa-synuklein, mikroglia, autofagi, tunneling‑nanotuber