Clear Sky Science · ar
ضعف التخلص من تراكمات $$\alpha$$-سينوكلين في الخلايا العصبية يدفع انتشارها إلى الخلايا الدبقية الصغيرة عبر الأنابيب النفقية
لماذا تهم تكتلات البروتين الصغيرة لصحة الدماغ
تتصف مرض باركنسون والاضطرابات ذات الصلة بتراكم تدريجي لتكتلات من بروتين يُسمى ألفا‑سينوكلين داخل خلايا الدماغ. يمكن أن تُلحق هذه التكتلات ضرراً بالخلايا، لكن الدماغ ليس بلا دفاع: فله آليات تنظيف وخلايا داعمة. تستقصي هذه الدراسة كيفية تقاسم الخلايا العصبية والخلايا المناعية الدماغية عبء إزالة هذه التكتلات، وكيف أن نوعاً قليلاً معلوماً من الجسور الخلوية، المسمى الأنابيب النفقية، يتحول إلى طريق سريع لنقل المواد السامة من الخلايا العصبية المتعثرة إلى الخلايا الدبقية الصغيرة الأكثر تحمّلاً.
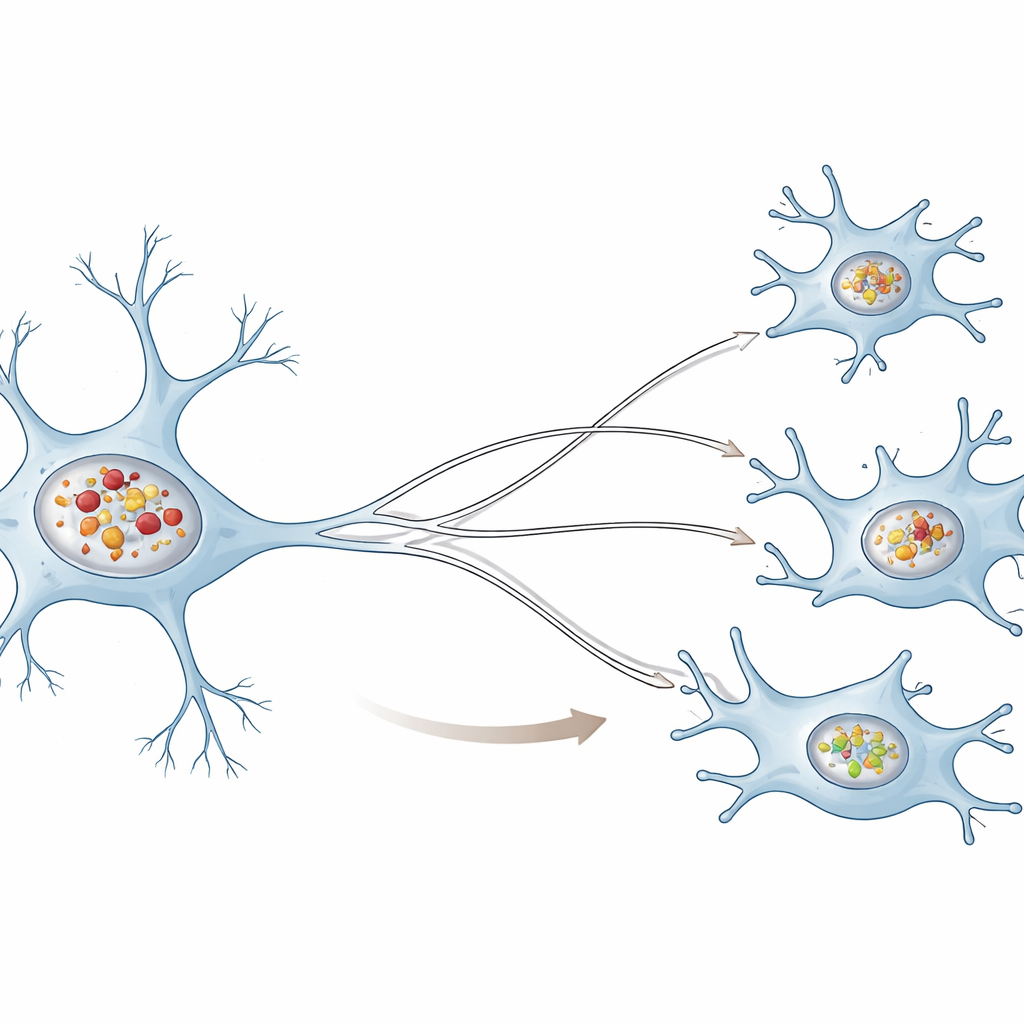
فريقان مختلفان تماماً للتنظيف
قارن الباحثون بين خلايا شبيهة بالعصبونات البشرية وخلايا دبقية صغيرة بشرية، وهي خلايا جهاز المناعة المقيمة في الدماغ، وعرضوا كلا النوعين لألياف ألفا‑سينوكلين المكوّنة مسبقاً، وهي نسخة مخبرية من التكتلات الضارة المرصودة في المرض. في كلا النوعين، تم ابتلاع التكتلات الواردة وإرسالها إلى حويصلات إعادة التدوير الصغيرة المسماة الجسيمات الحالة. مع ذلك، تراكمت التكتلات داخل جسيمات الخلايا العصبية أكثر بكثير مما حدث في الخلايا الدبقية الصغيرة. مع مرور الوقت، أصبحت جسيمات الخلايا العصبية أقل حمضية وكانت أقل قدرة على تحطيم بروتين اختبار، مما يدل على تراجع وظيفة إعادة التدوير الأساسية لديها. بالمقابل، حافظت جسيمات الخلايا الدبقية الصغيرة إلى حد كبير على حموضتها وقدرتها على التحلل حتى عندما احتوت على ألفا‑سينوكلين.
عندما يفشل إعادة التدوير، ينتشر الضرر
يمكن أن تتسرب الجسيمات التالفة أو تتمزق. باستخدام علامات لكسور الغشاء وبروتينات إصلاحه، وجد الباحثون أن الخلايا العصبية تعرضت لضرر في الجسيمات أكبر بكثير من الخلايا الدبقية الصغيرة بعد التعرض لألفا‑سينوكلين. فقدت الجسيمات المتضررة في الخلايا العصبية حركيتها وتجَمّعت، وهو علامة أخرى على الخلل. استجابت الخلايا الدبقية الصغيرة بشكل مختلف: فعَّلت عملية تسمى ليزوفاجي، وهي إزاحة مستهدفة للجسيمات التالفة، وبطريقة متزامنة زادت من تكوين جسيمات حالة جديدة. انتقل بروتين ضابط رئيسي يحفز برامج الجينات المتعلقة بالجسيمات والحَسَب التنظيفي إلى نواة كلتا الخلقتين، لكن الجينات اللاحقة فعّلت بقوة فقط في الخلايا الدبقية الصغيرة. تعني هذه اللامتماثلية أن الخلايا العصبية تكافح لاستعادة نظام إعادة التدوير لديها، بينما تستطيع الخلايا الدبقية تجديد نظامها.
الالتهام الذاتي: انسداد في الخلايا العصبية، وتعزيز في الخلايا الدبقية الصغيرة
عادةً ما تُعالج تكتلات البروتين عبر الالتهام الذاتي، وهو مسار يحيط بالمواد غير المرغوب فيها ويوصلها إلى الجسيمات الحالة. قيَّم الفريق "تدفق" الالتهام الذاتي ووجد أن ألفا‑سينوكلين أعاق هذا التدفق في الخلايا العصبية إلى حد كبير لكنه لم يفعل ذلك في الخلايا الدبقية الصغيرة. أظهرت الخلايا العصبية المعرضة للتكتلات تراكم بروتين وسطاء الشحنة (p62) دون زيادة إضافية عندما تم حجب الخطوة النهائية للمسار كيميائياً، وهو ما يتوافق مع سير ناقل تجمَّد. بالمقابل، صنعت الخلايا الدبقية الصغيرة المزيد من p62 وأظهرت ارتفاعاً قوياً عندما حُجبت الخطوة النهائية، مما يشير إلى أن المسار ما زال يعمل بل وربما مُعزَّز. كشفت الميكروسكوبات عن مواقع أكثر بكثير في الخلايا الدبقية الصغيرة حيث التقت ألفا‑سينوكلين وعلامات الالتهام الذاتي والجسيمات الحالة، مما يوحي بأن الخلايا الدبقية الصغيرة أفضل بكثير في التعرف على التكتلات وتوجيهها نحو التحلل.
طرق النانو‑أنابيب للشحنات السامة
ماذا يحدث عندما لا تواكب الخلايا العصبية حجم النفايات؟ تظهر الدراسة أنها تمرر المشكلة إلى الخلايا الدبقية الصغيرة. عندما حُجِب الالتهام الذاتي كيميائياً في الخلايا العصبية المحمَّلة بألفا‑سينوكلين، انتقل المزيد من التكتلات إلى الخلايا الدبقية المجاورة، وعندما نُشِّط الالتهام الذاتي انخفض النقل. لم تعتمد هذه التبادلات على المواد المُطلقة في وسط الزرع، مما يشير بدلاً من ذلك إلى وصلات خلوية مباشرة. ركز الباحثون على الأنابيب النفقية—جسور رفيعة مرتكزة على الأكتين بين الخلايا—ووجدوا أن حجب الالتهام الذاتي في الخلايا العصبية أو الخلايا الدبقية الصغيرة زاد كلاً من عدد هذه الوصلات وكمية الشحنات العامة التي تمر عبرها. حتى عندما كانت الخلايا الدبقية الصغيرة هي المانح بدلاً من المستلم، أدى إضعاف الالتهام الذاتي لديها إلى زيادة النقل إلى الخلايا العصبية، مما يوحي بأن فشل التنظيف الذاتي هو إشارة تشجع الخلايا على الاتصال وتمرير التكتلات.
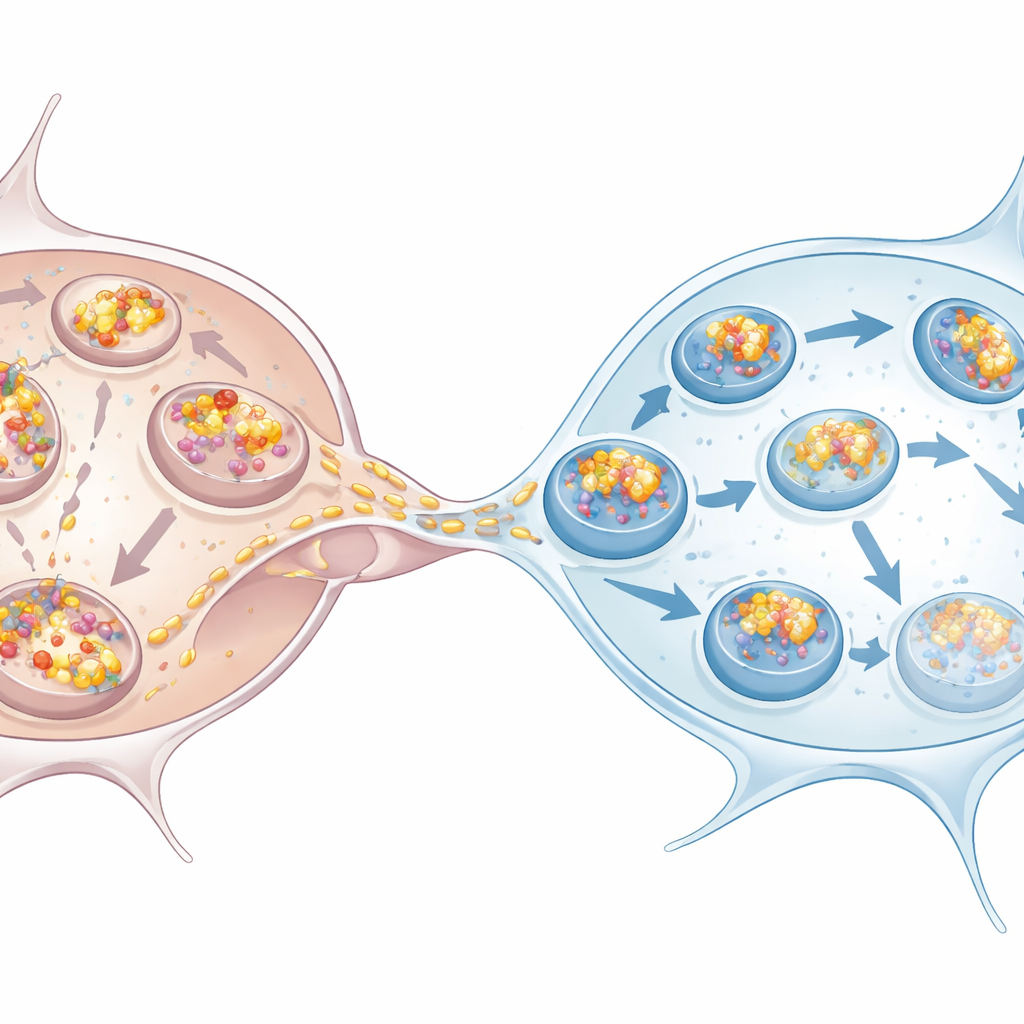
الخلايا الدبقية الصغيرة تنهض لمواجهة التحدي
فحص العمل أيضاً خلايا عصبية ناقلة للدوبامين مشتقة من الخلايا الجذعية البشرية والخلايا الدبقية الصغيرة، التي تشبه أفضل الخلايا المتأثرة في مرض باركنسون. ظهر النمط نفسه: تراكمت في الخلايا العصبية المزيد من ألفا‑سينوكلين، وأظهرت علامات ضعف الالتهام الذاتي، واعتمدت على الخلايا الدبقية الصغيرة لتولي التخلص. عزَّزت الخلايا الدبقية الصغيرة المزروعة جنباً إلى جنب مع الخلايا العصبية المتراكمة، أو حتى المعرضة فقط لوسطها المهوّى، الالتهام الذاتي الخاص بها. عندما استلمت ألفا‑سينوكلين عبر الأنابيب النفقية، انتهى جزء كبير من التكتلات الواردة في هياكل مُميزة بـ p62، وهو متسق مع مسار نحو التحلل. أدت تعايش الخلايا العصبية مع الخلايا الدبقية الصغيرة إلى تقليل عدد التكتلات والحمولة الإجمالية داخل الخلايا العصبية، مؤكداً أن الخلايا الدبقية الصغيرة تعمل كحوض فعال لالتقاط التكتلات السامة.
ماذا يعني هذا لمرض باركنسون وما بعده
بالنسبة للقارئ غير المتخصص، الرسالة الرئيسية هي أن ليس كل خلايا الدماغ مجهزة بنفس القدر للتعامل مع نفايات البروتين. الخلايا العصبية، وخصوصاً تلك الضعيفة في مرض باركنسون، تملك أنظمة إعادة تدوير هشة يمكن أن تُغمر بتكتلات ألفا‑سينوكلين. بالمقابل، الخلايا الدبقية الصغيرة منظّفة أكثر متانة ويمكن أن تساعد في إنقاذ الخلايا العصبية عبر استيعاب وتحطيم فائض التكتلات عبر جسور نانوية ضئيلة. لكن هذا العون له ثمن: قد يساعد نفس العملية أيضاً في نشر البروتينات المرتبطة بالمرض عبر الدماغ. قد تساهم العلاجات التي تستعيد الالتهام الذاتي الخلوي أو تضبط تنظيف الخلايا الدبقية الصغيرة بدقة في خفض العبء السام داخل الخلايا الفردية وكذلك إبطاء الانتشار الخلوي لتكتلات البروتين الضارة.
الاستشهاد: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
الكلمات المفتاحية: مرض باركنسون, ألفا-سينوكلين, الخلايا الدبقية الصغيرة, الالتهام الذاتي, الأنابيب النفقية