Clear Sky Science · pt
Limpeza prejudicada de agregados de $$\alpha$$-sinucleína em células neuronais impulsiona sua disseminação para micróglias através de nanotubos de túnel
Por que pequenos aglomerados de proteína importam para a saúde do cérebro
A doença de Parkinson e transtornos relacionados são marcados pelo acúmulo lento de aglomerados de uma proteína chamada alfa‑sinucleína dentro das células cerebrais. Esses aglomerados podem danificar as células, mas o cérebro não está indefeso: ele possui seus próprios times de limpeza e células de suporte. Este estudo investiga como neurônios e células imunes do cérebro compartilham o ônus de eliminar esses aglomerados, e como um tipo pouco conhecido de ponte entre células, chamado nanotubo de túnel, torna‑se uma rodovia para transferir material tóxico de neurônios em dificuldade para micróglias mais resistentes.
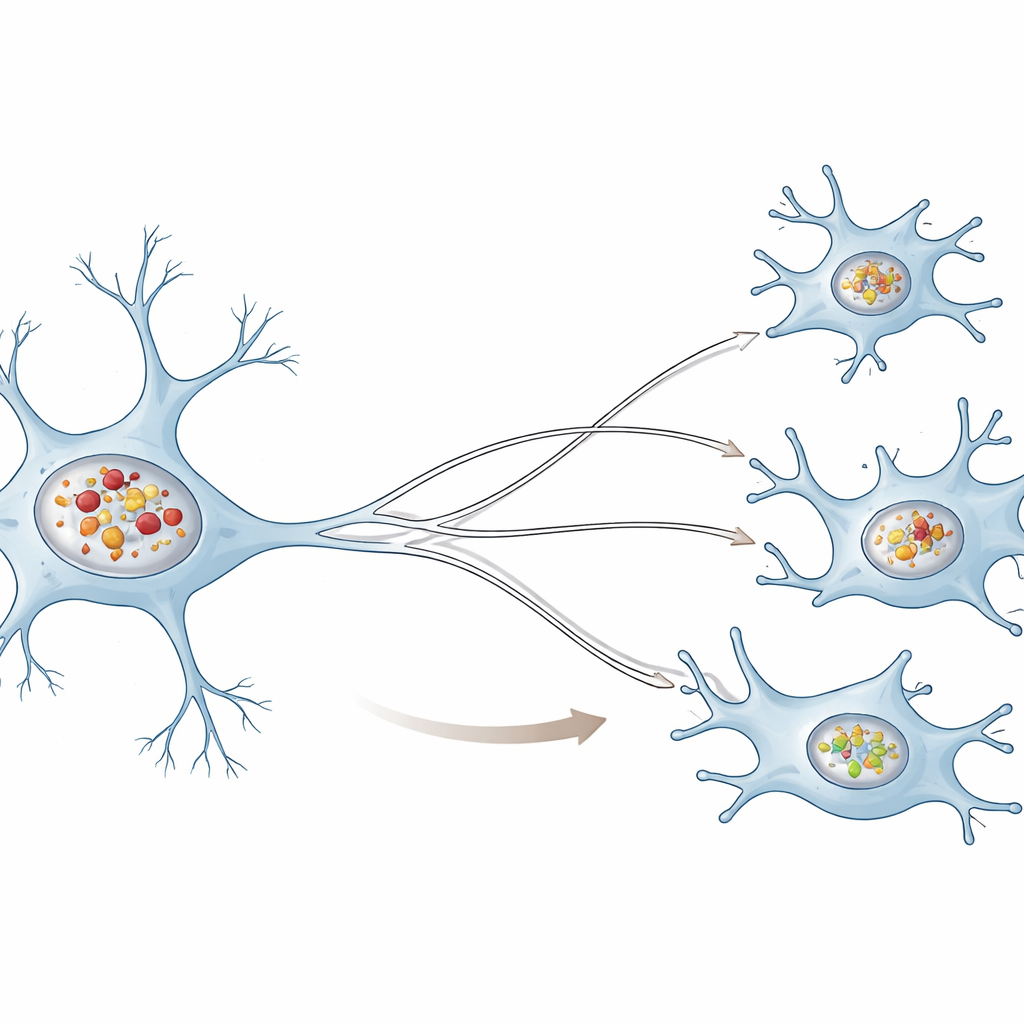
Dois times de limpeza muito diferentes
Os autores compararam células humanas do tipo neuronal com micróglias humanas, as células imunes residentes do cérebro, e expuseram ambos a fibrilas pré‑formadas de alfa‑sinucleína, uma versão laboratorial dos aglomerados nocivos observados na doença. Em ambos os tipos celulares, os aglomerados entraram e foram enviados para pequenos compartimentos de reciclagem chamados lisossomos. No entanto, os neurônios acumularam muito mais aglomerados dentro de seus lisossomos do que as micróglias. Com o tempo, os lisossomos neuronais tornaram‑se menos ácidos e menos capazes de degradar uma proteína teste, mostrando que sua função central de reciclagem estava falhando. Os lisossomos das micróglias, em contraste, preservaram em grande parte sua acidez e capacidade de degradação mesmo quando continham alfa‑sinucleína.
Quando a reciclagem falha, o dano se espalha
Lisossomos danificados podem vazar e romper. Usando marcadores de quebra de membrana e proteínas de reparo, os pesquisadores descobriram que os neurônios sofreram muito mais lesão lisossomal do que as micróglias após a exposição à alfa‑sinucleína. Os lisossomos afetados nos neurônios perderam mobilidade e se aglomeraram, outro sinal de disfunção. As micróglias responderam de forma diferente: ativaram um processo chamado lisofagia, uma remoção direcionada de lisossomos danificados, e ao mesmo tempo aumentaram o surgimento de novos lisossomos. Uma proteína controladora mestre que regula programas genéticos de lisossomos e limpeza translocou para o núcleo em ambos os tipos celulares, mas apenas nas micróglias os genes a jusante foram fortemente ativados. Essa assimetria significa que os neurônios têm dificuldade em restaurar seu sistema de reciclagem, enquanto as micróglias conseguem renovar o delas.
Autofagia: obstruída em neurônios, reforçada em micróglias
Os aglomerados de proteína são normalmente tratados pela autofagia, uma via que envolve o material indesejado e o entrega aos lisossomos. A equipe mediu o “fluxo” de autofagia e constatou que a alfa‑sinucleína bloqueou em grande parte esse fluxo nos neurônios, mas não nas micróglias. Neurônios expostos aos aglomerados mostraram acúmulo de uma proteína adaptadora de carga (p62) sem aumento adicional quando a etapa final da via foi quimicamente bloqueada, consistente com uma esteira rolante parada. As micróglias, por outro lado, produziram mais p62 e exibiram forte aumento quando a etapa final foi bloqueada, indicando uma via ainda em funcionamento e até regulada para cima. A microscopia revelou muitos mais locais nas micróglias onde alfa‑sinucleína, marcadores de autofagia e lisossomos se encontravam, sugerindo que as micróglias são muito melhores em reconhecer e encaminhar aglomerados para destruição.
Rodovias nanotubulares para carga tóxica
O que acontece quando os neurônios não conseguem acompanhar o lixo? O estudo mostra que eles repassam o problema para as micróglias. Quando a autofagia em neurônios carregados de alfa‑sinucleína foi quimicamente inibida, mais aglomerados foram transferidos para micróglias vizinhas, e quando a autofagia foi estimulada, a transferência diminuiu. Essas trocas não dependiam de material liberado no meio de cultura, apontando em vez disso para conexões diretas entre células. Os autores focaram nos nanotubos de túnel — pontes finas, baseadas em actina, entre células — e descobriram que bloquear a autofagia em neurônios ou micróglias aumentou tanto o número dessas conexões quanto a quantidade de carga geral que passava por elas. Mesmo quando as micróglias eram doadoras em vez de receptoras, prejudicar sua autofagia aumentou a transferência para os neurônios, sugerindo que a limpeza deficiente funciona como um sinal que incentiva as células a se conectar e repassar agregados.
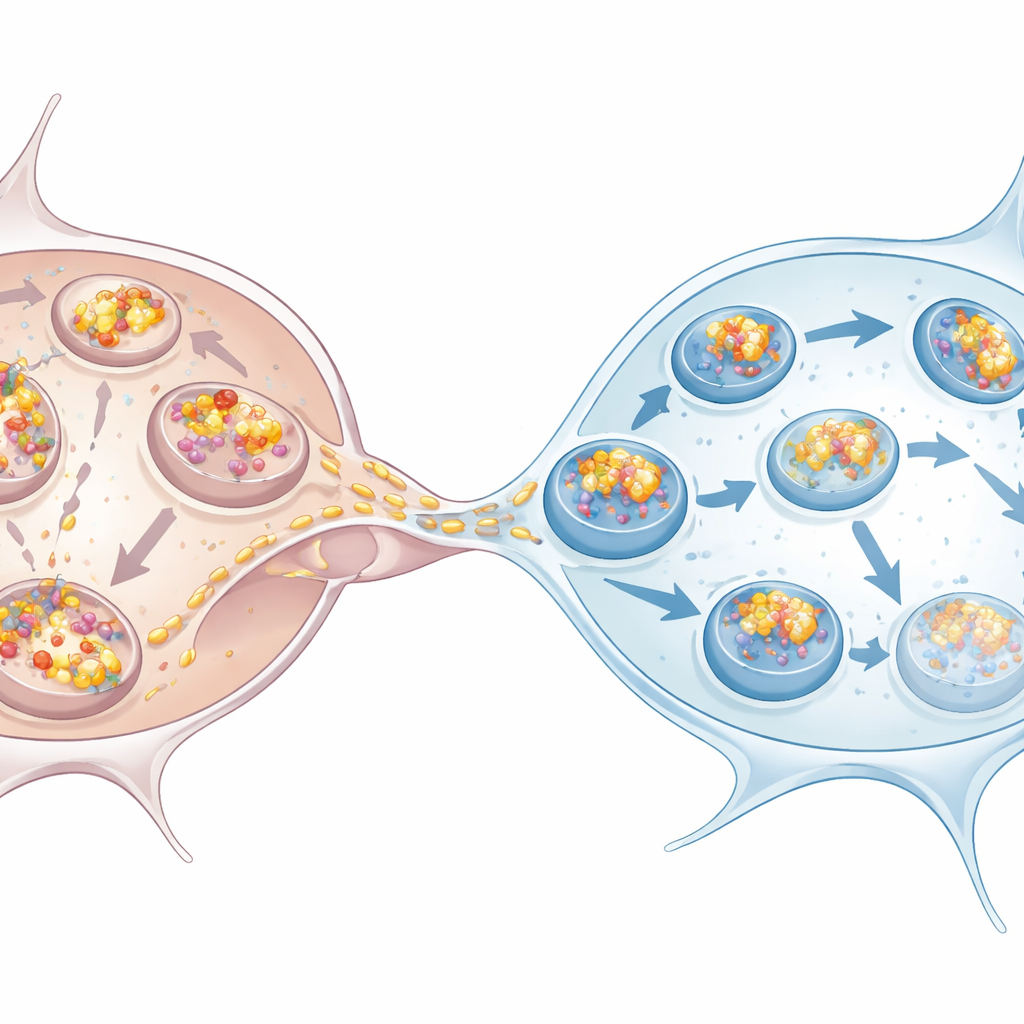
Micróglias se mostram à altura do desafio
O trabalho também examinou neurônios dopaminérgicos derivados de células‑tronco humanas e micróglias, que se assemelham melhor às células afetadas na doença de Parkinson. O mesmo padrão emergiu: os neurônios acumularam mais alfa‑sinucleína, mostraram sinais de autofagia prejudicada e dependeram das micróglias para assumir a eliminação. Micróglias cultivadas ao lado de neurônios sobrecarregados, ou mesmo apenas expostas ao meio condicionado por eles, aumentaram sua própria autofagia. Uma vez que receberam alfa‑sinucleína via nanotubos, uma grande fração dos aglomerados entrantes terminou em estruturas marcadas por p62, consistente com uma rota rumo à degradação. Co‑cultivar neurônios com micróglias reduziu o número e a carga total de aglomerados dentro dos neurônios, confirmando que as micróglias atuam como sumidouros eficazes para agregados tóxicos.
O que isso significa para Parkinson e além
Para um público não especializado, a mensagem principal é que nem todas as células cerebrais estão igualmente preparadas para lidar com o lixo proteico. Neurônios, especialmente os vulneráveis na doença de Parkinson, têm sistemas de reciclagem frágeis que podem ser sobrecarregados por aglomerados de alfa‑sinucleína. As micróglias, em contraste, são limpadoras mais robustas e podem ajudar a salvar neurônios ao absorver e degradar seus agregados em excesso por meio de minúsculas pontes nanotubulares. Mas essa ajuda tem um custo: o mesmo processo pode também facilitar a propagação de proteínas relacionadas à doença pelo cérebro. Terapias que restabeleçam a autofagia neuronal ou ajustem a limpeza microglial podem não apenas reduzir a carga tóxica dentro de células individuais, mas também desacelerar a propagação célula a célula de aglomerados proteicos danosos.
Citação: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Palavras-chave: Doença de Parkinson, alfa-sinucleína, micróglias, autofagia, nanotubos de túnel