Clear Sky Science · de
Beeinträchtigte $$\alpha$$-Synuclein-Aggregatbeseitigung in Nervenzellen treibt ihre Ausbreitung auf Mikroglia über Tunneling-Nanotubes
Warum winzige Proteinansammlungen für die Gehirngesundheit wichtig sind
Die Parkinson-Krankheit und verwandte Störungen sind durch die langsame Ansammlung von Klumpen des Proteins Alpha‑Synuclein in Gehirnzellen gekennzeichnet. Diese Aggregate können Zellen schädigen, doch das Gehirn ist nicht wehrlos: Es verfügt über eigene Aufräumtruppen und Stützzellen. Diese Studie untersucht, wie Nervenzellen und Gehirn-Immunzellen die Last der Beseitigung dieser Klumpen teilen und wie eine wenig bekannte Art von Zell‑zu‑Zell‑Brücke, sogenannte Tunneling‑Nanotubes, zur Autobahn wird, über die toxisches Material aus angeschlagenen Neuronen in widerstandsfähigere Mikroglia gelangt.
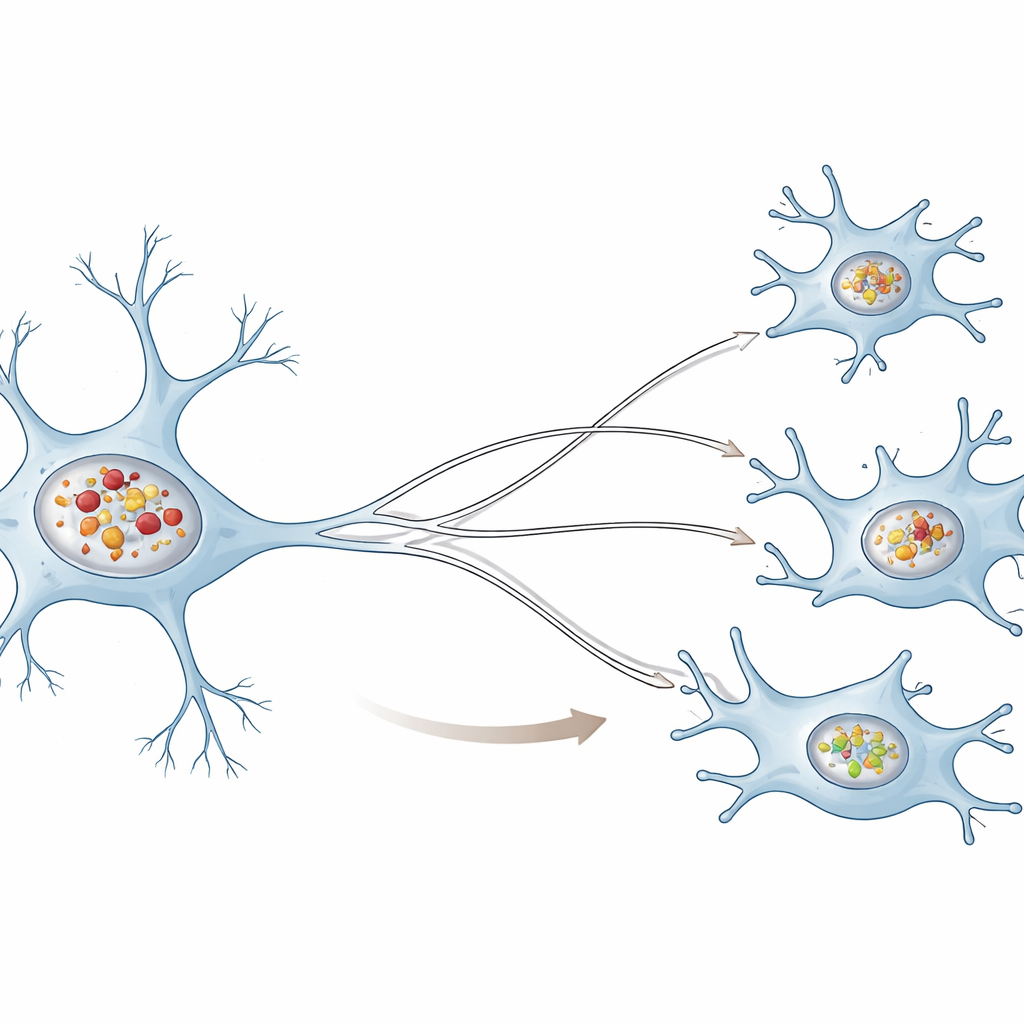
Zwei sehr unterschiedliche Aufräumtruppen
Die Autor:innen verglichen humane neuronähnliche Zellen mit humanen Mikroglia, den residenten Immunzellen des Gehirns, und setzten beide Zelltypen vorgeformten Alpha‑Synuclein‑Fibrillen aus, einer Laborversion der schädlichen Aggregate, die bei der Krankheit zu finden sind. In beiden Zelltypen wurden die eingehenden Aggregate aufgenommen und in kleine Recyclingkompartimente, die Lysosomen, gebracht. Neuronen häuften jedoch deutlich mehr Aggregate in ihren Lysosomen an als Mikroglia. Im Laufe der Zeit wurden neuronale Lysosomen weniger sauer und weniger fähig, ein Testprotein abzubauen, was zeigt, dass ihre zentrale Recyclingfunktion nachließ. Im Gegensatz dazu bewahrten mikrogliale Lysosomen weitgehend ihre Säure und Abbaukapazität, selbst wenn sie Alpha‑Synuclein enthielten.
Wenn das Recycling versagt, breitet sich Schaden aus
Beschädigte Lysosomen können undicht werden oder aufreißen. Mithilfe von Markern für Membranschäden und Reparaturproteinen fanden die Forschenden heraus, dass Neuronen nach Alpha‑Synuclein‑Exposition deutlich mehr lysosomale Schäden erlitten als Mikroglia. Die betroffenen Lysosomen in Neuronen verloren ihre Mobilität und klumpten zusammen, ein weiteres Zeichen für Dysfunktion. Mikroglia reagierten anders: Sie schalteten einen Prozess namens Lysophagie ein, die gezielte Entfernung beschädigter Lysosomen, und gleichzeitig förderten sie die Entstehung neuer Lysosomen. Ein Master‑Kontrollprotein, das Lysosom‑ und Aufräum‑Genprogramme steuert, wanderte in den Zellkern beider Zelltypen, doch nur in Mikroglia wurden die nachgeschalteten Gene kräftig aktiviert. Diese Asymmetrie bedeutet, dass Neuronen Schwierigkeiten haben, ihr Recyclingsystem wiederherzustellen, während Mikroglia es erneuern können.
Autophagie: verstopft in Neuronen, verstärkt in Mikroglia
Proteinaggregate werden normalerweise durch Autophagie gehandhabt, einen Weg, der unerwünschtes Material umschließt und zu Lysosomen liefert. Das Team maß den Autophagie‑"Flux" und fand, dass Alpha‑Synuclein diesen Fluss in Neuronen weitgehend blockierte, nicht aber in Mikroglia. Neuronen, die den Klumpen ausgesetzt waren, zeigten eine Anhäufung eines Fracht‑Adapter‑Proteins (p62), ohne dass es bei chemischer Blockade des letzten Schritts der Bahn zu einem weiteren Anstieg kam — was einem stillstehenden Förderband entspricht. Mikroglia hingegen produzierten mehr p62 und zeigten bei Blockade des letzten Schritts einen starken Anstieg, was auf einen noch laufenden, sogar hochregulierten Weg hindeutet. Die Mikroskopie zeigte in Mikroglia deutlich mehr Stellen, an denen Alpha‑Synuclein, Autophagie‑Marker und Lysosomen zusammenkamen, was darauf hindeutet, dass Mikroglia viel besser darin sind, Aggregate zu erkennen und zur Zerstörung zu leiten.
Nanotuben‑Autobahnen für toxische Fracht
Was passiert, wenn Neuronen mit dem Müll nicht mehr nachkommen? Die Studie zeigt, dass sie das Problem an Mikroglia weiterreichen. Wenn die Autophagie in Alpha‑Synuclein‑beladenen Neuronen chemisch gehemmt wurde, wurden mehr Aggregate auf benachbarte Mikroglia übertragen; wenn die Autophagie angeregt wurde, sank die Übertragung. Diese Austausche hingen nicht von in das Kulturmedium freigesetzten Materialien ab, sondern von direkten Zell‑zu‑Zell‑Verbindungen. Die Autor:innen konzentrierten sich auf Tunneling‑Nanotubes — dünne, aktinbasierte Brücken zwischen Zellen — und fanden, dass die Blockade der Autophagie in Neuronen oder Mikroglia sowohl die Anzahl dieser Verbindungen als auch die Menge an allgemeiner Fracht, die hindurch bewegt wurde, erhöhte. Selbst wenn Mikroglia Spender statt Empfänger waren, erhöhte eine Beeinträchtigung ihrer Autophagie die Übertragung an Neuronen, was darauf hindeutet, dass fehlerhaftes Selbstrecycling ein Signal ist, das Zellen dazu anregt, Verbindungen aufzubauen und Aggregate weiterzugeben.
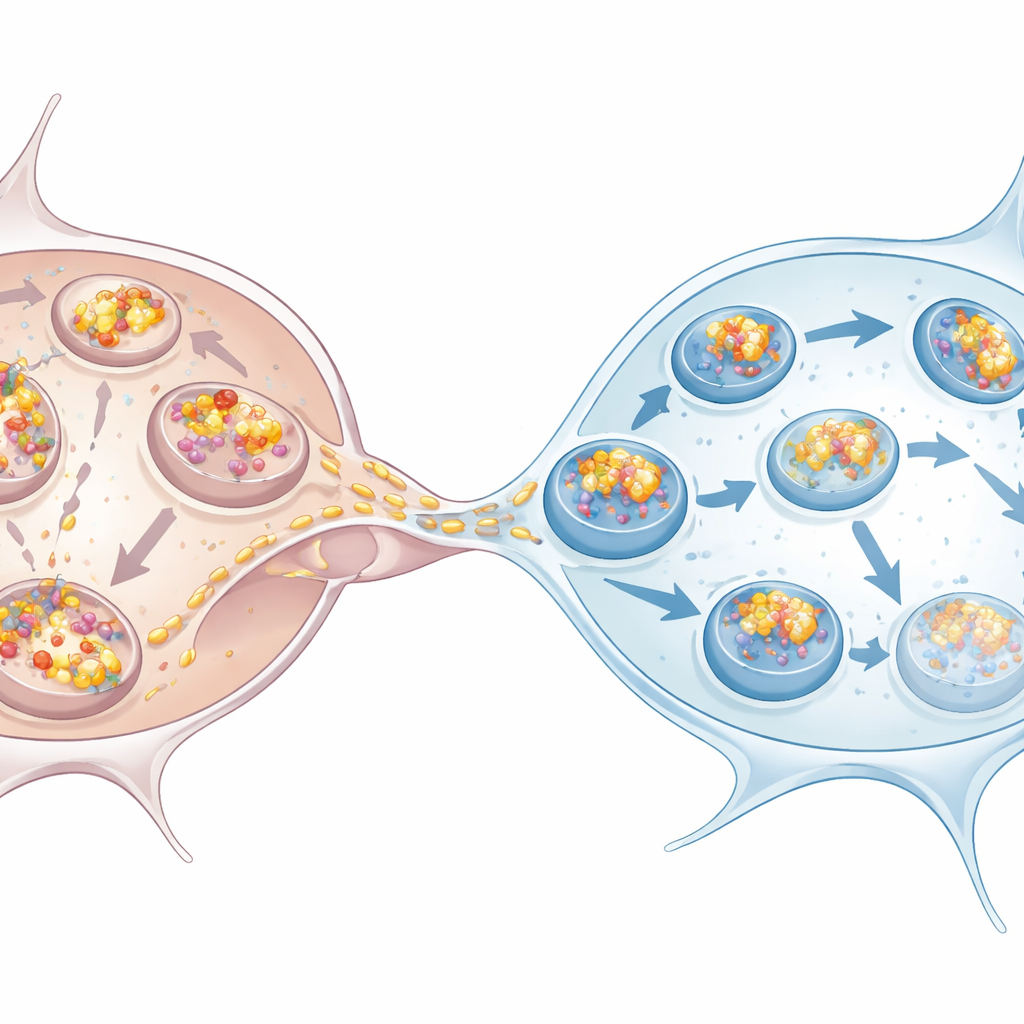
Mikroglia meistern die Herausforderung
Die Arbeit untersuchte außerdem aus menschlichen Stammzellen gewonnene dopaminerge Neuronen und Mikroglia, die den in der Parkinson‑Krankheit betroffenen Zellen näher kommen. Dasselbe Muster zeigte sich: Neuronen häuften mehr Alpha‑Synuclein an, zeigten Anzeichen einer beeinträchtigten Autophagie und waren auf Mikroglia angewiesen, um die Entsorgung zu übernehmen. Mikroglia, die neben überlasteten Neuronen gezüchtet wurden oder sogar nur ihrem konditionierten Medium ausgesetzt waren, steigerten ihre eigene Autophagie. Sobald sie Alpha‑Synuclein über Nanotubes erhielten, landete ein großer Anteil der eingehenden Aggregate in p62‑markierten Strukturen, was mit einem Weg zur Degradation vereinbar ist. Das Co‑Kultivieren von Neuronen mit Mikroglia verringerte Anzahl und Gesamtbelastung der Aggregate in Neuronen und bestätigte, dass Mikroglia als effektive Senken für toxische Aggregate fungieren.
Was das für Parkinson und darüber hinaus bedeutet
Für Nicht‑Spezialist:innen ist die Hauptaussage: Nicht alle Gehirnzellen sind gleichermaßen gerüstet, mit Proteinabfall umzugehen. Neuronen, insbesondere jene, die bei Parkinson anfällig sind, haben fragile Recyclingsysteme, die durch Alpha‑Synuclein‑Klumpen überfordert werden können. Mikroglia sind dagegen robustere Reiniger und können Neuronen helfen, indem sie deren überschüssige Aggregate über winzige Nanotuben‑Brücken aufnehmen und abbauen. Diese Hilfe hat jedoch einen Preis: Derselbe Prozess könnte auch die Ausbreitung krankheitsrelevanter Proteine im Gehirn begünstigen. Therapien, die die neuronale Autophagie wiederherstellen oder die mikrogliale Aufräumarbeit feinjustieren, könnten nicht nur die toxische Belastung in einzelnen Zellen senken, sondern auch die Zell‑zu‑Zell‑Ausbreitung schädlicher Proteinaggregate verlangsamen.
Zitation: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Schlüsselwörter: Morbus Parkinson, alpha-Synuclein, Mikroglia, Autophagozytose, Tunneling-Nanotubes