Clear Sky Science · pl
Uporczywe usuwanie agregatów $$\alpha$$-synukleiny w komórkach nerwowych napędza ich rozprzestrzenianie się do mikrogleju przez nanoprzełączniki (tunneling nanotubes)
Dlaczego małe skupiska białka mają znaczenie dla zdrowia mózgu
Choroba Parkinsona i powiązane zaburzenia charakteryzują się stopniowym gromadzeniem się grudek białka zwanego alfa‑synukleiną wewnątrz komórek mózgu. Te agregaty mogą uszkadzać komórki, ale mózg nie jest bezbronny: dysponuje własnymi mechanizmami oczyszczania i komórkami wspomagającymi. W badaniu przeanalizowano, jak neurony i komórki odpornościowe mózgu dzielą się zadaniem usuwania tych grudek oraz w jaki sposób mało znany rodzaj połączenia międzykomórkowego — tzw. tunneling nanotube (nanoprzełącznik) — staje się autostradą do przenoszenia toksycznego materiału z osłabionych neuronów do odporniejszych mikroglejów.
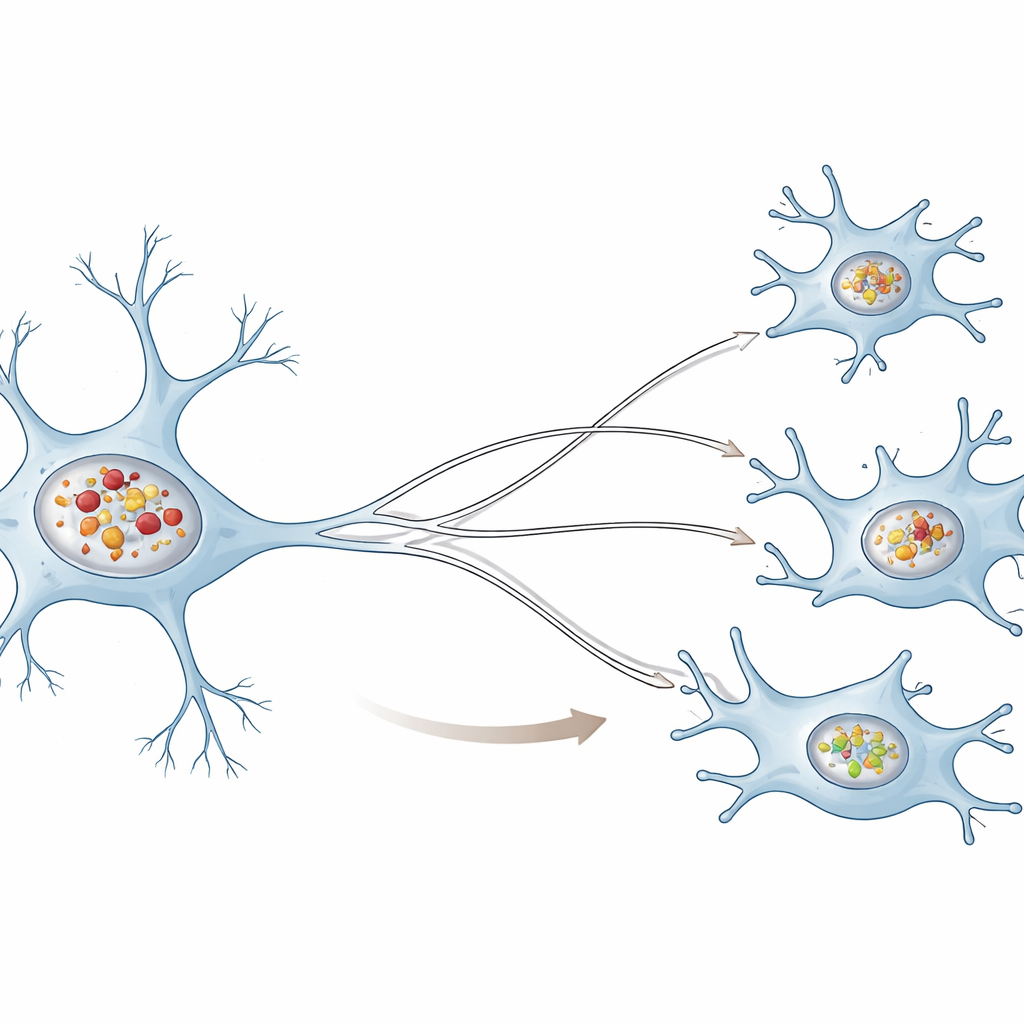
Dwie bardzo różne ekipy sprzątające
Autorzy porównali komórki o cechach ludzkich neuronów z ludzkimi mikroglejami, rezydentnymi komórkami odpornościowymi mózgu, i wystawili obie na preformowane fibryle alfa‑synukleiny — laboratoryjną wersję szkodliwych grudek obserwowanych w chorobie. W obu typach komórek przyjęte agregaty były internalizowane i kierowane do małych „kompartmentów recyklingowych” zwanych lizosomami. Jednak neurony gromadziły w lizosomach znacznie więcej grudek niż mikrogleje. Z czasem lizosomy neuronalne stawały się mniej kwaśne i mniej zdolne do rozkładu testowego białka, co wskazuje na upośledzenie ich podstawowej funkcji recyklingu. Lizosomy mikrogleju, przeciwnie, w dużej mierze zachowywały kwasowość i zdolność do rozkładu nawet przy obecności alfa‑synukleiny.
Gdy recykling zawodzi, szkoda się rozprzestrzenia
Uszkodzone lizosomy mogą przeciekać i ulegać pękaniu. Przy użyciu znaczników przerwań błon i białek naprawczych badacze stwierdzili, że po ekspozycji na alfa‑synukleinę neurony doświadczyły znacznie więcej uszkodzeń lizosomów niż mikrogleje. Dotknięte lizosomy w neuronach traciły mobilność i tworzyły skupiska — kolejny sygnał dysfunkcji. Mikroglej zareagował inaczej: uruchomił proces zwany lizofagią, czyli selektywne usuwanie uszkodzonych lizosomów, a równocześnie zwiększył powstawanie nowych lizosomów. Kluczowy białkowy regulator, który steruje programami genów związanych z lizosomami i oczyszczaniem, przemieścił się do jądra w obu typach komórek, lecz tylko w mikrogleju docelowe geny zostały silnie aktywowane. Ta asymetria oznacza, że neurony mają trudności z przywróceniem systemu recyklingu, podczas gdy mikroglej potrafi go odnowić.
Autofagia: zatkana w neuronach, pobudzona w mikrogleju
Agregaty białkowe są zwykle usuwane przez autofagię — szlak, który otacza niechciany materiał i dostarcza go do lizosomów. Zespół zmierzył „przepływ” autofagii i odkrył, że alfa‑synukleina w dużej mierze blokuje ten proces w neuronach, ale nie w mikrogleju. Neurony narażone na grudki wykazywały nagromadzenie białka adaptora ładunku (p62) bez dalszego wzrostu po chemicznym zablokowaniu końcowego etapu szlaku, co jest zgodne z zatrzymaną taśmą transportową. Mikrogleje natomiast produkowały więcej p62 i wykazywały silny wzrost po zablokowaniu końcowego etapu, co wskazuje na działający, a nawet upregulowany, szlak. Mikroskopia ujawniła znacznie więcej miejsc w mikrogleju, gdzie alfa‑synukleina, markery autofagii i lizosomy zbiegały się, sugerując, że mikroglej znacznie lepiej rozpoznaje i kieruje grudki ku degradacji.
Nanoprzełącznikowe autostrady dla toksycznego ładunku
Co się dzieje, gdy neurony nie nadążają z usuwaniem odpadów? Badanie pokazuje, że przekazują problem mikroglejowi. Gdy autofagia w neuronach obciążonych alfa‑synukleiną została chemicznie zahamowana, więcej grudek było przekazywanych do sąsiednich mikroglejów, a stymulacja autofagii zmniejszała transfer. Wymiana ta nie zależała od materiału uwalnianego do płynu hodowlanego, lecz od bezpośrednich połączeń między komórkami. Autorzy skupili się na tunneling nanotubes — cienkich, opartych na aktynie mostkach międzykomórkowych — i odkryli, że blokada autofagii w neuronach lub mikrogleju zwiększała zarówno liczbę tych połączeń, jak i ilość ogólnego ładunku przechodzącego przez nie. Nawet gdy mikroglej pełnił rolę dawcy zamiast biorcy, upośledzenie jego autofagii zwiększało transfer do neuronów, co sugeruje, że wadliwe samooczyszczanie stanowi sygnał zachęcający komórki do łączenia się i przekazywania agregatów.
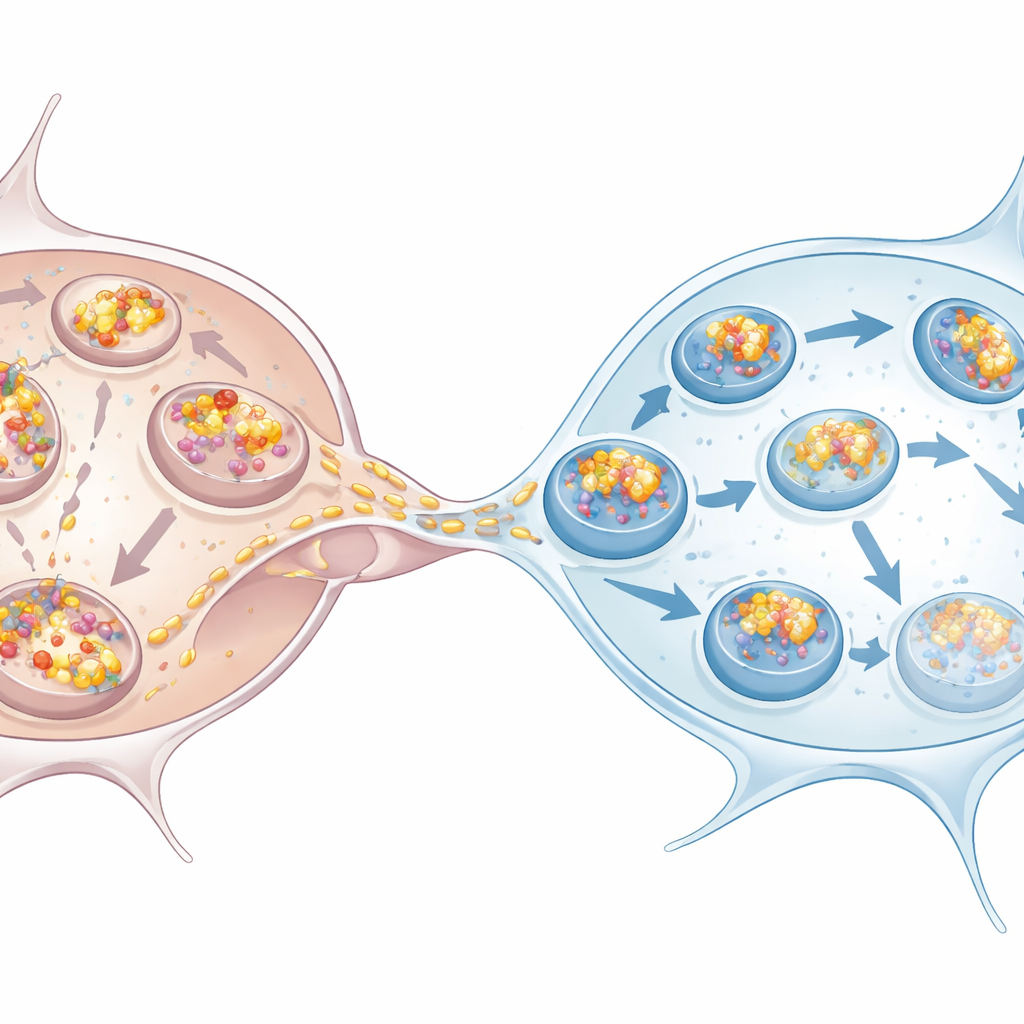
Mikroglej staje na wysokości zadania
Praca objęła także neurony dopaminergiczne i mikroglej pochodne z ludzkich komórek macierzystych, które lepiej przypominają komórki dotknięte w chorobie Parkinsona. Pojawił się ten sam wzorzec: neurony gromadziły więcej alfa‑synukleiny, wykazywały oznaki upośledzonej autofagii i polegały na mikrogleju w przejęciu utylizacji. Mikroglej hodowany razem z przeładowanymi neuronami, a nawet tylko wystawiony na ich medium warunkowane, zwiększał własną autofagię. Po otrzymaniu alfa‑synukleiny przez nanotuby duża część napływających grudek trafiała do struktur oznaczonych p62, zgodnie z drogą prowadzącą do degradacji. Ko‑hodowla neuronów z mikroglejem zmniejszała liczbę i całkowite obciążenie grudek wewnątrz neuronów, potwierdzając, że mikroglej działa jako skuteczne „zbiorniki” dla toksycznych agregatów.
Co to oznacza dla choroby Parkinsona i nie tylko
Dla odbiorcy niebędącego specjalistą główne przesłanie jest takie, że nie wszystkie komórki mózgowe są równie wyposażone do radzenia sobie z białkowym odpadem. Neurony, szczególnie te podatne w chorobie Parkinsona, mają kruche systemy recyklingu, które mogą zostać przytłoczone przez grudki alfa‑synukleiny. Mikroglej, przeciwnie, jest bardziej odpornym „sprzątaczem” i może pomóc uratować neurony, przyjmując i rozkładając ich nadmiar agregatów przez mikroskopijne nanotubowe mosty. Jednak ta pomoc ma swoją cenę: ten sam proces może także ułatwiać rozprzestrzenianie się białek związanych z chorobą po mózgu. Terapie przywracające autofagię w neuronach lub precyzyjnie regulujące czynność mikrogleju mogą nie tylko zmniejszyć toksyczne obciążenie w pojedynczych komórkach, lecz także spowolnić rozprzestrzenianie się szkodliwych grudek między komórkami.
Cytowanie: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Słowa kluczowe: Choroba Parkinsona, alfa-synukleina, mikroglej, autofagia, nanoprzełączniki (tunneling nanotubes)