Clear Sky Science · es
El aclarado de agregados de $$\alpha$$-sinucleína deteriorado en células neuronales impulsa su propagación a microglía mediante nanotúneles
Por qué importan los pequeños racimos de proteínas para la salud cerebral
La enfermedad de Parkinson y trastornos relacionados se caracterizan por la acumulación lenta de racimos de una proteína llamada alfa‑sinucleína dentro de las células cerebrales. Estos racimos pueden dañar a las células, pero el cerebro no está indefenso: dispone de equipos de limpieza y células de apoyo. Este estudio explora cómo las neuronas y las células inmunitarias del cerebro comparten la carga de eliminar estos racimos, y cómo un tipo poco conocido de puente entre células, llamado nanotúnel (tunneling nanotube), se convierte en una autopista para mover material tóxico fuera de neuronas en apuros y hacia microglía más resistentes.
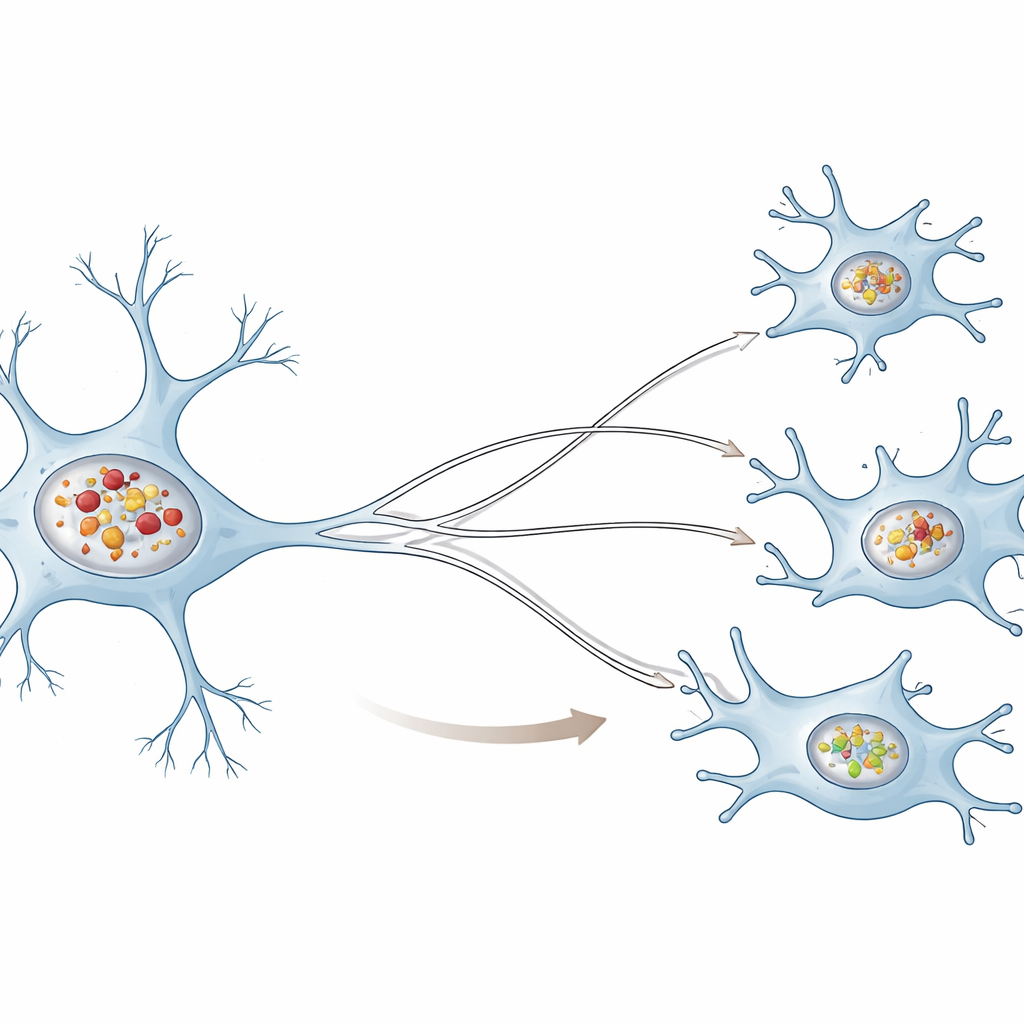
Dos equipos de limpieza muy distintos
Los autores compararon células humanas de tipo neuronal con microglía humana, las células inmunitarias residentes del cerebro, y expusieron ambos tipos a fibrillas de alfa‑sinucleína preformadas, una versión de laboratorio de los racimos dañinos observados en la enfermedad. En ambos tipos celulares, los racimos entrantes fueron captados y enviados a pequeños compartimentos de reciclaje llamados lisosomas. Sin embargo, las neuronas acumularon muchos más racimos dentro de sus lisosomas que la microglía. Con el tiempo, los lisosomas neuronales se volvieron menos ácidos y menos capaces de degradar una proteína de prueba, lo que muestra que su función central de reciclaje estaba fallando. Los lisosomas de la microglía, en contraste, conservaron en gran medida su acidez y capacidad de degradación incluso cuando contenían alfa‑sinucleína.
Cuando el reciclaje falla, el daño se propaga
Los lisosomas dañados pueden filtrarse y romperse. Usando marcadores de roturas de membrana y proteínas de reparación, los investigadores encontraron que las neuronas sufrieron mucho más daño lisosomal que la microglía tras la exposición a alfa‑sinucleína. Los lisosomas afectados en neuronas perdieron movilidad y formaron cúmulos, otra señal de disfunción. La microglía respondió de forma diferente: activó un proceso llamado lisofagia, una eliminación selectiva de lisosomas dañados, y al mismo tiempo aumentó la formación de nuevos lisosomas. Una proteína maestra que controla programas génicos de lisosomas y limpieza se trasladó al núcleo en ambos tipos celulares, pero solo en la microglía los genes aguas abajo se activaron de forma robusta. Esta asimetría significa que las neuronas tienen dificultades para restaurar su sistema de reciclaje, mientras que la microglía puede renovarlo.
Autofagia: atascada en neuronas, potenciada en microglía
Los racimos de proteínas normalmente se manejan mediante la autofagia, una vía que envuelve material no deseado y lo entrega a los lisosomas. El equipo midió el “flujo” de autofagia y encontró que la alfa‑sinucleína bloqueaba en gran medida este flujo en las neuronas pero no en la microglía. Las neuronas expuestas a racimos mostraron acumulación de una proteína adaptadora de carga (p62) sin aumento adicional cuando se bloqueó químicamente el paso final de la vía, lo que es consistente con una cinta transportadora detenida. La microglía, por el contrario, produjo más p62 y mostró un fuerte aumento cuando se bloqueó el paso final, lo que indica una vía aún activa e incluso regulada al alza. La microscopía reveló muchos más sitios en la microglía donde alfa‑sinucleína, marcadores de autofagia y lisosomas convergían, lo que sugiere que la microglía es mucho mejor identificando y dirigiendo los racimos hacia la degradación.
Autopistas de nanotúneles para carga tóxica
¿Qué ocurre cuando las neuronas no pueden seguir el ritmo de la basura? El estudio muestra que transfieren el problema a la microglía. Cuando la autofagia en neuronas cargadas de alfa‑sinucleína se inhibió químicamente, se transfirieron más racimos a microglía vecinas, y cuando la autofagia se estimuló, la transferencia disminuyó. Estos intercambios no dependieron del material liberado al medio de cultivo, sino de conexiones directas entre células. Los autores se centraron en los nanotúneles—puentes delgados basados en actina entre células—y encontraron que bloquear la autofagia en neuronas o microglía aumentaba tanto el número de estas conexiones como la cantidad de carga general que circulaba por ellas. Incluso cuando la microglía actuaba como donante en lugar de receptor, deteriorar su autofagia aumentaba la transferencia a neuronas, lo que sugiere que una limpieza propia defectuosa es una señal que anima a las células a conectarse y pasar agregados.
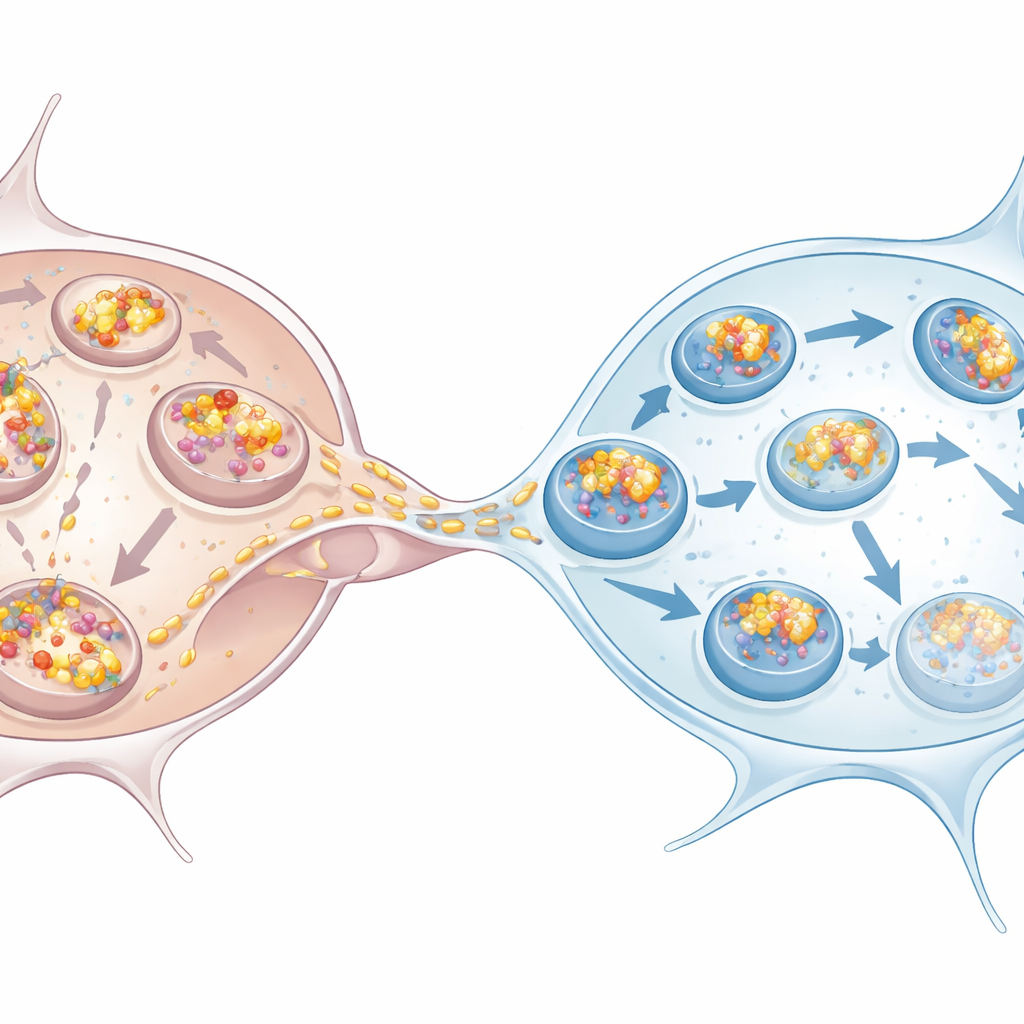
La microglía responde al reto
El trabajo también examinó neuronas dopaminérgicas derivadas de células madre humanas y microglía, que se parecen más a las células afectadas en la enfermedad de Parkinson. Surgió el mismo patrón: las neuronas acumularon más alfa‑sinucleína, mostraron signos de autofagia deteriorada y dependieron de la microglía para hacerse cargo de la eliminación. La microglía cultivada junto a neuronas sobrecargadas, o incluso simplemente expuesta a su medio condicionado, aumentó su propia autofagia. Una vez que recibieron alfa‑sinucleína vía nanotúneles, una gran fracción de los racimos entrantes terminó en estructuras marcadas por p62, consistente con una ruta hacia la degradación. El cocultivo de neuronas con microglía redujo el número y la carga global de racimos dentro de las neuronas, confirmando que la microglía actúa como sumideros eficaces para los agregados tóxicos.
Qué significa esto para el Parkinson y más allá
Para un público general, el mensaje principal es que no todas las células cerebrales están igualmente equipadas para lidiar con los desechos proteicos. Las neuronas, especialmente las vulnerables en la enfermedad de Parkinson, tienen sistemas de reciclaje frágiles que pueden verse desbordados por racimos de alfa‑sinucleína. La microglía, en contraste, es limpiadora más robusta y puede ayudar a rescatar a las neuronas al absorber y degradar sus agregados excedentes a través de pequeños puentes nanotubulares. Pero esta ayuda tiene un coste: el mismo proceso puede también facilitar la propagación de proteínas relacionadas con la enfermedad por el cerebro. Terapias que restauren la autofagia neuronal o ajusten la limpieza microglial podrían no solo reducir la carga tóxica dentro de células individuales, sino también ralentizar la propagación de agregados proteicos dañinos de célula a célula.
Cita: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Palabras clave: Enfermedad de Parkinson, alfa-sinucleína, microglía, autofagia</keyword'autofagia'> <keyword>nanotúneles