Clear Sky Science · nl
Verstoorde verwijdering van $$\alpha$$-synucleïne-aggregaten in neuronale cellen bevordert hun verspreiding naar microglia via tunnelingnanobuisjes
Waarom kleine eiwitklontertjes belangrijk zijn voor de gezondheid van de hersenen
De ziekte van Parkinson en verwante aandoeningen worden gekenmerkt door de langzame ophoping van klompjes van een eiwit genaamd alpha-synucleïne in hersencellen. Deze klonten kunnen cellen beschadigen, maar de hersenen staan niet hulpeloos: ze hebben eigen opruimteams en ondersteunende cellen. Deze studie onderzoekt hoe zenuwcellen en immuuncellen van de hersenen samen de last van het opruimen van deze klonten dragen, en hoe een weinig bekend type cel-tot-celbrug, tunnelingnanobuisjes genoemd, een snelweg wordt voor het verplaatsen van toxisch materiaal uit worstelende neuronen naar veerkrachtigere microglia.
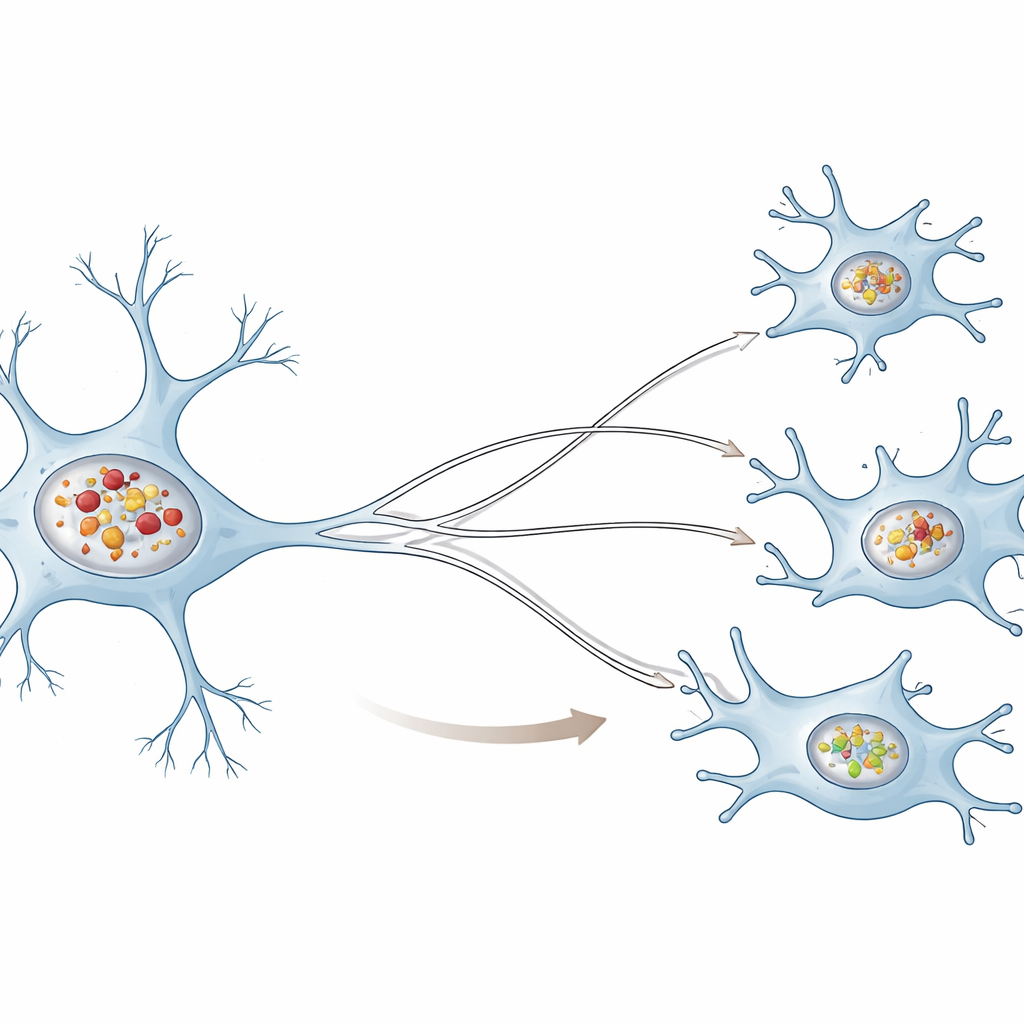
Twee heel verschillende opruimploegen
De auteurs vergeleken mensachtige neuronale cellen met menselijke microglia, de residentiële immuuncellen van de hersenen, en stelden beide bloot aan voorafgevormde alpha-synucleïne-fibrillen, een laboratoriumversie van de schadelijke klonten die in de ziekte worden gezien. In beide celtypen werden de binnenkomende klonten opgenomen en naar kleine recyclingcompartimenten gestuurd die lysosomen worden genoemd. Neuronen daarentegen stapelden veel meer klonten in hun lysosomen op dan microglia. In de loop van de tijd werden neuronale lysosomen minder zuur en minder goed in staat een test-eiwit af te breken, wat aangeeft dat hun kernfunctie voor recycling haperde. Microgliale lysosomen behielden daarentegen grotendeels hun zuurtegraad en afbraakcapaciteit, zelfs wanneer ze alpha-synucleïne bevatten.
Wanneer recycling faalt, verspreidt schade zich
Beschadigde lysosomen kunnen lekken en scheuren. Met behulp van markers voor membraanbreuken en reparatie-eiwitten vonden de onderzoekers dat neuronen veel meer lysosomale schade ondervonden dan microglia na blootstelling aan alpha-synucleïne. De aangedane lysosomen in neuronen verloren mobiliteit en clusteerden, een ander teken van disfunctie. Microglia reageerden anders: zij schakelden een proces in dat lysophagie wordt genoemd, een gerichte verwijdering van beschadigde lysosomen, en stimuleerden tegelijkertijd de aanmaak van nieuwe lysosomen. Een centrale controle-eiwit dat lysosoom- en opruimgenprogramma’s aanstuurt verplaatste zich naar de kern in beide celtypen, maar alleen in microglia schakelden de downstream-genen krachtig aan. Deze asymmetrie betekent dat neuronen moeite hebben hun recyclingsysteem te herstellen, terwijl microglia dat wél kunnen vernieuwen.
Autofagie: verstopt in neuronen, versterkt in microglia
Eiwitklonten worden normaal verwerkt via autofagie, een route die ongewenst materiaal omsluit en afleveren aan lysosomen. Het team meette de autofagie-„flux” en vond dat alpha-synucleïne deze stroom grotendeels blokkeerde in neuronen maar niet in microglia. Neuronen die aan klonten waren blootgesteld toonden een ophoping van een lading-adaptoreiwit (p62) zonder verdere toename wanneer de laatste stap van de route chemisch werd geblokkeerd, wat consistent is met een vastgelopen lopende band. Microglia maakten daarentegen meer p62 aan en lieten een sterke stijging zien wanneer de laatste stap werd geblokkeerd, wat wijst op een nog steeds lopende, zelfs opgevoerde route. Microscopen toonden veel meer plekken in microglia waar alpha-synucleïne, autofagiemarkers en lysosomen samenkwamen, wat suggereert dat microglia veel beter zijn in het herkennen en routeren van klonten naar afbraak.
Nanobuis‑snelwegen voor toxische lading
Wat gebeurt er als neuronen de rommel niet kunnen bijbenen? De studie toont aan dat zij het probleem doorschuiven naar microglia. Wanneer autofagie in alpha-synucleïne-beladen neuronen chemisch werd geremd, werden meer klonten overgedragen aan naburige microglia, en wanneer autofagie werd gestimuleerd, nam de overdracht af. Deze uitwisselingen waren niet afhankelijk van materiaal dat in het kweekmedium werd vrijgegeven, maar wezen juist op directe cel‑tot‑celverbindingen. De auteurs concentreerden zich op tunnelingnanobuisjes—dunne, actine-gebaseerde bruggen tussen cellen—en vonden dat het blokkeren van autofagie in zowel neuronen als microglia zowel het aantal van deze verbindingen als de hoeveelheid algemene lading die erdoorheen bewoog verhoogde. Zelfs wanneer microglia donor in plaats van ontvanger waren, verhoogde het aantasten van hun autofagie de overdracht naar neuronen, wat suggereert dat slechte zelfopruiming een signaal is dat cellen aanzet zich te verbinden en aggregaten door te geven.
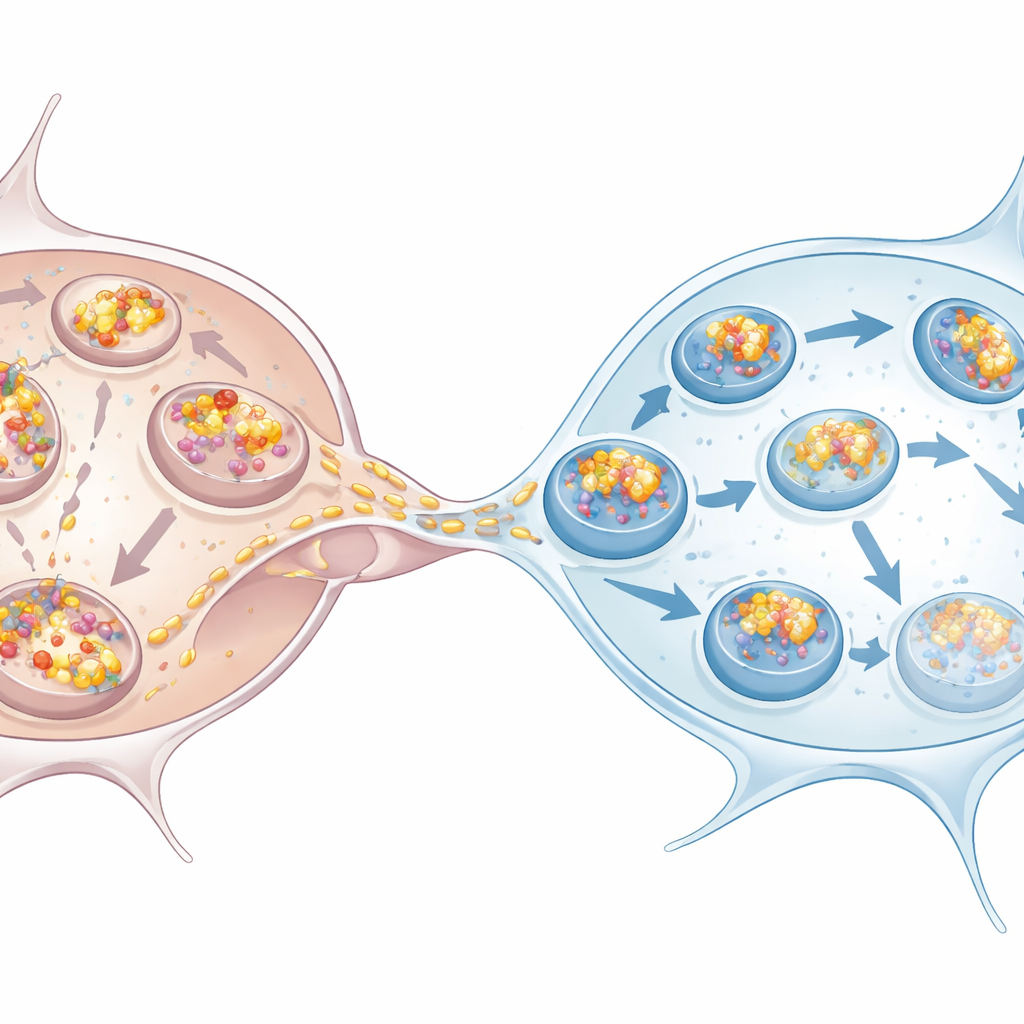
Microglia nemen de uitdaging aan
Het werk onderzocht ook uit menselijke stamcellen afgeleide dopaminerge neuronen en microglia, die meer lijken op de cellen die bij de ziekte van Parkinson worden aangetast. Zelfde patroon verscheen: neuronen stapelden meer alpha-synucleïne op, vertoonden tekenen van aangetaste autofagie en waren afhankelijk van microglia om de verwijdering over te nemen. Microglia die naast overbelaste neuronen groeiden, of zelfs alleen werden blootgesteld aan hun geconditioneerde medium, verhoogden hun eigen autofagie. Zodra zij alpha-synucleïne via nanobuisjes ontvingen, belandde een groot deel van de binnenkomende klonten in p62-gemarkeerde structuren, consistent met een route richting degradatie. Co-teelt van neuronen met microglia verminderde het aantal en de totale lading van klonten in neuronen, wat bevestigt dat microglia als effectieve putten voor toxische aggregaten fungeren.
Wat dit betekent voor Parkinson en verder
Voor de niet‑specialist is de belangrijkste boodschap dat niet alle hersencellen even goed uitgerust zijn om met eiwitafval om te gaan. Neuronen, vooral die kwetsbaar bij de ziekte van Parkinson, hebben fragiele recyclingsystemen die overweldigd kunnen raken door alpha-synucleïne-klonten. Microglia zijn daarentegen robuustere schoonmakers en kunnen neuronen helpen door hun overtollige aggregaten op te nemen en af te breken via kleine nanobuisbruggen. Maar deze hulp heeft een keerzijde: hetzelfde proces kan ook bijdragen aan de verspreiding van ziekteveroorzakende eiwitten door de hersenen. Therapieën die de neuronaire autofagie herstellen of de microgliale opruiming verfijnen, zouden niet alleen de toxische last in individuele cellen kunnen verlagen maar ook de cel‑tot‑celpropagatie van schadelijke eiwitklonten kunnen vertragen.
Bronvermelding: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
Trefwoorden: Ziekte van Parkinson, alpha-synucleïne, microglia, autofagie, tunnelingnanobuisjes