Clear Sky Science · he
ניקוי מצברי $$\alpha$$-סינוקלאין פגום בתאי עצב דוחף את הפצתם לתאי מיקרוגליה דרך תעלות‑ננו
מדוע גושי חלבון זעירים חשובים לבריאות המוח
מחלת פרקינסון והפרעות קשורות מאופיינות בהצטברות איטית של גושים של חלבון שנקרא אלפא‑סינוקלאין בתוך תאי המוח. גושים אלה עלולים לגרום נזק לתאים, אך המוח אינו חסר אמצעי הגנה: יש לו צוותי ניקיון ותאי תמיכה משלו. המחקר חוקר כיצד תאי עצב ותאי חיסון מוחיים חולקים את העומס של ניקוי הגושים הללו, וכיצד סוג מעט ידוע של גשר תא‑לתא, הנקרא תעלת‑ננו (tunneling nanotube), הופך לנתיב להוצאת חומר רעיל מתוך נוירונים מתקשים ולתוך מיקרוגליה עמידים יותר.
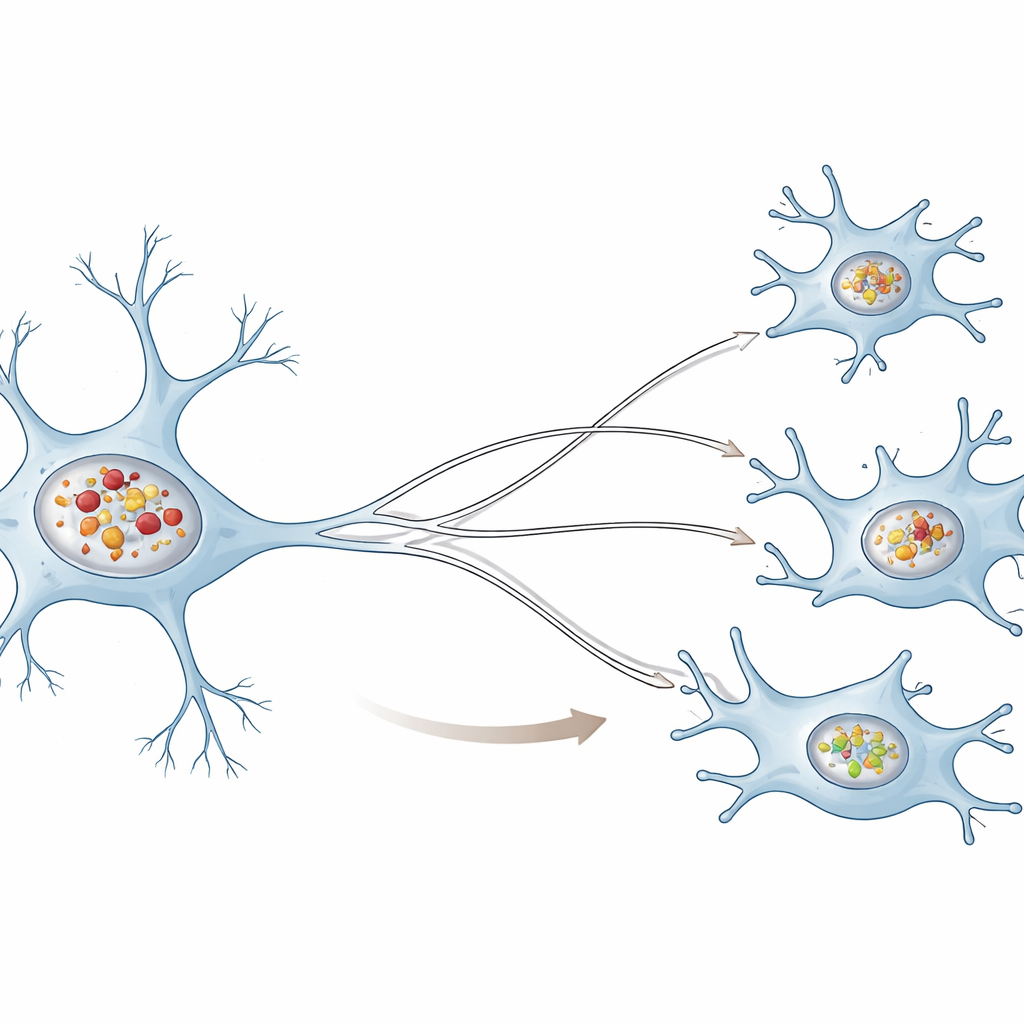
שני צוותי ניקיון שונים בתכלית
המחברים השוו תאי דמויי‑נוירון אנושיים עם תאי מיקרוגליה אנושיים, תאי החיסון התושבים של המוח, וחשפו את שניהם לסיבים של אלפא‑סינוקלאין שהוכנו מראש—גרסה מעבדתית של הגושים המזיקים שנמצאים במחלה. בשני סוגי התאים הבליטות הנכנסות נבלעו ונשלחו למחלקות מיחזור קטנות הנקראות ליזוזומים. עם זאת, הנוירונים הצטברו בהרבה יותר גושים בתוך הליזוזומים שלהם מאשר המיקרוגליה. עם הזמן הפכו הליזוזומים הנוירונליים לפחות חומציים ופחות מסוגלים לפרק חלבון‑מבחן, מה שמעיד על שקיעת תפקודיהם המרכזיים של מיחזור. לעומת זאת, ליזוזומי המיקרוגליה שמרו במידה רבה על החומציות ועל יכולת הפרוק גם כאשר הם הכילו אלפא‑סינוקלאין.
כשמיחזור נכשל — הנזק מתפשט
ליזוזומים פגועים עלולים לדלוף ולהיקרע. באמצעות סמנים לשבירת ממברנות וחלבוני תיקון, החוקרים מצאו כי הנוירונים חוו הרבה יותר פגיעת ליזוזום מאשר המיקרוגליה לאחר חשיפה לאלפא‑סינוקלאין. הליזוזומים המושפעים בנוירונים איבדו ניידות והצטברו באשכולות, עוד סימן לתפקוד לקוי. המיקרוגליה הגיבה אחרת: הן הפעילו תהליך שנקרא ליזופגיה (lysophagy), הסרה ממוקדת של ליזוזומים פגועים, ובמקביל הגבירו יצירה של ליזוזומים חדשים. חלבון בקרה ראשי שמפעיל תוכניות גנטיות של ליזוזום וניקיון עבר אל הגרעין בשני סוגי התאים, אך רק במיקרוגליה הגנים התחתונים הופעלו בעוצמה. אי‑סימטריה זו משמעותה שהנוירונים מתקשים לשקם את מערכת המיחזור שלהם, בעוד המיקרוגליה מסוגלת לחדש את שלה.
אוטופאגיה: סתומה בניורונים, מחוזקת במיקרוגליה
גושי חלבון מטופלים בדרך כלל על‑ידי אוטופאגיה, מסלול שעוטף חומר לא רצוי ומוביל אותו לליזוזומים. הצוות מדד את "הזרימה" של האוטופאגיה ומצא שאלפא‑סינוקלאין חסם ברובו את הזרימה הזו בנוירונים אך לא במיקרוגליה. נוירונים שנחשפו לגושים הראו הצטברות של חלבון‑מוביל (p62) ללא עלייה נוספת כאשר השלב הסופי של המסלול נחסם כימית, תואם למסוע תקוע. לעומת זאת, המיקרוגליה ייצרו יותר p62 והראו עלייה חזקה כאשר השלב הסופי נחסם, מה שמרמז שהמסלול עדיין פועל ואף מועצם. מיקרוסקופיה גילתה הרבה יותר אתרים במיקרוגליה שבהם אלפא‑סינוקלאין, סמני אוטופאגיה וליזוזומים נפגשו, דבר שמרמז שמיקרוגליה טובה בהרבה בזיהוי והכוונה של גושים להשמדה.
כבישים של תעלות‑ננו למטען רעיל
מה קורה כשנוירונים אינם מצליחים לעמוד בקצב הפסולת? המחקר מראה שהם מעבירים את הבעיה למיקרוגליה. כאשר האוטופאגיה לנוירונים שטופי אלפא‑סינוקלאין הועמדה בעיכוב כימי, יותר גושים הועברו למיקרוגליה שכנות, וכאשר האוטופאגיה גולתה, ההעברה ירדה. החילופים הללו לא תלויים בחומר שדהר מהמדיה התרבושתית, אלא בהתחברויות ישירות תא‑לתא. המחברים התמקדו בתעלות‑ננו—גשרים דקים מבוססי אקטין בין תאים—ומצאו שחסימת האוטופאגיה אלא באחד משני סוגי התאים הגדילה הן את מספר הקשרים האלו והן את כמות המטען הכללי הנע דרכן. גם כאשר המיקרוגליה היו התורמות ולא המקבלות, פגיעה באוטופאגי שלהן הגבירו העברה לנוירונים, מה שמרמז שניקיון עצמי לקוי הוא אות המעודד תאים להתחבר ולהעביר גושים.
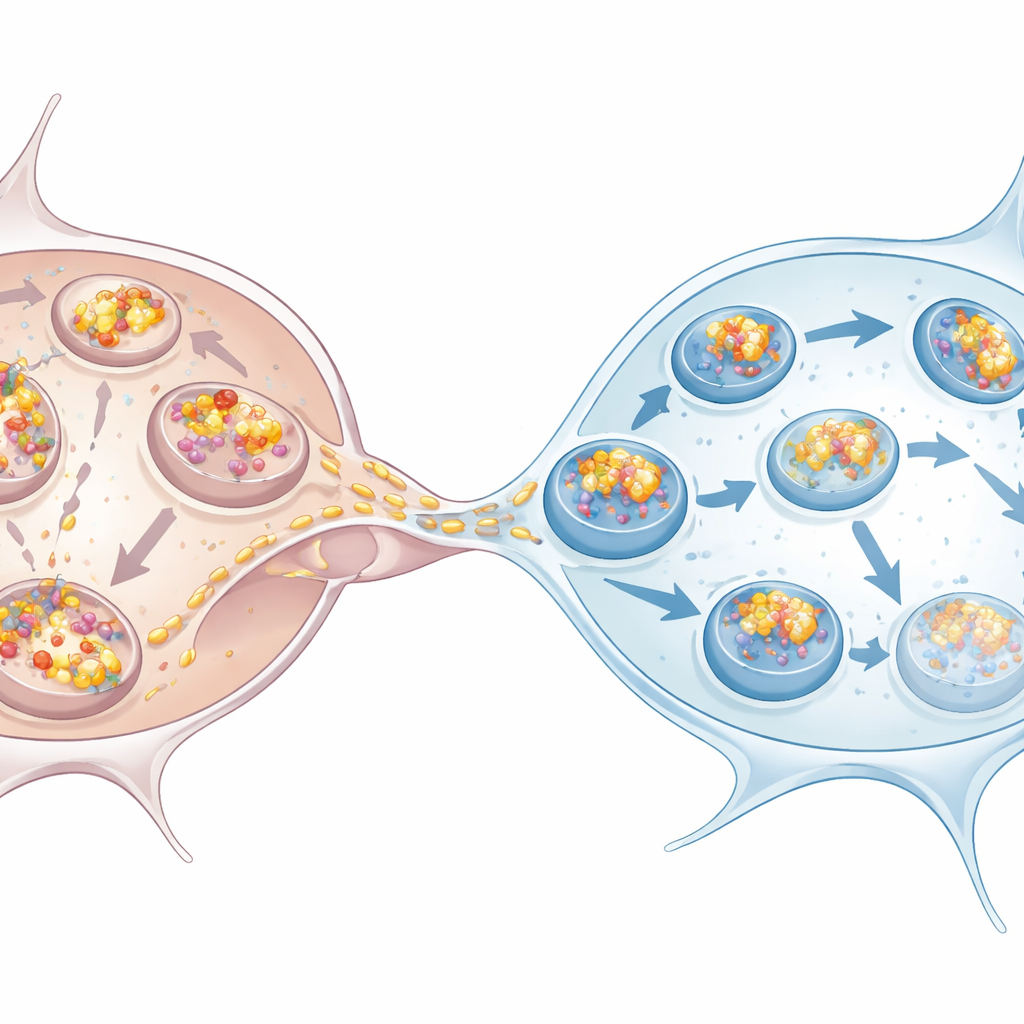
מיקרוגליה עונה לאתגר
העבודה בדקה גם נוירונים דופמינרגיים ומיקרוגליה שמקורם בתאי גזע אנושיים, הדומים יותר לתאים המעורבים במחלת פרקינסון. אותו תבנית הופיעה: הנוירונים הצטברו ביותר אלפא‑סינוקלאין, הראו סימנים של אוטופאגיה לקויה והסתמכו על מיקרוגליה כדי overtake את מפעל ההשלכה. מיקרוגליה שגודלו לצד נוירונים עמוסים, או אפילו שנחשפו למדייתם המותנית בלבד, הגבירו את האוטופאגיה שלהם. ברגע שקיבלו אלפא‑סינוקלאין דרך תעלות‑ננו, חלק גדול מהגושים הנכנסים מצא את דרכו למבנים המסומנים ב‑p62, תואם למסלול לעבר פירוק. תרבית משותפת של נוירונים עם מיקרוגליה הקטינה את מספר ועומס הגושים בתוך הנוירונים, ואישרה שמיקרוגליה פועלות כבולעות יעילות של מצברי הרעל.
מה משמעות הדבר לפרקינסון ולתחומים נוספים
ללא מומחיות מיוחדת, המסר המרכזי הוא שלא כל תאי המוח מצוידים באותה מידה להתמודד עם פסולת חלבונית. נוירונים, ובמיוחד אלה הפגיעים בפרקינסון, בעלי מערכות מיחזור שבירות שעלולות להיות מוצפות על‑ידי גושי אלפא‑סינוקלאין. לעומת זאת, המיקרוגליה הן מנקות חסונות יותר ויכולות לעזור להציל נוירונים על ידי לקיחת והפרקת עודפי הגושים שלהם באמצעות גשרים זעירים של תעלות‑ננו. אך עזרה זו באה במחיר: אותו מנגנון עלול גם לסייע בהתפרשות חלבונים הקשורים למחלה ברחבי המוח. טיפולים המשקמים אוטופאגיה בנוירונים או מכוונים בדייקנות לניקיון המיקרוגליה עשויים לא רק להוריד את העומס הרעיל בתאים בודדים אלא גם להאט את הפצת הגושים הפוגעניים מתא לתא.
ציטוט: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
מילות מפתח: מחלת פרקינסון, אלפא-סינוקלאין, מיקרוגליה, אוטופאגיה, תעלות‑ננו (tunneling nanotubes)