Clear Sky Science · ja
ニューロン細胞における$$\alpha$$-シヌクレイン凝集体の除去障害がトンネリングナノチューブを介してミクログリアへの拡散を駆動する
脳の健康にとって小さなタンパク質塊が重要な理由
パーキンソン病や関連疾患では、アルファ‑シヌクレインと呼ばれるタンパク質の塊が脳細胞内に徐々に蓄積することが特徴です。これらの塊は細胞に損傷を与え得ますが、脳には独自の清掃機構や支援細胞が備わっています。本研究は、神経細胞と脳の免疫担当細胞であるミクログリアがこれらの塊の処理負担をどのように分担するか、またトンネリングナノチューブと呼ばれるあまり知られていない細胞間ブリッジが、苦境にあるニューロンから有害物質を移送する高速道路となる仕組みを調べています。
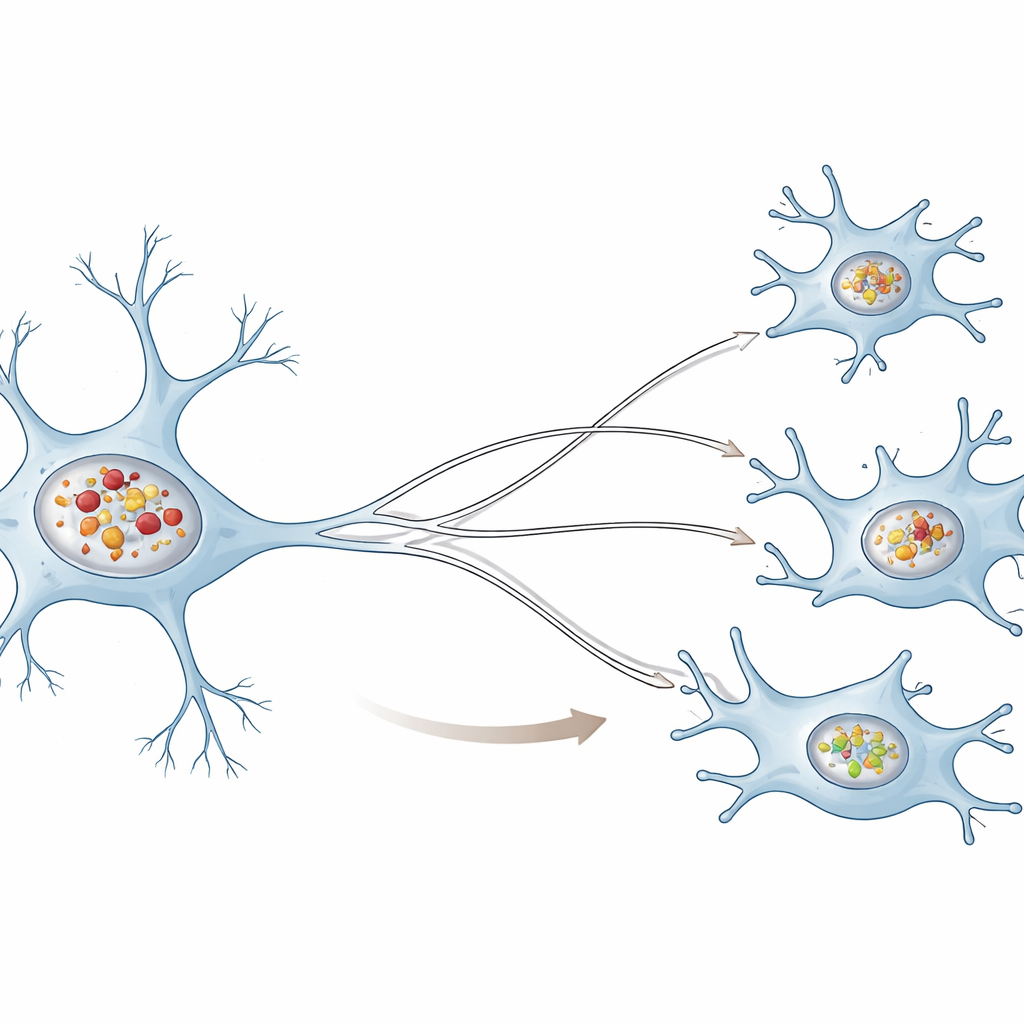
まったく異なる二つの清掃隊
著者らはヒトのニューロン様細胞と脳の常在免疫細胞であるヒトミクログリアを比較し、どちらにも事前に形成したアルファ‑シヌクレイン線維(疾患で見られる有害な塊の実験的な模倣)を曝露しました。両細胞種とも取り込んだ塊をリソソームと呼ばれる小さなリサイクルコンパートメントへ送っていましたが、ニューロンはミクログリアに比べてリソソーム内にはるかに多くの塊を蓄積しました。時間が経つとニューロンのリソソームは酸性度が低下し、試験用タンパク質の分解能も落ち、中心的なリサイクル機能が低下していることが示されました。一方でミクログリアのリソソームは、アルファ‑シヌクレインを含んでいても酸性度や分解能力を概ね保っていました。
リサイクルが破綻すると損傷が広がる
損傷したリソソームは漏出や破裂を起こすことがあります。膜破損や修復タンパク質のマーカーを用いると、アルファ‑シヌクレイン曝露後にニューロンの方がミクログリアよりもはるかに多くのリソソーム損傷を経験していることがわかりました。影響を受けたニューロンのリソソームは可動性を失い凝集するなど、別の機能障害の兆候も示しました。ミクログリアは異なる応答を示し、損傷したリソソームを標的的に除去するプロセスであるリソフォジーを活性化すると同時に、新しいリソソームの生成を促進しました。リソソームや清掃遺伝子プログラムを制御するマスタープロテインは両細胞種の核に移行しましたが、その下流の遺伝子が強く発現したのはミクログリアのみでした。この非対称性は、ニューロンがリサイクルシステムを回復するのに苦労する一方で、ミクログリアはそれを再生できることを意味します。
オートファジー:ニューロンでは渋滞、ミクログリアでは増強
タンパク質の塊は通常オートファジーという経路で扱われ、不要物を包んでリソソームに届けます。研究チームはオートファジーの「フラックス」を測定し、アルファ‑シヌクレインが主にニューロンでこの流れを遮断する一方、ミクログリアではそうではないことを見出しました。塊に曝露されたニューロンは貨物アダプター蛋白質(p62)が蓄積し、経路の最終段階を化学的に阻害してもさらなる増加を示さず、コンベアが停止していることと一致しました。対照的にミクログリアはp62をより多く産生し、最終段階を阻害すると顕著に増加しており、経路がまだ稼働しているかむしろ上方制御されていることを示しました。顕微鏡観察では、ミクログリア内にアルファ‑シヌクレイン、オートファジーマーカー、リソソームが集合する部位がはるかに多く見られ、ミクログリアが塊を認識して破壊へとルーティングする能力に優れていることが示唆されました。
有害物質のナノチューブ高速道路
ニューロンがゴミ処理に追いつけない場合、何が起きるのでしょうか。本研究は、ニューロンがその問題をミクログリアに渡すことを示しています。アルファ‑シヌクレインを抱えたニューロンのオートファジーを化学的に阻害すると、近隣のミクログリアへ移される塊が増え、オートファジーを刺激すると移動は減少しました。これらの交換は培地中に放出された物質に依存しておらず、むしろ直接の細胞間接続に依存していました。著者らはトンネリングナノチューブ—細胞間を結ぶ細いアクチン依存性の橋—に着目し、ニューロンまたはミクログリアでオートファジーを阻害するとこれらの接続の数と一般的な貨物の通過量が増加することを見出しました。ミクログリアが供与者で受容者でない場合でも、彼らのオートファジーを障害するとニューロンへの移動が増え、自己清掃の障害が細胞同士を結び付け塊を受け渡すシグナルになることが示唆されます。
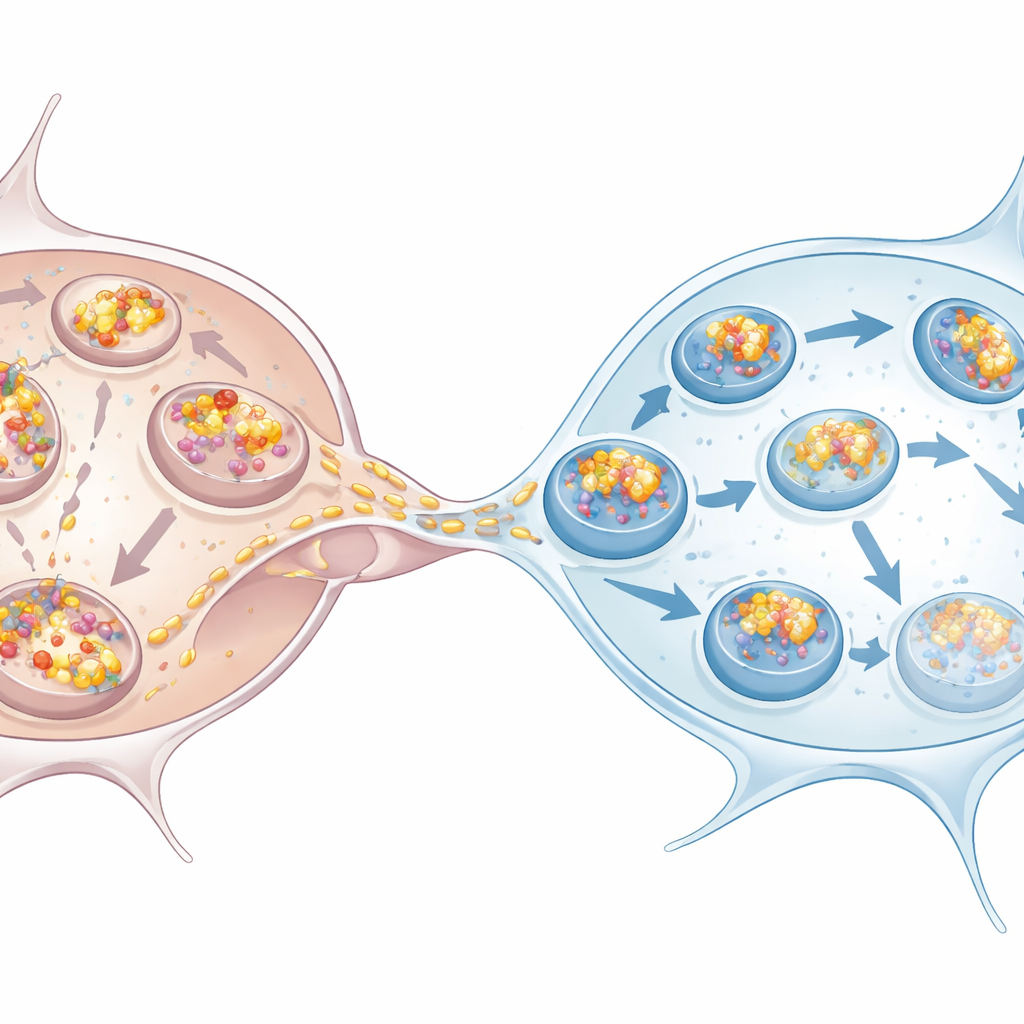
ミクログリアが課題に立ち向かう
研究はまた、パーキンソン病で影響を受ける細胞により近いヒト幹細胞由来のドーパミン作動性ニューロンとミクログリアも調べました。そこでも同じパターンが現れました:ニューロンはより多くのアルファ‑シヌクレインを蓄積し、オートファジー障害の兆候を示し、過剰な凝集体の処理をミクログリアに依存していました。過負荷のニューロンと共培養された、あるいはその条件培養液に曝されたミクログリアは、自身のオートファジーを高めました。トンネリングナノチューブを介してアルファ‑シヌクレインを受け取ると、到着した塊の大部分がp62で標識された構造に入ることが多く、分解に向かう経路と一致しました。ニューロンをミクログリアと共培養するとニューロン内の塊の数と総負荷が減少し、ミクログリアが有害な凝集体の効果的な受け皿として機能することが確認されました。
パーキンソン病とそれを越えて意味すること
専門外の読者にとっての主なメッセージは、すべての脳細胞がタンパク質廃棄物の処理能力において同じではないということです。特にパーキンソン病で脆弱なニューロンはリサイクル機構が弱く、アルファ‑シヌクレインの塊に圧倒されやすい。一方でミクログリアはより頑健な洗浄者であり、小さなナノチューブ橋を介して過剰な凝集体を取り込み分解することでニューロンを救う手助けができます。しかしその助けは代償を伴う可能性があり、同じプロセスが病的なタンパク質を脳内に拡散させるのを助けることもあります。ニューロンのオートファジーを回復させる治療やミクログリアの清掃機能を精密に調整する治療は、個々の細胞内の毒性負荷を下げるだけでなく、有害なタンパク質塊の細胞間伝播を遅らせる可能性があります。
引用: Chakraborty, R., Palese, F., Samella, P. et al. Impaired \(\alpha\)-Synuclein aggregate clearance in neuronal cells drive their spread to microglia through tunneling nanotubes. Nat Commun 17, 3832 (2026). https://doi.org/10.1038/s41467-026-69930-y
キーワード: パーキンソン病, アルファシヌクレイン, ミクログリア, オートファジー, トンネリングナノチューブ