Clear Sky Science · tr
H pilin siklizasyonu ve pilus biyogenezi hoşgörülüdür ancak elektrostatik bozulmalar konjugasyon verimini bozar
Neden küçük bakteriyel kablolar önemlidir
Bakteriler sürekli olarak DNA değiş tokuşu yapar; bu sayede zararsız mikroplar tedavisi zor tehditlere dönüşebilen antibiyotik direnci gibi özellikler paylaşılır. Bu değişimin başlıca yollarından biri konjugasyondur: bir verici bakteri, pilus adı verilen uzun, ince yüzey kablosunu kullanarak bir komşuya bağlanır ve plazmid DNA’sını aktarır. Bu çalışma, sonuçları büyük etkiler doğurabilecek beklenmedik derecede ince bir soruyu inceliyor: pilusun yüzeyindeki atomların ve alıcının dış zarındaki lipitlerin tam olarak hangi özellikleri DNA aktarımının başarılı olup olmayacağını kontrol ediyor?
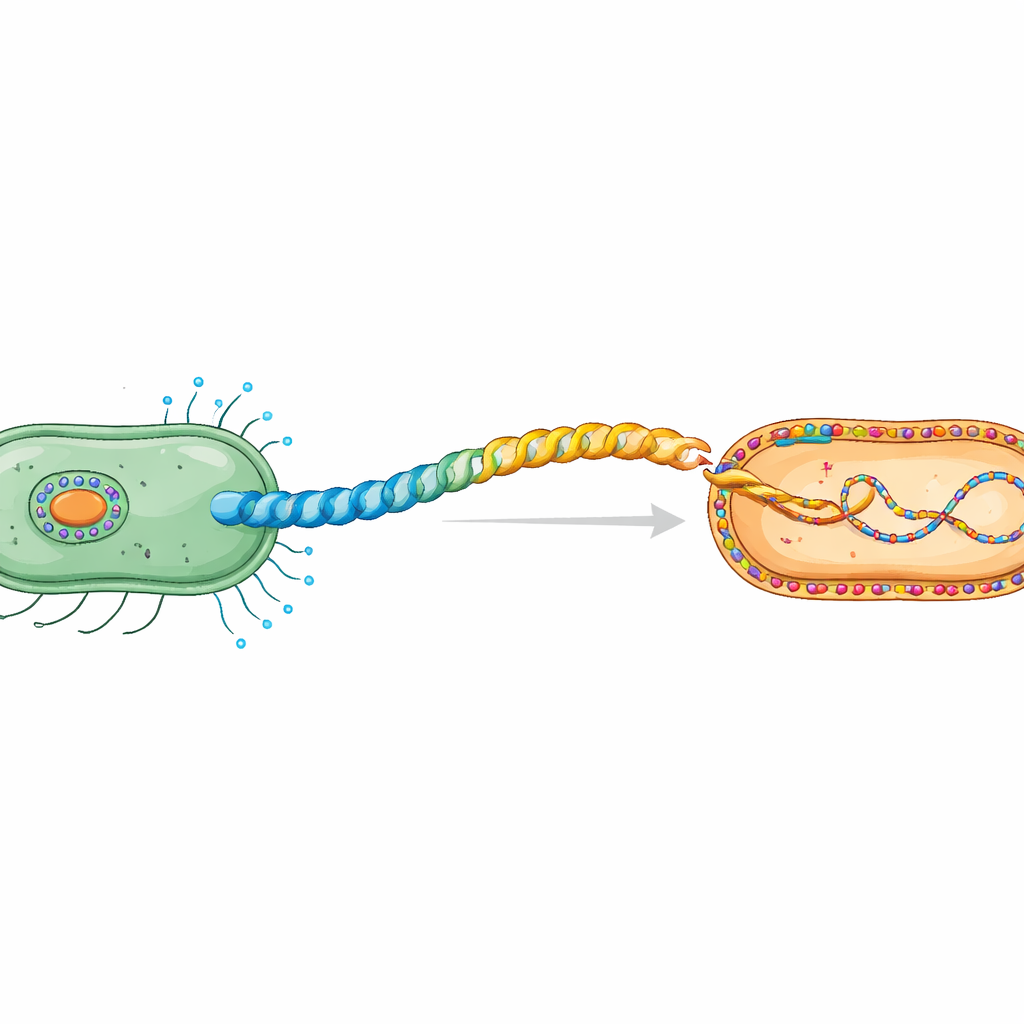
Bakteriyel hücreler arasındaki gizli tokalaşma
Konjugasyon sırasında plazmid DNA’sı temas bağımlı bir süreçle verici hücreden alıcıya taşınır. Verici hücreler, tekrarlayan pilin protein birimlerinden oluşan, esnek bir helikal tüp olan özel bir pilus inşa eder. Çalışma, antibiyotik direncini yaymasıyla bilinen IncHI1 plazmid R27 tarafından kodlanan H‑pilusa odaklanıyor. Daha önceki kriyo‑elektron mikroskobu, onun pilininin, TrhA’nın alışılmadık olduğunu ortaya koymuştu: zincir uçları açık bir yapı yerine, proteinin başı (Gly1) ile sonu (Asp69) birbirine bağlanarak “bir halka içine bağlanmıştır”. Bu siklizasyon, DNA aktarabilen fonksiyonel bir pilus oluşturmak için esastır.
Oldukça korunmuş protein uçları, şaşırtıcı derecede tolere edici kimya
Büyük bir plazmid veritabanını tarayarak yazarlar, ilişkili plazmidlerden 147 TrhA dizisini incelediler. Birçok konum değişken olmasına rağmen, halkayı kapatan iki kalıntı—Gly1 ve Asp69—kesinlikle korunmuştu; bu durum bunları korumaya yönelik güçlü evrimsel baskıya işaret ediyor. Ekip daha sonra laboratuvarda bu iki pozisyonu sistematik olarak değiştirdi ve birkaç mutant pilin oluşturdu. Yüksek çözünürlüklü kriyo‑EM, Asp69’daki oldukça farklı amino asitlerin (örneğin Asn, Ala, Gly veya Arg) bile TrhA’nın siklize olmasına ve vahşi tip ile yapısal olarak neredeyse ayırt edilemez piliiler oluşturmasına izin verdiğini gösterdi. Başka bir deyişle, halka oluşumu ve pilus inşasının kimyası şaşırtıcı derecede hoşgörülüdür.
Kablonun yükü bağlantıyı engellediğinde
Görünüşleri normal olmasına rağmen mutant piluslar, çeşitli Gram‑negatif alıcılarda yapılan konjugasyon testlerinde çok farklı davrandı. Asp69 nötr amino asitlerle (Asn, Ala, Gly) değiştirildiğinde plazmidler hâlâ E. coli ve Klebsiella pneumoniae içine iyi aktı. Bazı diğer türlerde ince eğilimler ortaya çıktı: genelde daha büyük yan zincirler küçük olanlara göre biraz daha yüksek aktarım verimini destekledi. Çok farklı bir tablo ise Asp69 veya Gly1 pozisyonları arginin ya da lizin gibi pozitif yüklü amino asitlerle değiştirildiğinde görüldü. Bu değişiklikler pilus dış yüzeyini negatiften güçlü bir pozitife çevirdi. Mutant piluslar hâlâ oluşsa da, normal alıcılara konjugasyon vahşi tipe göre bir milyona varan oranda düştü.
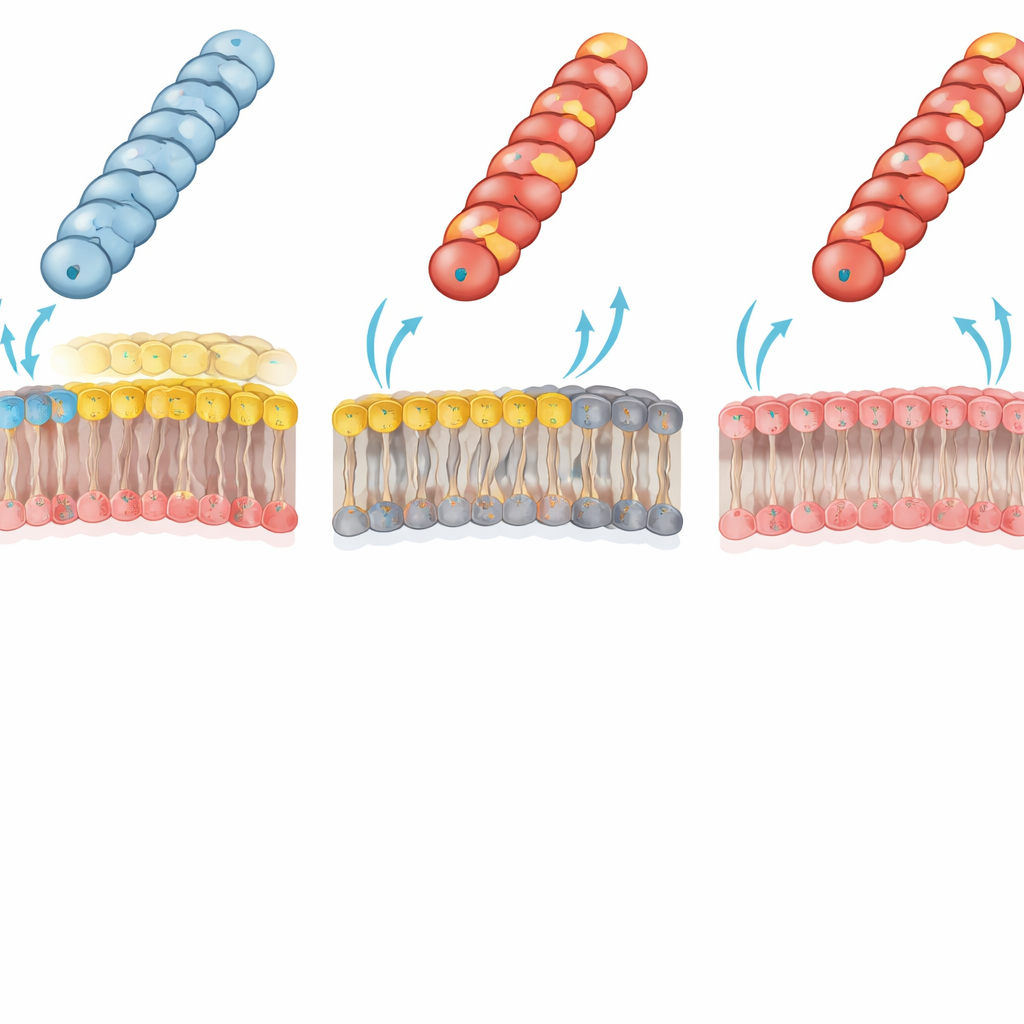
Hangi bakterinin DNA alabileceğini zar lipitleri belirler
Yazarlar bu dramatik başarısızlığı pilus ile alıcının dış zarı arasındaki elektrostatik çatışmaya bağladılar. Tipik Gram‑negatif bakterilerde dış zarın iç tabakası, hem pozitif hem negatif grup taşıyan başlıca bir zwitteryonik fosfolipit olan fosfatidiletanolamin (PE) içerir. Ekip, PE içermeyen özel olarak tasarlanmış bir E. coli suşu kullandı; bu suşta dış zarın iç tabakası bunun yerine tamamen negatif yüklü lipitlerden oluşuyordu. Bu PE‑eksik alıcıda, daha önce etkisizleşmiş pozitif yüklü piluslar (Gly1Lys, Asp69Lys veya Asp69Arg) artık plazmidleri neredeyse vahşi tip kadar verimli şekilde aktardı. Bu tersine dönüş, pozitif yüklü bir pilus yüzeyi ile PE açısından zengin zarlı arasındaki olumsuz yük–yük etkileşiminin normalde pilus ucunun DNA aktarımı için gerekli doğru temas geometrisini benimsemesini engellediği fikrini güçlü şekilde destekliyor.
Elektrostatik hassas ayarın antibiyotik direnci yayılımını nasıl şekillendirdiği
Birlikte ele alındığında sonuçlar belirgin bir işbölümünü ortaya koyuyor. Pilin zincirini kesip tekrar birleştirerek bir halka oluşturmak için gereken kimyasal mekanizma oldukça esnektir—birçok farklı uç kalıntısı hâlâ birleştirilip normal görünümlü bir pilus oluşturulabilir. Ancak başarılı konjugasyon, bu dışa dönük kalıntıların boyutu ve özellikle yükü konusunda son derece hassastır; çünkü bunlar, alıcının zar lipid ortamıyla eşleşmesi gereken pilus yüzey potansiyelini biçimlendirir. Bu elektrostatik “ayar”, doğada Gly1 ve Asp69’in neden bu kadar sıkı korunduğunu açıklamaya yardımcı olur. Ayrıca çevresel stres veya konak koşullarının yol açtığı zar lipit bileşimi değişikliklerinin, bakterilerin antibiyotik direnç genleri taşıyan plazmidleri ne kadar kolayca değiş tokuş ettiklerini modüle edebileceğini öne sürer. Özetle, bakteriyel “tokalaşmanın” her iki ortağı da gen paylaşımının faydaları ve riskleri arasında denge kurmak için yüzeylerini birlikte evrimleştirir.
Atıf: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Anahtar kelimeler: bakteriyel konjugasyon, antibiyotik direnci, pilus yapısı, zar lipitleri, elektrostatik etkileşimler