Clear Sky Science · he
הצלבת H pilin וביוגנזה של pilus הן פתייניות אך שיבושים אלקטרוסטטיים פוגעים ביעילות ההעברה
מדוע כבלים זעירים של חיידקים חשובים
חיידקים מחליפים באופן קבוע DNA, משתפים תכונות כמו עמידות לאנטיביוטיקה שיכולות להפוך מיקרובים תמימים לאיומים קשים לטיפול. מסלול עיקרי להחלפה זו הוא קונוגציה, שבה חיידק תורם משתמש בכבל דק וארוך על פני השטח שנקרא פילוס כדי להתחבר לשכן ולהעביר פלסמיד DNA. המחקר הזה שואל שאלה מפתיעה בעדינותה ובעלת השלכות גדולות: כיצד האטומים המדויקים על פני הפילוס וליפידים בממברנת המקבל קובעים אם העברת ה‑DNA תצליח או תיכשל?
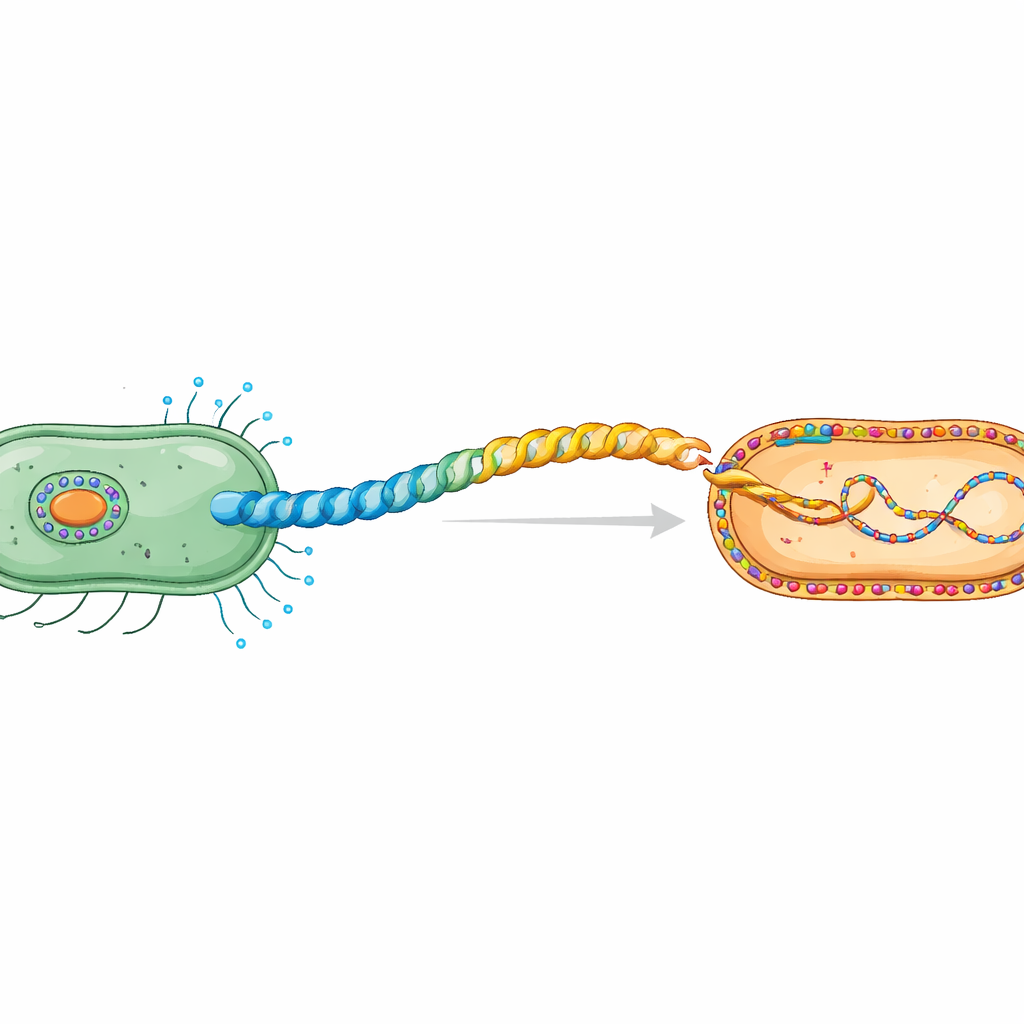
הלחיצה הסודית בין תאי חיידק
במהלך קונוגציה, פלסמיד DNA נוסע מתא תורם לתא מקבל בתהליך התלוי במגע. תאים תורמים בונים פילוס מיוחד, צינור ספירלי גמיש המורכב מיחידות חלבוניות חוזרות של פילין. העבודה מתמקדת ב‑H‑pilus המקודד על ידי הפלסמיד IncHI1 R27, משפחת פלסמידים הידועה בהפצת עמידות לאנטיביוטיקה. מיקרוסקופיה אלקטרונית קפיאית קודמת הראתה שהפילין שלו, TrhA, הוא יוצא דופן: במקום שרשרת בעלת קצוות פתוחים, החלבון "קשור לטבעת" על ידי חיבור ההתחלה שלו (Gly1) והסוף (Asp69). ציקליזציה זו חיונית ליצירת פילוס פונקציונלי המסוגל להעביר DNA.
קצוות חלבוניים שמורים מאוד, כימיה מפתיעה סלחנית
באמצעות כריית מאגר פלסמידים גדול, החוקרים בחנו 147 רצפי TrhA מפלסמידים קרובים. אף שעמדות רבות הראו שונות, שני החומצות שמסגרות את הטבעת — Gly1 ו‑Asp69 — היו שמורות ללא יוצא מן הכלל, מה שמרמז על לחץ אבולוציוני חזק לשמרן. הצוות שינה שיטתית שתי עמדות אלו במעבדה ויצר מספר מוטנטים של פילין. קרי‑EM ברזולוציה גבוהה הראה שגם חומצות אמינו שונות יחסית ב‑Asp69 (כגון Asn, Ala, Gly או Arg) עדיין אפשרו ל‑TrhA לעבור ציקליזציה ולהרכיב פילוסים שהיו למראית עין כמעט זהים לסוג הבר. במילים אחרות, הכימיה של יצירת הטבעת ובניית הפילוס הייתה מפתיעה פרומיסקואלית.
כאשר מטען על הכבל חוסם את החיבור
למרות המראה התקין שלהם, הפילוסים המוטנטיים התנהגו בצורה שונה מאוד במבחני קונוגציה עם מגוון מקבלי גרם‑שליליים. כאשר Asp69 הוחלפה בחומצות ניטרליות (Asn, Ala, Gly), הפלסמידים עודדו להעתק היטב ל‑E. coli ו‑Klebsiella pneumoniae. במינים אחרים התגלו מגמות עדינות: שרשראות צד גדולות בדרך כלל תמכו ביעילות העברה מעט גבוהה יותר מאשר קטנות יותר. תמונה שונה לחלוטין הופיעה כאשר Asp69 או Gly1 הוחלפו בחומצות חיוביות כמו ארגינין או ליזין. שינויים אלו הפכו את החזית החיצונית של הפילוס ממטען שלילי לחזק חיובי. אף שהפילוסים המוטנטיים עדיין נוצרו, הקונוגציה אל מקבלים תקינים צנחה בעד מיליון פעמים בהשוואה לפילוס מסוג הבר.
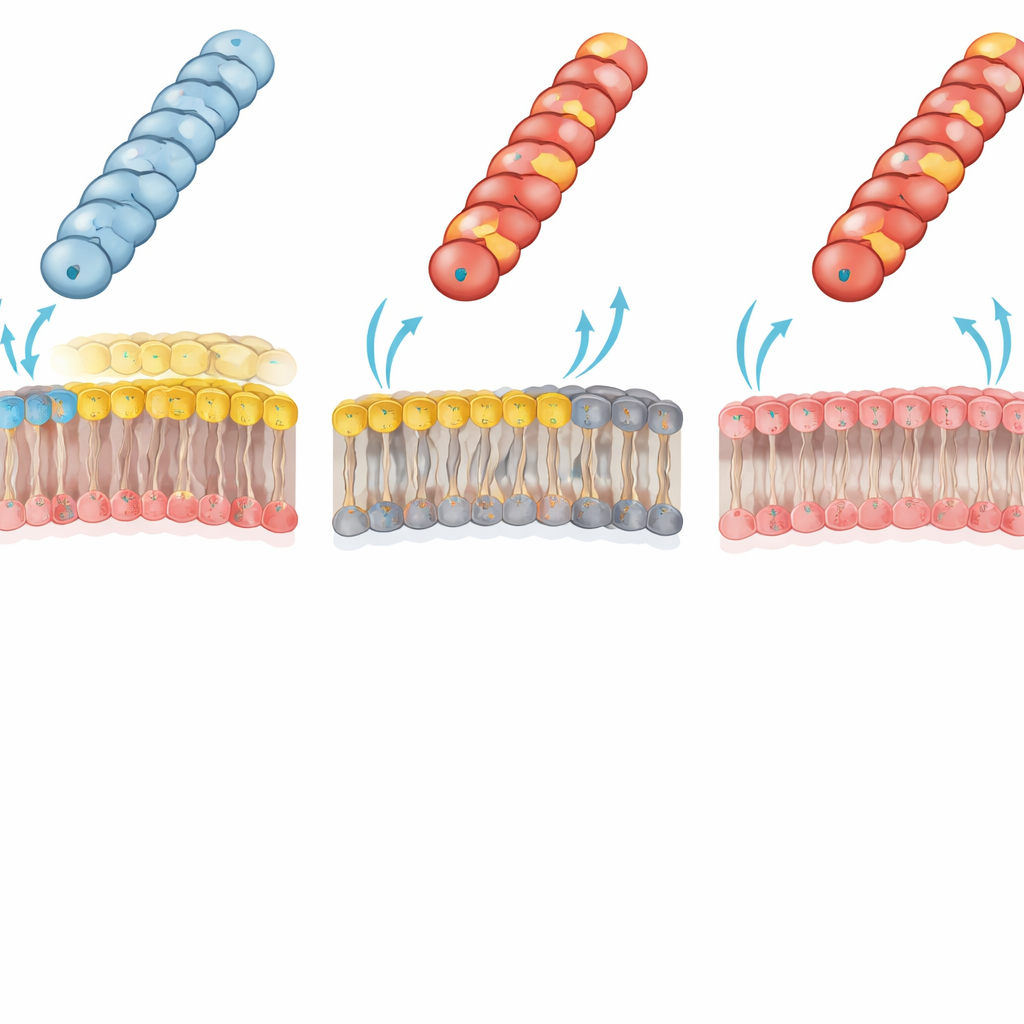
הליפידים בממברנה מחליטים מי יכול לקבל DNA
החוקרים עקבו אחרי הכישלון הדרמטי הזה ונכנסו לעימות אלקטרוסטטי בין הפילוס לממברנת החיצונית של המקבל. בחיידקי גרם‑שליליים טיפוסיים, שכבת הפנימית של הממברנה החיצונית מכילה ליפיד עיקרי "מצוות־מטען" זוויתריוני, פוספטידילאתנולאמין (PE), שנושא הן קבוצה חיובית והן שלילית. הצוות השתמש בזן E. coli מהונדס במיוחד החסר PE; שכבת הפנימית של הממברנה החיצונית שלו מורכבת כולה מליפידים בעלי מטען שלילי. במקבל חסר‑PE זה, הפילוסים החיוביים שהיו מושפלים קודם (עם Gly1Lys, Asp69Lys או Asp69Arg) העבירו כעת את הפלסמידים כמעט ביעילות של סוג הבר. היפוך זה תומך בחוזקה ברעיון שאינטראקציית מטען לא טובה בין משטח פילוס חיובי לממברנה עשירה ב‑PE מונעת בדרך כלל מהקצה של הפילוס לאמץ את הגיאומטריה הנכונה של המגע להעברה יעילה של DNA.
כיצד כוונון אלקטרוסטטי מעצב את התפשטות עמידות לאנטיביוטיקה
ביחד, התוצאות מגלות חלוקת עבודה ברורה. המכאניקה הכימית הקוטעת ומחברת מחדש את שרשרת הפילין ליצירת טבעת היא גמישה למדי — שאריות קצה רבות שונות יכולות עדיין להיות תפרו ולהרכיב פילוס בעל מראה נורמלי. אבל קונוגציה מוצלחת רגישה להפליא לגודל ובמיוחד למטען של שאריות אלו החשופות, כי הן מעצבות את הפוטנציאל החשמלי של פני הפילוס שעליו חייב להתאים סביבת הליפידים של ממברנת המקבל. ה"כוונון" האלקטרוסטטי הזה מסייע להסביר מדוע Gly1 ו‑Asp69 שמורים באופן כה מחמיר בטבע. בנוסף, הוא מצביע על כך ששינויים בהרכב הליפידים הממברנליים — מונעים על‑ידי דחק סביבתי או תנאי המאכסן — עשויים לווסת עד כמה בקלות חיידקים מחליפים פלסמידים הנשאבים גנים לעמידות לאנטיביוטיקה. למעשה, שני השותפים ב"לחיצת היד" החיידקית מתפתחים ביחד על פני השטח כדי לאזן את היתרונות והסיכונים של שיתוף גנים.
ציטוט: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
מילות מפתח: העברה בקונוגציה חיידקית, עמידות לאנטיביוטיקה, מבנה הפילוס, ליפידים ממברנליים, אינטראקציות אלקטרוסטטיות