Clear Sky Science · ru
Циклизация H-пилина и биогенез пилиусов являются неприхотливыми, но электростатические нарушения ухудшают эффективность конъюгации
Почему важны крошечные бактериальные «кабели»
Бактерии постоянно обмениваются ДНК, передавая признаки, такие как устойчивость к антибиотикам, которые могут превратить безвредные микроорганизмы в трудноизлечимые угрозы. Один из основных путей такого обмена — конъюгация, при которой донорная бактерия использует длинный тонкий поверхностный «кабель», называемый пилиусом, чтобы связаться с соседней клеткой и передать плазмидную ДНК. В этом исследовании задают, на первый взгляд, тонкий вопрос с большими последствиями: как именно атомы на поверхности пилиуса и липиды во внешней мембране реципиента контролируют, удастся ли передача ДНК или нет?
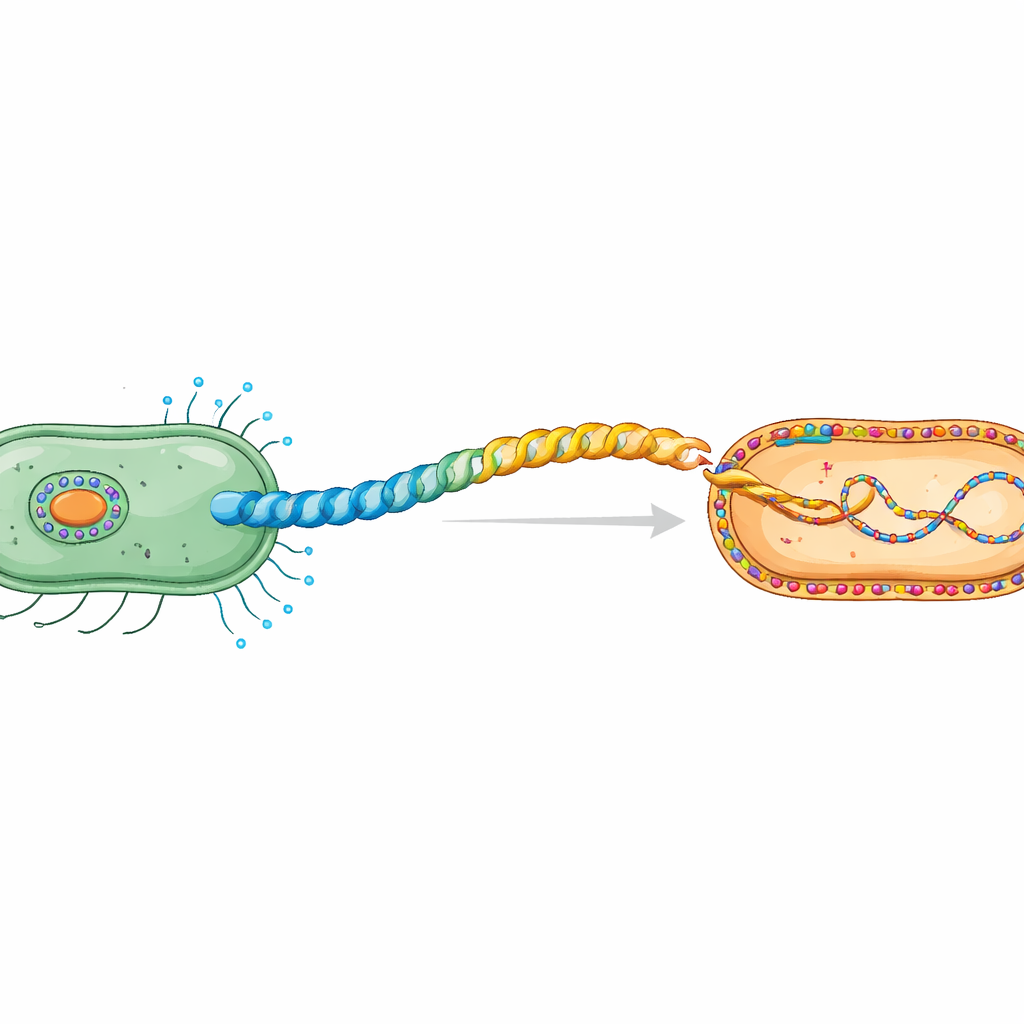
Тайное рукопожатие между бактериальными клетками
Во время конъюгации плазмидная ДНК перемещается от донорной клетки к реципиенту в процессе, зависящем от контакта. Доноры строят специальный пилиус — гибкую спиральную трубку, состоящую из повторяющихся субъединиц пилина. Работа сосредоточена на H‑пилиусе, кодируемом плазмидой IncHI1 R27, представителем семейства плазмид, известных распространением антибиотикорезистентности. Ранее крио‑ЭМ показала, что его пилин TrhA необычен: вместо открытой полипептидной цепи белок «завязан в кольцо» за счёт соединения своего начала (Gly1) и конца (Asp69). Эта циклизация необходима для образования функционального пилиуса, способного передавать ДНК.
Высоко консервативные концы белка, химия, удивительно терпимая к изменениям
Проанализировав большую базу плазмид, авторы изучили 147 последовательностей TrhA из родственных плазмид. Хотя многие позиции варьировали, две остатка, замыкающие кольцо — Gly1 и Asp69 — были абсолютно консервативны, что указывает на мощное эволюционное давление сохранять их. Затем команда систематически меняла эти две позиции в лаборатории, создавая несколько мутантных пилинов. Рентгеновская крио‑ЭМ высокого разрешения показала, что даже довольно разные аминокислоты в положении Asp69 (например, Asn, Ala, Gly или Arg) всё ещё позволяли TrhA циклизоваться и собираться в пилиусы, которые были по структуре почти неотличимы от дикого типа. Другими словами, химия образования кольца и сборки пилиуса оказалась удивительно неприхотливой.
Когда заряд «кабеля» блокирует соединение
Несмотря на нормальный внешний вид, мутантные пилиусы вели себя совершенно иначе в тестах конъюгации с рядом грамотрицательных реципиентов. При замене Asp69 на нейтральные аминокислоты (Asn, Ala, Gly) плазмиды по‑прежнему хорошо передавались в E. coli и Klebsiella pneumoniae. В некоторых других видах выявлялись тонкие закономерности: более крупные боковые цепи обычно обеспечивали немного более высокую эффективность передачи, чем более мелкие. Совсем иная картина наблюдалась при замене Asp69 или Gly1 положительно заряженными аминокислотами, такими как аргинин или лизин. Эти изменения обращали внешний заряд поверхности пилиуса с отрицательного на сильно положительный. Хотя мутантные пилиусы всё ещё формировались, конъюгация в нормальные реципиенты падала до миллиона раз по сравнению с пилиусом дикого типа.
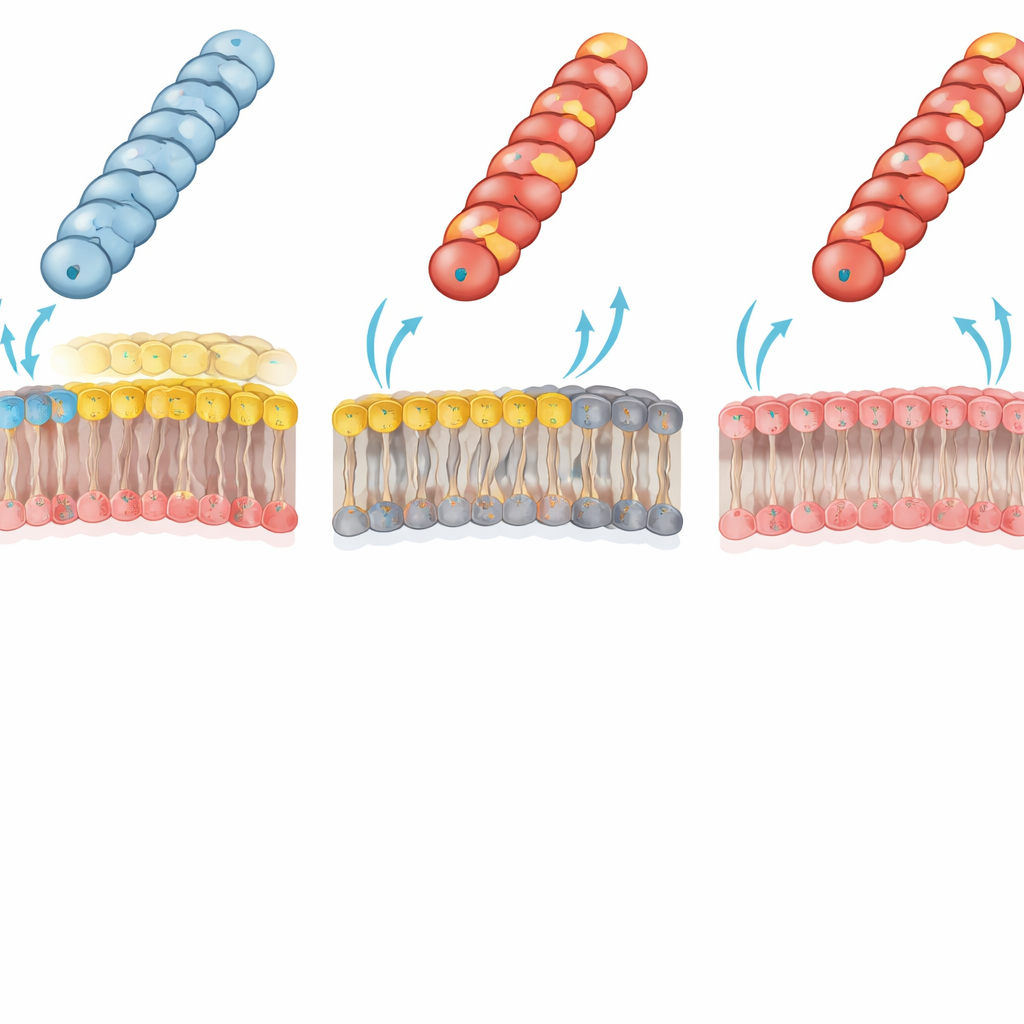
Липиды мембраны решают, кто может получить ДНК
Авторы проследили эту резкую неудачу до электростатического конфликта между пилиусом и внешней мембраной реципиента. У типичных грамотрицательных бактерий внутренний слой внешней мембраны содержит основной «цвиттерионный» фосфолипид фосфатидилэтаноламин (PE), который несёт и положительную, и отрицательную группу. Команда использовала специально сконструированный штамм E. coli, лишённый PE; внутренний лист этого штамма внешней мембраны полностью состоит из отрицательно заряженных липидов. У такого реципиента, дефицитного по PE, ранее непригодные положительно заряженные пилиусы (с Gly1Lys, Asp69Lys или Asp69Arg) теперь передавали плазмиды почти так же эффективно, как дикий тип. Это восстановление функции сильно поддерживает идею о том, что неблагоприятное заряд–зарядовое взаимодействие между положительно заряженной поверхностью пилиуса и PE‑богатой мембраной обычно мешает кончику пилиуса занять правильную контактную геометрию для эффективной передачи ДНК.
Как электростатическая тонкая настройка формирует распространение устойчивости к антибиотикам
В сумме результаты выявляют чёткое разделение ролей. Химический механизм, который разрезает и вновь соединяет цепь пилина для образования кольца, достаточно гибок — многие разные конечные остатки всё ещё могут быть состыкованы и собраны в внешне нормальный пилиус. Но успешная конъюгация исключительно чувствительна к размеру и, особенно, к заряду этих экспонированных остатков, поскольку они формируют поверхностный потенциал пилиуса, который должен соответствовать липидной среде мембраны реципиента. Эта электростатическая «настройка» помогает объяснить, почему Gly1 и Asp69 так строго сохраняются в природе. Также это указывает на то, что изменения в составе липидов мембраны — вызванные стрессом окружающей среды или условиями хозяина — могли бы модулировать готовность бактерий обмениваться плазмидами, несущими гены устойчивости к антибиотикам. По сути, оба участника бактериального «рукопожатия» коэволюционируют свои поверхности, чтобы сбалансировать выгоды и риски обмена генами.
Цитирование: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Ключевые слова: бактериальная конъюгация, антибиотикорезистентность, структура пилиуса, липиды мембраны, электростатические взаимодействия