Clear Sky Science · es
La ciclización de la pilina H y la biogénesis del pilus son promiscuas, pero las perturbaciones electrostáticas perjudican la eficiencia de la conjugación
Por qué importan los diminutos cables bacterianos
Las bacterias intercambian continuamente ADN, compartiendo rasgos como la resistencia a antibióticos que pueden convertir microbios inofensivos en amenazas difíciles de tratar. Una vía principal para este intercambio es la conjugación, en la que una bacteria donante utiliza un cable largo y muy delgado en la superficie —llamado pilus— para conectarse a una vecina y transferir ADN plasmídico. Este estudio plantea una pregunta sorprendentemente sutil con grandes implicaciones: ¿cómo controlan los átomos concretos en la superficie de ese pilus y los lípidos en la membrana externa del receptor si la transferencia de ADN tiene éxito o fracasa?
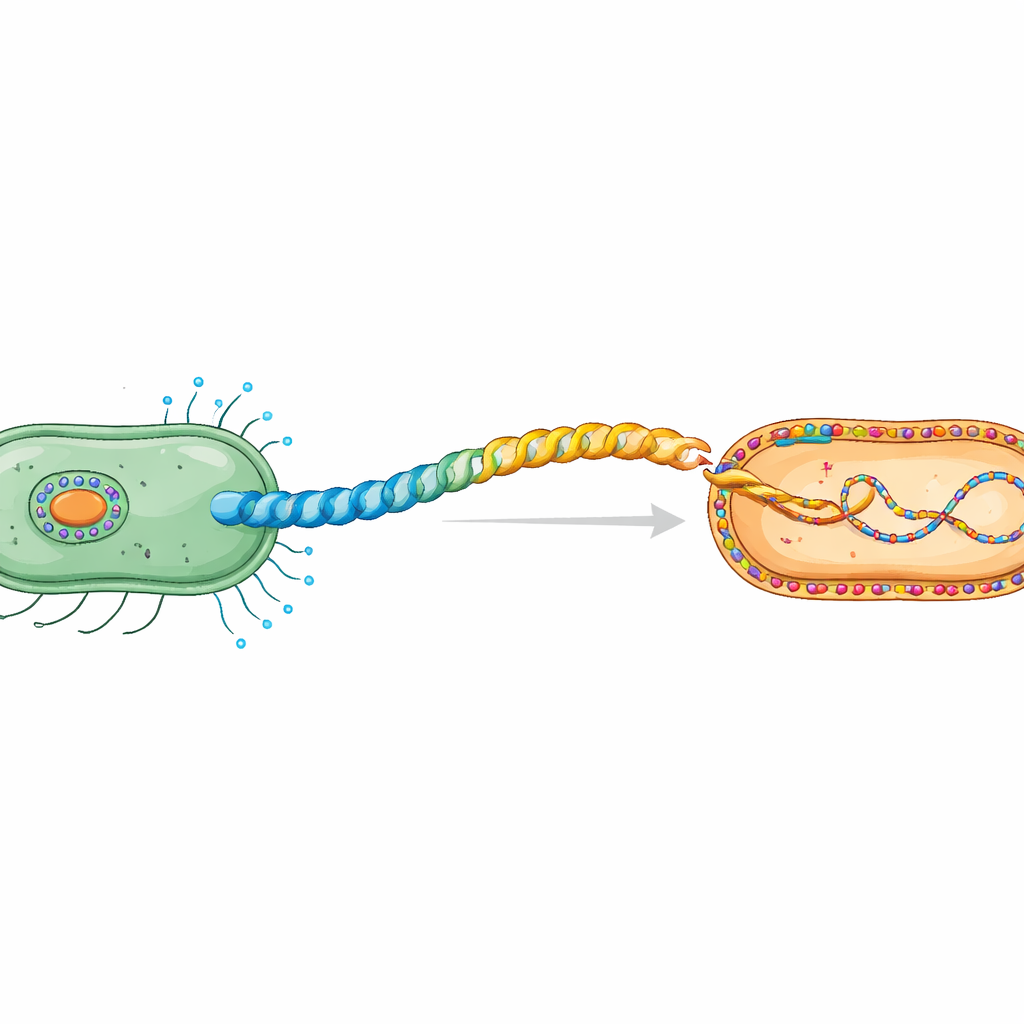
El apretón de manos secreto entre células bacterianas
Durante la conjugación, el ADN plasmídico viaja de una célula donante a una receptora en un proceso que depende del contacto. Las células donantes construyen un pilus especial, un tubo helicoidal flexible formado por unidades repetidas de la proteína pilina. El trabajo se centra en el pilus H codificado por el plásmido IncHI1 R27, una familia de plásmidos conocida por difundir la resistencia a antibióticos. Microscopía crioelectrónica previa reveló que su pilina, TrhA, es inusual: en lugar de tener una cadena abierta, la proteína está “anudada en un anillo” al unirse su inicio (Gly1) y su extremo (Asp69). Esta ciclización es esencial para formar un pilus funcional capaz de transferir ADN.
Puntas proteicas altamente conservadas, química sorprendentemente tolerante
Al explorar una amplia base de datos de plásmidos, los autores examinaron 147 secuencias de TrhA de plásmidos emparentados. Aunque muchas posiciones variaban, los dos residuos que cierran el anillo—Gly1 y Asp69—estaban absolutamente conservados, lo que sugiere una fuerte presión evolutiva para mantenerlos. El equipo cambió sistemáticamente estas dos posiciones en el laboratorio, creando varias pilinas mutantes. La crio‑EM de alta resolución mostró que incluso aminoácidos bastante distintos en Asp69 (como Asn, Ala, Gly o Arg) aún permitían que TrhA se ciclizará y se ensamblara en pilis que eran estructuralmente casi indistinguibles del tipo salvaje. En otras palabras, la química de la formación del anillo y la construcción del pilus era sorprendentemente promiscuosa.
Cuando la carga en el cable bloquea la conexión
A pesar de su apariencia normal, los pilis mutantes se comportaron de forma muy diferente en pruebas de conjugación con una variedad de receptores Gram‑negativos. Cuando Asp69 fue reemplazado por aminoácidos neutros (Asn, Ala, Gly), los plásmidos todavía se transferían bien a E. coli y Klebsiella pneumoniae. En algunas otras especies surgieron tendencias sutiles: las cadenas laterales más grandes generalmente soportaban una eficiencia de transferencia ligeramente mayor que las más pequeñas. Surgió un panorama muy distinto cuando Asp69 o Gly1 fueron reemplazados por aminoácidos cargados positivamente como arginina o lisina. Estos cambios invirtieron el exterior del pilus de cargado negativamente a fuertemente positivo. Aunque los pilis mutantes todavía se formaban, la conjugación hacia receptores normales cayó hasta un millón de veces en comparación con el pilus tipo salvaje.
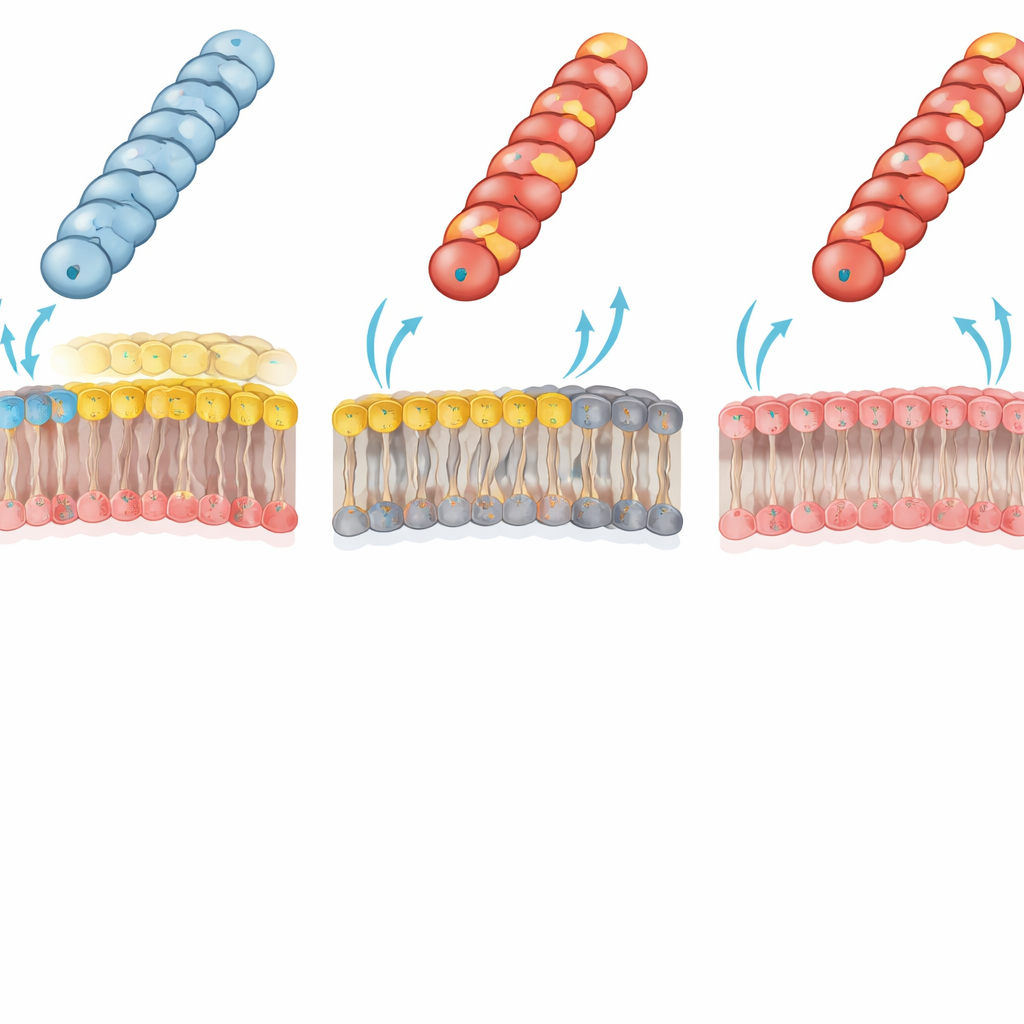
Los lípidos de membrana deciden quién puede recibir ADN
Los autores rastrearon este fracaso dramático hasta un choque electrostático entre el pilus y la membrana externa del receptor. En bacterias Gram‑negativas típicas, la capa interna de la membrana externa contiene un fosfolípido mayoritariamente «zwitteriónico», la fosfatidiletanolamina (PE), que porta tanto un grupo positivo como uno negativo. El equipo utilizó una cepa de E. coli especialmente diseñada carente de PE; su hoja interna de la membrana externa está en su lugar compuesta enteramente por lípidos cargados negativamente. En este receptor deficiente en PE, los pilis previamente inutilizados y cargados positivamente (con Gly1Lys, Asp69Lys o Asp69Arg) ahora transfirieron plásmidos casi con la misma eficiencia que el tipo salvaje. Esta reversión apoya con fuerza la idea de que una interacción carga–carga desfavorable entre una superficie de pilus cargada positivamente y una membrana rica en PE normalmente impide que la punta del pilus adopte la geometría de contacto adecuada para una transferencia de ADN eficiente.
Cómo el ajuste electrostático fino moldea la propagación de la resistencia a antibióticos
En conjunto, los resultados revelan una clara división del trabajo. La maquinaria química que corta y vuelve a unir la cadena de pilina para formar un anillo es bastante flexible: muchos residuos terminales diferentes aún pueden coserse y ensamblarse en un pilus de aspecto normal. Pero la conjugación exitosa es exquisitamente sensible al tamaño y, especialmente, a la carga de estos residuos expuestos, porque configuran el potencial superficial del pilus que debe coincidir con el entorno lipídico de la membrana receptora. Este «ajuste» electrostático ayuda a explicar por qué Gly1 y Asp69 están tan estrictamente conservados en la naturaleza. También sugiere que cambios en la composición de lípidos de la membrana —provocados por estrés ambiental o condiciones del huésped— podrían modular la facilidad con que las bacterias intercambian plásmidos que portan genes de resistencia a antibióticos. En efecto, ambas partes del “apretón de manos” bacteriano coevolucionan sus superficies para equilibrar los beneficios y riesgos del intercambio genético.
Cita: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Palabras clave: conjugación bacteriana, resistencia a antibióticos, estructura del pilus, lípidos de membrana, interacciones electrostáticas