Clear Sky Science · fr
La cyclisation de la piline H et la biogenèse du pilus sont permissives mais des perturbations électrostatiques réduisent l’efficacité de la conjugaison
Pourquoi de minuscules câbles bactériens comptent
Les bactéries échangent constamment de l’ADN, partageant des caractères comme la résistance aux antibiotiques qui peuvent transformer des microbes inoffensifs en agents difficiles à traiter. Une voie majeure de cet échange est la conjugaison, où une bactérie donneuse utilise un long câble fin en surface, appelé pilus, pour se connecter à une voisine et lui transmettre un plasmide. Cette étude pose une question étonnamment subtile mais aux grandes implications : comment les atomes précis à la surface de ce pilus, et les lipides dans la membrane externe du receveur, déterminent‑ils si le transfert d’ADN réussit ou échoue ?
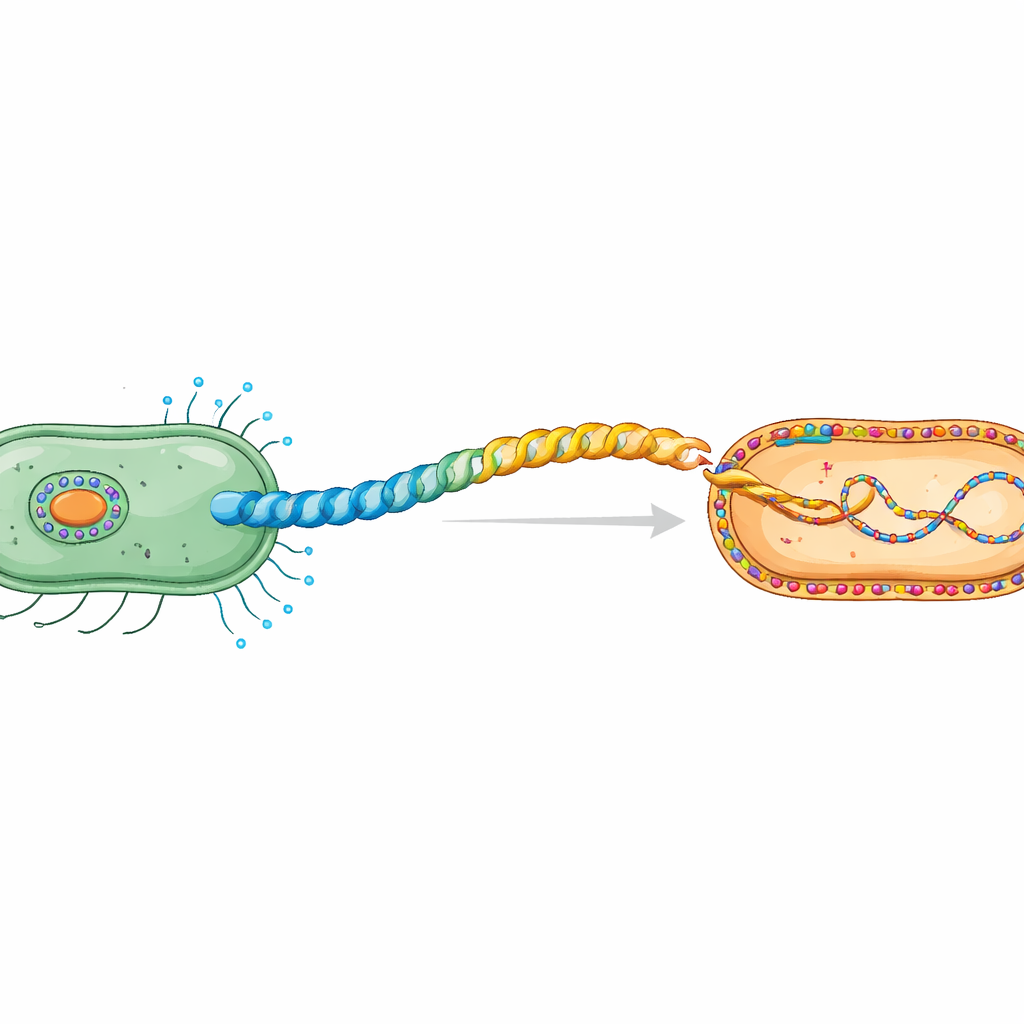
La poignée de main secrète entre cellules bactériennes
Pendant la conjugaison, l’ADN plasmidique voyage d’une cellule donneuse vers une cellule réceptrice dans un processus dépendant du contact. Les donneurs construisent un pilus spécialisé, un tube hélicoïdal flexible composé d’unités répétées de la piline. Le travail se concentre sur le pilus H codé par le plasmide IncHI1 R27, une famille de plasmides connue pour propager la résistance aux antibiotiques. Des études antérieures en cryo‑microscopie électronique ont révélé que sa piline, TrhA, est inhabituelle : au lieu d’avoir une chaîne ouverte, la protéine est « nouée en anneau » en joignant son début (Gly1) et sa fin (Asp69). Cette cyclisation est essentielle pour former un pilus fonctionnel capable de transférer de l’ADN.
Des extrémités protéiques hautement conservées, une chimie étonnamment tolérante
En explorant une large base de données de plasmides, les auteurs ont examiné 147 séquences de TrhA provenant de plasmides apparentés. Bien que de nombreuses positions varient, les deux résidus qui ferment l’anneau — Gly1 et Asp69 — étaient absolument conservés, suggérant une forte pression évolutive pour les maintenir. L’équipe a ensuite modifié systématiquement ces deux positions en laboratoire, créant plusieurs pilines mutantes. La cryo‑EM à haute résolution a montré que même des acides aminés assez différents en position Asp69 (comme Asn, Ala, Gly ou Arg) permettaient encore à TrhA de se cycliser et de s’assembler en pilus dont la structure était presque indistinguable du type sauvage. Autrement dit, la chimie de la formation de l’anneau et de l’assemblage du pilus se révèle étonnamment permissive.
Quand la charge du câble bloque la connexion
Malgré leur apparence normale, les pilus mutants se comportaient très différemment lors d’essais de conjugaison avec une gamme de récepteurs à Gram négatif. Lorsque Asp69 était remplacé par des acides aminés neutres (Asn, Ala, Gly), les plasmides se transféraient encore bien dans E. coli et Klebsiella pneumoniae. Chez d’autres espèces, des tendances subtiles ont émergé : des chaînes latérales plus grosses soutenaient généralement une efficacité de transfert légèrement supérieure à celle des plus petites. Un tableau très différent est apparu lorsque Asp69 ou Gly1 étaient remplacés par des acides aminés chargés positivement comme l’arginine ou la lysine. Ces changements inversaient l’extérieur du pilus, passant d’une surface négative à une surface fortement positive. Bien que les pilus mutants se forment toujours, la conjugaison vers des récepteurs normaux chutait jusqu’à un million de fois par rapport au pilus sauvage.
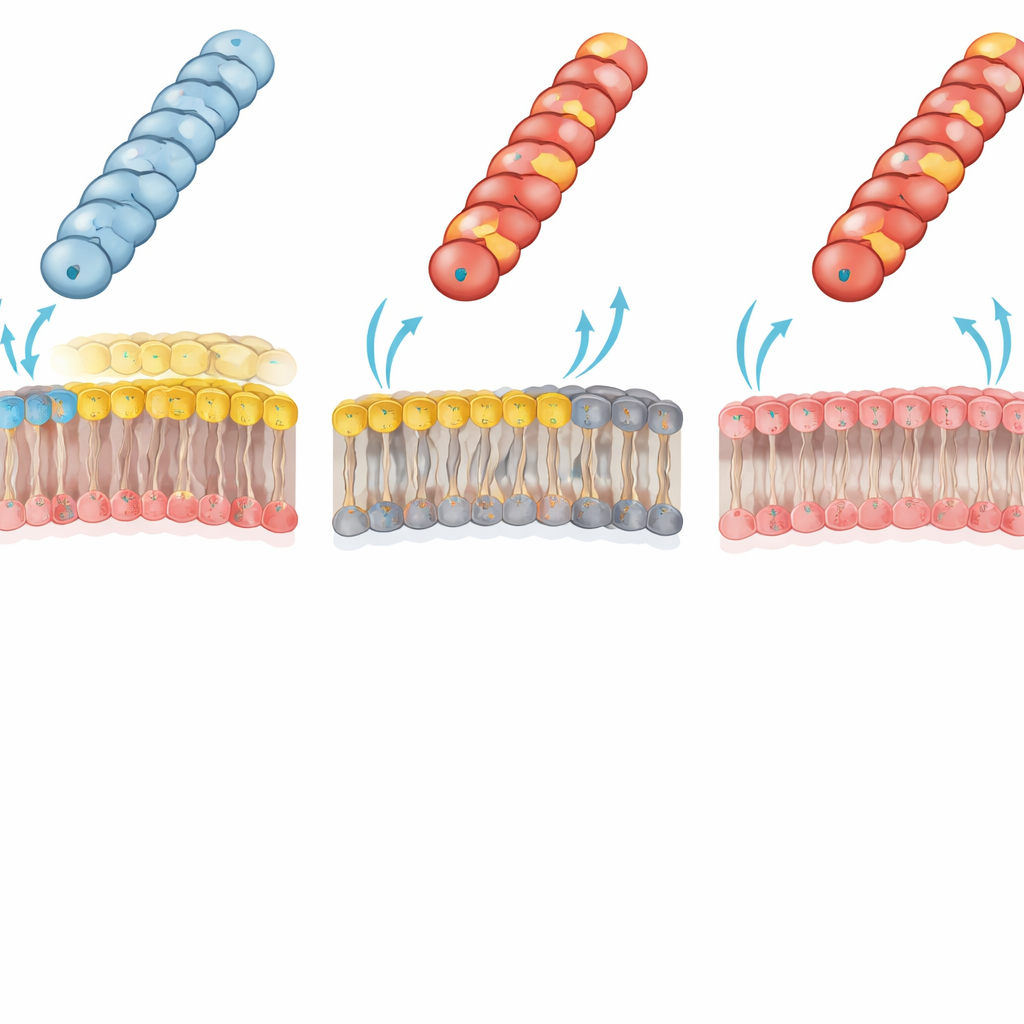
Les lipides membranaires décident qui peut recevoir de l’ADN
Les auteurs ont attribué cet échec spectaculaire à un conflit électrostatique entre le pilus et la membrane externe du récepteur. Chez les bactéries à Gram négatif typiques, la feuillet interne de la membrane externe contient un phospholipide majeur « zwitterionique », la phosphatidyléthanolamine (PE), qui porte à la fois un groupe positif et un groupe négatif. L’équipe a utilisé une souche d’E. coli spécialement modifiée dépourvue de PE ; la feuillet interne de sa membrane externe est alors entièrement composé de lipides à charge négative. Chez ce récepteur déficient en PE, les pilus précédemment déficients mais chargés positivement (avec Gly1Lys, Asp69Lys ou Asp69Arg) ont désormais transféré des plasmides presque aussi efficacement que le type sauvage. Cette inversion soutient fortement l’idée qu’une interaction charge–charge défavorable entre une surface de pilus positivement chargée et une membrane riche en PE empêche normalement la pointe du pilus d’adopter la géométrie de contact appropriée pour un transfert d’ADN efficace.
Comment l’accordage électrostatique façonne la propagation de la résistance aux antibiotiques
Dans l’ensemble, les résultats révèlent une division du travail claire. La machinerie chimique qui coupe et recoud la chaîne de piline pour former un anneau est assez flexible — de nombreux résidus terminaux différents peuvent encore être soudés et assemblés en un pilus d’apparence normale. Mais la conjugaison réussie est extrêmement sensible à la taille et, surtout, à la charge de ces résidus exposés, car ils modèlent le potentiel de surface du pilus qui doit être compatible avec l’environnement lipidique de la membrane du récepteur. Cet « accordage » électrostatique aide à expliquer pourquoi Gly1 et Asp69 sont si strictement conservés dans la nature. Il suggère aussi que des changements dans la composition lipidique des membranes — provoqués par le stress environnemental ou par les conditions de l’hôte — pourraient moduler la facilité avec laquelle les bactéries échangent des plasmides portant des gènes de résistance aux antibiotiques. En pratique, les deux partenaires de la « poignée de main » bactérienne co‑évoluent leurs surfaces pour équilibrer les bénéfices et les risques du partage de gènes.
Citation: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Mots-clés: conjugaison bactérienne, résistance aux antibiotiques, structure du pilus, lipides membranaires, interactions électrostatiques