Clear Sky Science · ar
دور إغلاق حلقة H‑pilin وتكوين البيلوس: سهولة التشكّل مقابل تأثيرات كهربائية تقلّل كفاءة الاقتران
لماذا تهمّ هذه الأسلاك البكتيرية الصغيرة
تتبادل البكتيريا باستمرار قطعاً من الحمض النووي، ناشرةً صفات مثل مقاومة المضادات الحيوية التي قد تحوّل ميكروبات غير ضارة إلى تهديدات يصعب علاجها. أحد الطرق الرئيسية لهذا التبادل هو الاقتران (conjugation)، حيث تستخدم الخلية المانحة سلكاً سطحياً طويلاً ورقيقاً يُسمى البيلوس لربط خلية مجاورة ونقل الحمض النووي البلازميدي إليها. تطرح هذه الدراسة سؤالاً يبدو دقيقاً لكن له تبعات كبيرة: كيف تتحكم الذرات الدقيقة على سطح ذلك البيلوس والدهون في غشاء الخلية المستقبلة فيما إذا كان نقل الحمض النووي سينجح أم يفشل؟
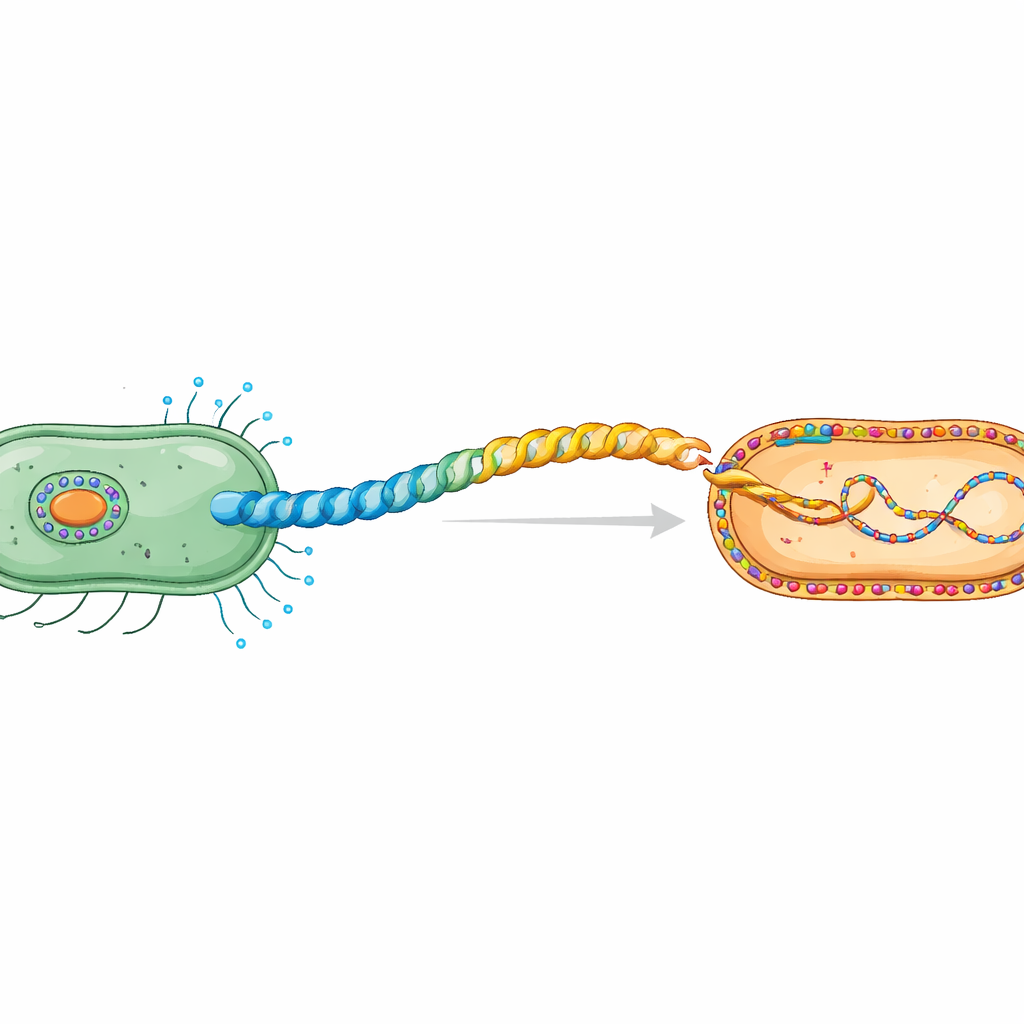
المصافحة السرية بين الخلايا البكتيرية
أثناء الاقتران، ينتقل الحمض النووي البلازميدي من الخلية المانحة إلى المستقبلة عبر عملية تعتمد على الاتصال المباشر. تبني الخلايا المانحة بيلوساً خاصاً، وهو أنبوب لولبي مرن يتكوّن من وحدات متكررة من بروتين البيلين. تركز العمل على بيلوس H المشفّر بواسطة البلازميد IncHI1 المعروف باسم R27، وهو من عائلة بلازميدات مرتبطة بنشر مقاومة المضادات الحيوية. أظهرت دراسات سابقة بالتصوير الإلكترونِي بالتبريد أن بروتين البيلين TrhA غير اعتيادي: بدلاً من امتلاكه سلسلة حرة النهايات، يُغلق البروتين على نفسه بتوصيل بدايته (Gly1) ونهايته (Asp69)، مكوّناً حلقة. هذا الإغلاق ضروري لتشكيل بيلوس وظيفي قادر على نقل الحمض النووي.
رؤوس بروتينية محفوظة بشدة لكن كيمياء مرنة بشكل مدهش
من خلال تنقيب قاعدة بيانات بلازميدات كبيرة، فحص المؤلفون 147 تسلسلاً لـ TrhA من بلازميدات ذات صلة. على الرغم من أن كثيراً من المواضع اختلفت، فإن البقرتين المسؤولتين عن إغلاق الحلقة—Gly1 وAsp69—كانتا محفوظتين تماماً، مما يشير إلى ضغط تطوري قوي للحفاظ عليهما. لاحقاً غيّر الفريق هذين الموضعين بشكل منهجي في المختبر، مكوّنين عدداً من طفرات البيلين. أظهر التصوير الإلكتروني بالجمود عالي الدقة أن أحجام حمض أميني مختلفة نسبياً عند Asp69 (مثل Asn، Ala، Gly، أو Arg) لا تزال تسمح لـ TrhA بالإغلاق والتجمع إلى بيلوسات تبدو هيكلياً شبيهة جداً بالنمط البري. بمعنى آخر، كانت كيمياء تكوّن الحلقة وبناء البيلوس مرنة إلى حد مدهش.
عندما تمنع الشحنة على السلك الاتصال
رغم مظهرها الطبيعي، تصرفت البيلوسات الطافرة بشكل مختلف جداً في اختبارات الاقتران مع مجموعة من المستقبلات سالبة الغرام. عندما استُبدل Asp69 بأحماض أمينية محايدة (Asn، Ala، Gly)، استمر نقل البلازميدات جيداً إلى E. coli وKlebsiella pneumoniae. في بعض الأنواع الأخرى ظهرت اتجاهات دقيقة: السلاسل الجانبية الأكبر دعمت عموماً كفاءة نقل أعلى قليلاً من السلاسل الأصغر. انقلب المشهد تماماً عندما استُبدل Asp69 أو Gly1 بأحماض أمينية موجبة الشحنة مثل الأرجينين أو الليسين. هذه التغيرات جعلت السطح الخارجي للبيلوس يتحول من مشحون سلبياً إلى موجب بشدة. ومع أن البيلوسات الطافرة ظلت تتكوّن، انخفضت قدرة الاقتران إلى مستقبلات طبيعية بما يصل إلى فرق مليون مرة مقارنة بالبيلوس البري.
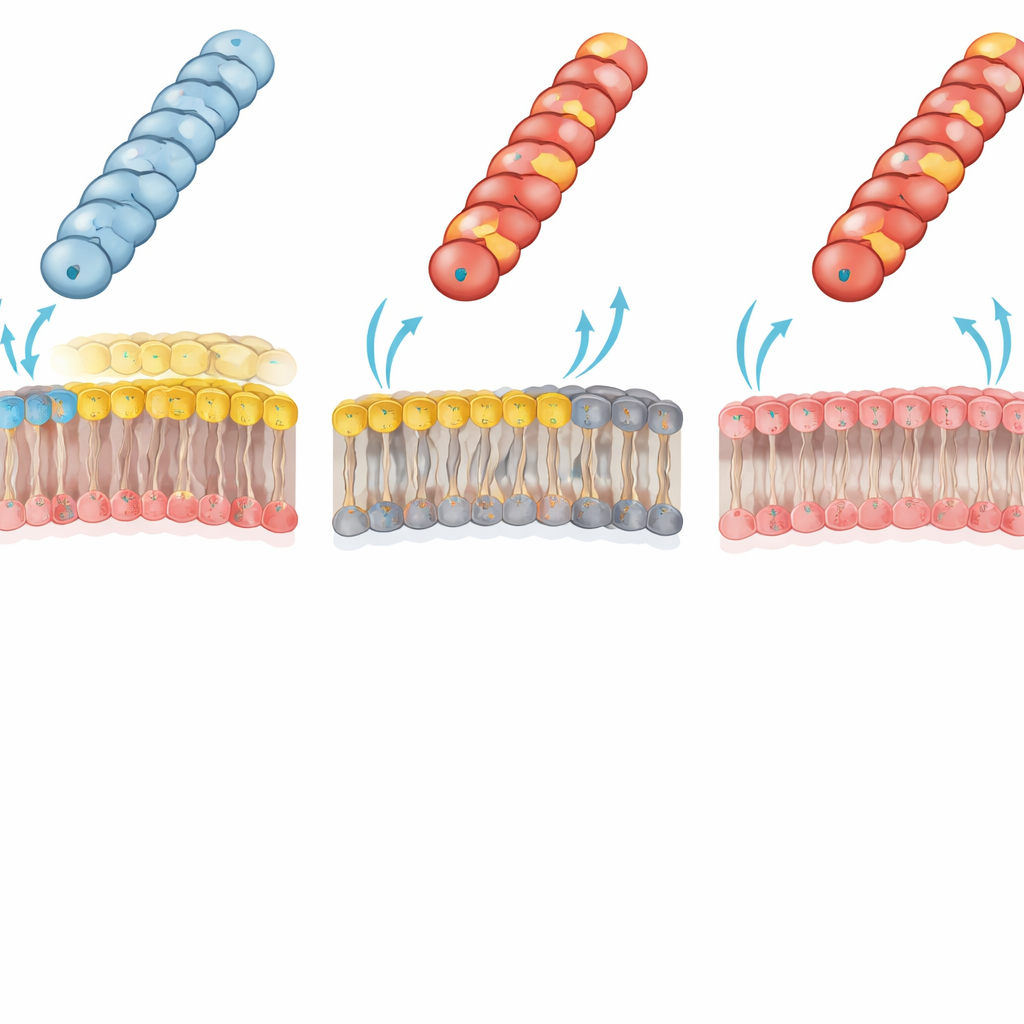
دهون الغشاء تحدد من يمكنه استقبال الحمض النووي
عزت المؤلفون هذا الفشل الدرامي إلى اصطدام كهروستاتيكي بين البيلوس وغشاء الخلية الخارجي للمستقبل. في البكتيريا سالبة الغرام النموذجية، تحتوي الطبقة الداخلية للغشاء الخارجي على فسفوليبيد رئيسي "زويتريوني"، الفسفاتيديليثانولامين (PE)، الذي يحمل مجموعات موجبة وسالبة معاً. استخدم الفريق سلالة هندسية من E. coli تفتقر إلى PE؛ إذ بُنيت الطبقة الداخلية لغشائها الخارجي بالكامل من دهون مشحونة سلبياً بدلاً من ذلك. في هذه المستقبلات الخالية من PE، استعيدت قدرة البيلوسات الإيجابية المشحونة سابقاً (مثل Gly1Lys، Asp69Lys أو Asp69Arg) على نقل البلازميدات تقريباً بمثل كفاءة النمط البري. يدعم هذا النتيجة بقوة الفكرة القائلة بأن التفاعل الضار بين شحنتي السطح الموجبة للبيلوس وغشاء غني بالـ PE يمنع عادةً الطرف البيلوسي من اعتماد هندسة اتصال مناسبة لنقل الحمض النووي بكفاءة.
كيف يشكّل الضبط الكهربائي الدقيق انتشار مقاومة المضادات الحيوية
بالجمع بين النتائج، تكشف الدراسة عن تقسيم واضح للمهام. الآلية الكيميائية التي تقطع وتلحم سلسلة البيلين لتشكيل حلقة مرنة إلى حد كبير—فالعديد من البقايا النهائية المختلفة يمكن ربطها وتشكيل بيلوس يبدو طبيعياً. لكن نجاح الاقتران حساس جداً لحجم وبوجه خاص لشحنة هذه البقايا المكشوفة، لأنها تشكل الجهد السطحي للبيلوس الذي يجب أن يتوافق مع بيئة الدهون في غشاء الخلية المستقبلة. يساعد هذا الضبط الكهروستاتيكي في تفسير لماذا تُحافَظ Gly1 وAsp69 بصرامة في الطبيعة. كما يوحي بأن التغيرات في تركيب دهون الغشاء—التي قد تفرضها ضغوط بيئية أو ظروف العائل—يمكن أن تعدل مدى استعداد البكتيريا لتبادل البلازميدات الحاملة لجينات مقاومة المضادات الحيوية. فعلياً، يتطور شريكا "المصافحة" البكتيرية معاً على أسطحهما لموازنة فوائد ومخاطر تبادل الجينات.
الاستشهاد: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
الكلمات المفتاحية: الاقتسام البكتيري, مقاومة المضادات الحيوية, بنية البيلوس, دهون الغشاء, التفاعلات الكهروستاتيكية