Clear Sky Science · de
H‑Pilin‑Cyclisierung und Pili‑Biogenese sind tolerant, doch elektrostatische Störungen beeinträchtigen die Konjugationseffizienz
Warum winzige bakterielle Kabel wichtig sind
Bakterien tauschen ständig DNA aus und geben damit Eigenschaften wie Antibiotikaresistenz weiter, die harmlose Mikroben in schwer behandelbare Bedrohungen verwandeln können. Ein zentraler Weg dieses Austauschs ist die Konjugation, bei der eine Spenderbakterie ein langes, haarfeines Oberflächenkabel — einen Pilus — nutzt, um Kontakt zu einem Nachbarn herzustellen und Plasmid‑DNA zu übertragen. Diese Studie stellt eine überraschend subtile Frage mit großen Folgen: Wie beeinflussen die genauen Atome auf der Pilusoberfläche und die Lipide in der äußeren Membran des Empfängers, ob der DNA‑Transfer gelingt oder scheitert?
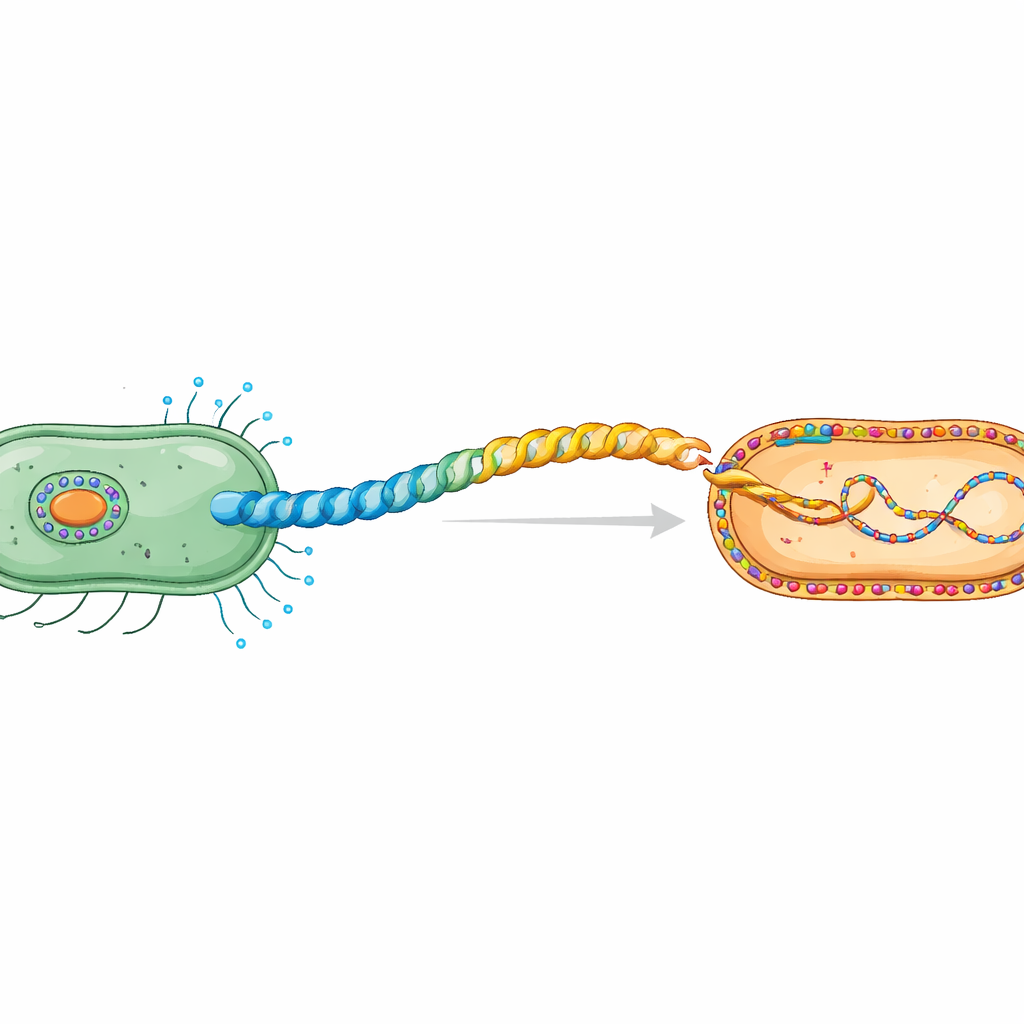
Der geheime Händedruck zwischen bakteriellen Zellen
Während der Konjugation wandert Plasmid‑DNA vom Spender zur Empfängerzelle in einem kontaktabhängigen Prozess. Spenderzellen bauen einen speziellen Pilus, ein flexibles, helicales Rohr aus wiederholten Pilin‑Proteinbausteinen. Die Arbeit konzentriert sich auf den H‑Pilus, der vom IncHI1‑Plasmid R27 kodiert wird, einer Plasmidfamilie, die für die Verbreitung von Antibiotikaresistenz bekannt ist. Frühere Kryo‑Elektronenmikroskopie zeigte, dass sein Pilin, TrhA, ungewöhnlich ist: Statt einer offenen Kette ist das Protein durch Verknüpfung seines Beginns (Gly1) und seines Endes (Asp69) „zu einem Ring gebunden“. Diese Cyclisierung ist essentiell für die Bildung eines funktionalen Pilus, der DNA übertragen kann.
Stark konservierte Proteinenden, überraschend tolerante Chemie
Durch Auswertung einer großen Plasmiddatenbank untersuchten die Autoren 147 TrhA‑Sequenzen verwandter Plasmide. Obwohl viele Positionen variierten, waren die beiden Aminosäuren, die den Ring schließen — Gly1 und Asp69 — absolut konserviert, was auf starken evolutionären Druck hindeutet, sie beizubehalten. Das Team veränderte diese beiden Positionen systematisch im Labor und erzeugte mehrere mutante Piline. Hochauflösende Kryo‑EM zeigte, dass selbst recht unterschiedliche Aminosäuren an Asp69 (etwa Asn, Ala, Gly oder Arg) TrhA weiterhin cyclisieren und zu Pili assembleiren ließen, die strukturell kaum vom Wildtyp zu unterscheiden waren. Anders gesagt: Die Chemie der Ringbildung und des Piliaufbaus war überraschend promiscuös.
Wenn Ladung am Kabel die Verbindung blockiert
Trotz normaler Erscheinung verhielten sich die mutanten Pili in Konjugationstests mit verschiedenen gramnegativen Empfängern sehr unterschiedlich. Wurde Asp69 durch neutrale Aminosäuren (Asn, Ala, Gly) ersetzt, übertragen sich Plasmide weiterhin gut in E. coli und Klebsiella pneumoniae. Bei einigen anderen Arten traten subtile Trends auf: Größere Seitenketten unterstützten allgemein leicht höhere Übertragungseffizienzen als kleinere. Ein ganz anderes Bild zeigte sich, wenn Asp69 oder Gly1 durch positiv geladene Aminosäuren wie Arginin oder Lysin ersetzt wurden. Diese Änderungen kehrten die Außenseite des Pilus von negativ zu stark positiv. Obwohl die mutanten Pili weiterhin gebildet wurden, sank die Konjugation in normale Empfänger im Vergleich zum Wildtyp‑Pilus um bis zu eine Millionfach.
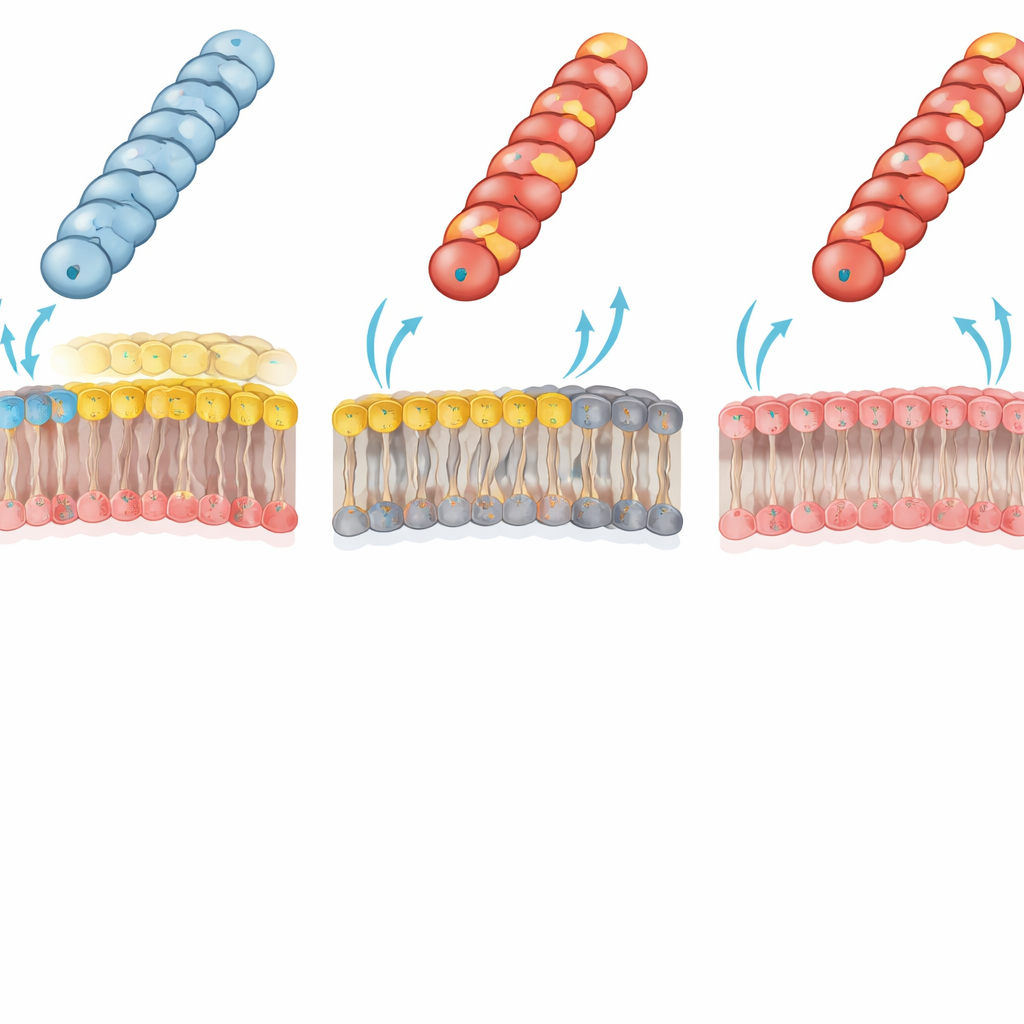
Membranlipide entscheiden, wer DNA empfangen kann
Die Autoren führten dieses dramatische Scheitern auf einen elektrostatischen Zusammenstoß zwischen Pilus und äußerer Membran des Empfängers zurück. In typischen gramnegativen Bakterien enthält die innere Lage der äußeren Membran ein wichtiges „zwitterionisches“ Phospholipid, Phosphatidylethanolamin (PE), das sowohl eine positive als auch eine negative Gruppe trägt. Das Team verwendete einen speziell konstruierten E. coli‑Stamm ohne PE; dessen innere Lage der äußeren Membran besteht stattdessen vollständig aus negativ geladenen Lipiden. In diesem PE‑defizienten Empfänger übertragen die zuvor funktionsgestörten positiv geladenen Pili (mit Gly1Lys, Asp69Lys oder Asp69Arg) Plasmide nun nahezu so effizient wie der Wildtyp. Diese Umkehr stützt stark die Idee, dass eine ungünstige Ladungs‑Ladungs‑Interaktion zwischen einer positiv geladenen Pilusoberfläche und der PE‑reichen Membran normalerweise verhindert, dass die Pilusspitze die richtige Kontaktgeometrie für effizienten DNA‑Transfer einnimmt.
Wie elektrostatische Feinabstimmung die Verbreitung von Antibiotikaresistenz formt
Insgesamt zeigen die Ergebnisse eine klare Arbeitsteilung. Die chemische Maschinerie, die die Pilinkette schneidet und wieder verbindet, um einen Ring zu bilden, ist ziemlich flexibel — viele verschiedene Endreste können trotzdem miteinander verknüpft und zu einem normal aussehenden Pilus assemblieren. Erfolgreiche Konjugation ist jedoch hochsensitiv gegenüber Größe und vor allem der Ladung dieser exponierten Reste, weil sie das Oberflächenpotenzial des Pilus formen müssen, das zur Lipidumgebung der Empfängermembran passen muss. Diese elektrostatische „Feinabstimmung“ erklärt, warum Gly1 und Asp69 in der Natur so streng konserviert sind. Sie legt auch nahe, dass Veränderungen in der Membranlipidzusammensetzung — bedingt durch Umweltstress oder Wirtsbedingungen — beeinflussen könnten, wie leicht Bakterien Plasmide mit Antibiotikaresistenzgenen austauschen. Effektiv ko‑evolvieren beide Partner des bakteriellen „Händedrucks“ ihre Oberflächen, um den Nutzen und die Risiken des Genaustauschs auszubalancieren.
Zitation: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Schlüsselwörter: bakterielle Konjugation, Antibiotikaresistenz, Pilusstruktur, Membranlipide, elektrostatische Wechselwirkungen