Clear Sky Science · pl
Cyklizacja białka H pilin i biogeneza pilusa są liberalne, lecz zaburzenia elektrostatyczne obniżają efektywność koniugacji
Dlaczego drobne bakteryjne przewody mają znaczenie
Bakterie nieustannie wymieniają DNA, przekazując cechy takie jak odporność na antybiotyki, które mogą przemienić nieszkodliwe mikroby w trudne do leczenia zagrożenia. Jedną z głównych dróg tego transferu jest koniugacja, w której komórka-dawca wykorzystuje długi, cienki jak włos kabel powierzchniowy zwany pilusem, aby połączyć się z sąsiadem i przekazać plazmidowe DNA. W tym badaniu zadano pozornie subtelne pytanie o dużych konsekwencjach: jak konkretne atomy na powierzchni pilusa oraz lipidy w zewnętrznej błonie biorcy kontrolują, czy transfer DNA powiedzie się czy zawiedzie?
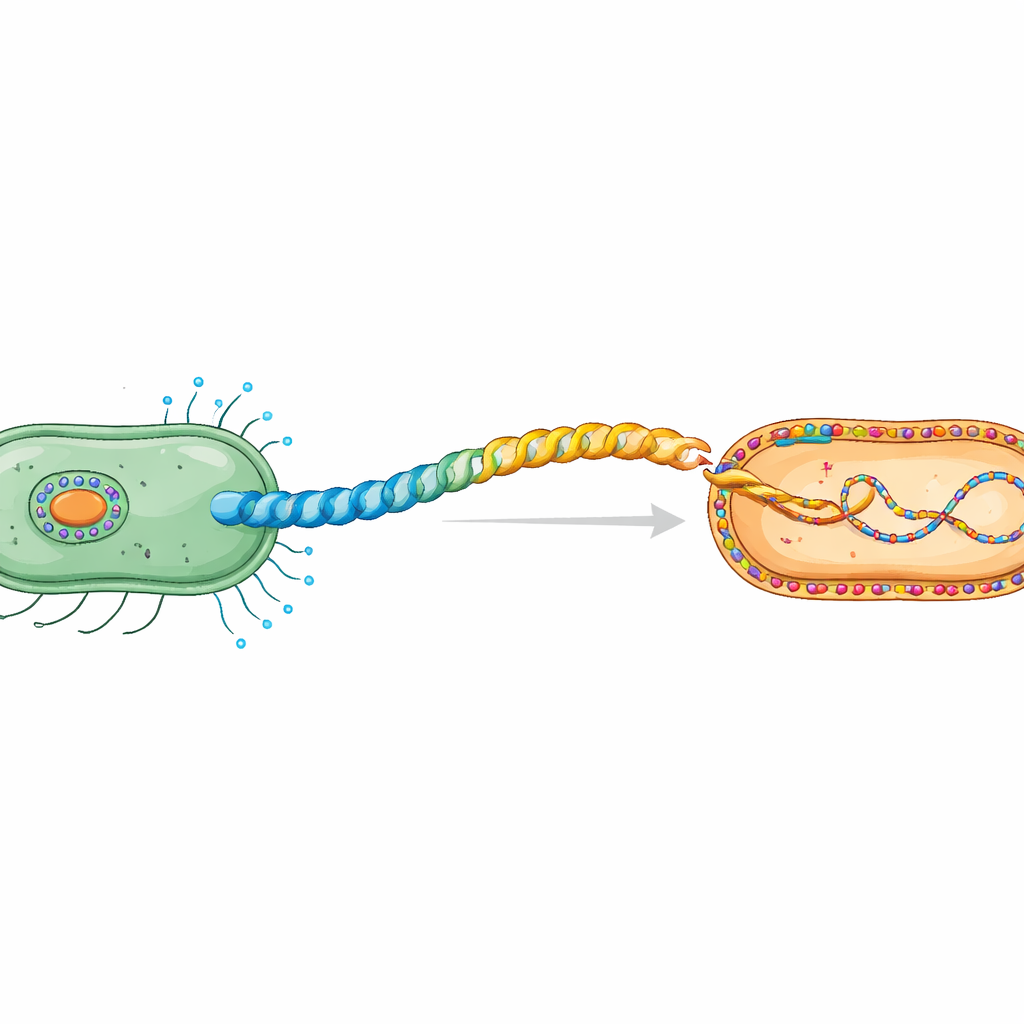
Tajny uścisk dłoni między komórkami bakteryjnymi
Podczas koniugacji plazmidowe DNA przemieszcza się z komórki-dawcy do biorcy w procesie zależnym od kontaktu. Komórki-dawcy budują specjalny pilus — elastyczną, helikalną rurkę zbudowaną z powtarzających się jednostek białkowych piliny. Praca skupia się na pilusie H kodowanym przez plazmid IncHI1 R27, rodzinę plazmidów znaną z szerzenia odporności na antybiotyki. Wcześniejsze badania za pomocą krioelektronowej mikroskopii wykazały, że jego pilina, TrhA, jest nietypowa: zamiast łańcucha z otwartymi końcami, białko jest „związane w pierścień” przez połączenie początku (Gly1) i końca (Asp69). Ta cyklizacja jest niezbędna do utworzenia funkcjonalnego pilusa zdolnego do przekazywania DNA.
Bardzo zachowane końcówki białka, zaskakująco tolerancyjna chemia
Analizując dużą bazę plazmidów, autorzy zbadali 147 sekwencji TrhA z pokrewnych plazmidów. Choć wiele pozycji wykazywało zmienność, dwa reszty zamykające pierścień — Gly1 i Asp69 — były absolutnie zachowane, co sugeruje silną presję ewolucyjną na ich utrzymanie. Zespół następnie systematycznie zmieniał te dwie pozycje w laboratorium, tworząc kilka mutantów piliny. Krio-EM o wysokiej rozdzielczości pokazała, że nawet dość różne aminokwasy w pozycji Asp69 (takie jak Asn, Ala, Gly czy Arg) nadal pozwalały TrhA na cyklizację i składanie się w pilusy, które były strukturalnie niemal nieodróżnialne od typu dzikiego. Innymi słowy, chemia tworzenia pierścienia i budowy pilusa okazała się zaskakująco liberalna.
Kiedy ładunek na kablu blokuje połączenie
Pomimo normalnego wyglądu, mutantowe pilusy zachowywały się zupełnie inaczej w testach koniugacji z różnymi biorcami Gram-ujemnymi. Gdy Asp69 zastąpiono aminokwasami obojętnymi (Asn, Ala, Gly), plazmidy nadal dobrze się przenosiły do E. coli i Klebsiella pneumoniae. W niektórych innych gatunkach pojawiały się subtelne trendy: większe łańcuchy boczne zwykle wspierały nieco wyższą efektywność transferu niż mniejsze. Zupełnie inny obraz dawały zamiany Asp69 lub Gly1 na dodatnio naładowane aminokwasy, takie jak arginina czy lizyna. Zmiany te odwracały zewnętrzną powierzchnię pilusa z ujemnie na silnie dodatnio naładowaną. Chociaż mutantowe pilusy wciąż się formowały, koniugacja do normalnych biorców spadła nawet do miliona razy w porównaniu z pilusem typu dzikiego.
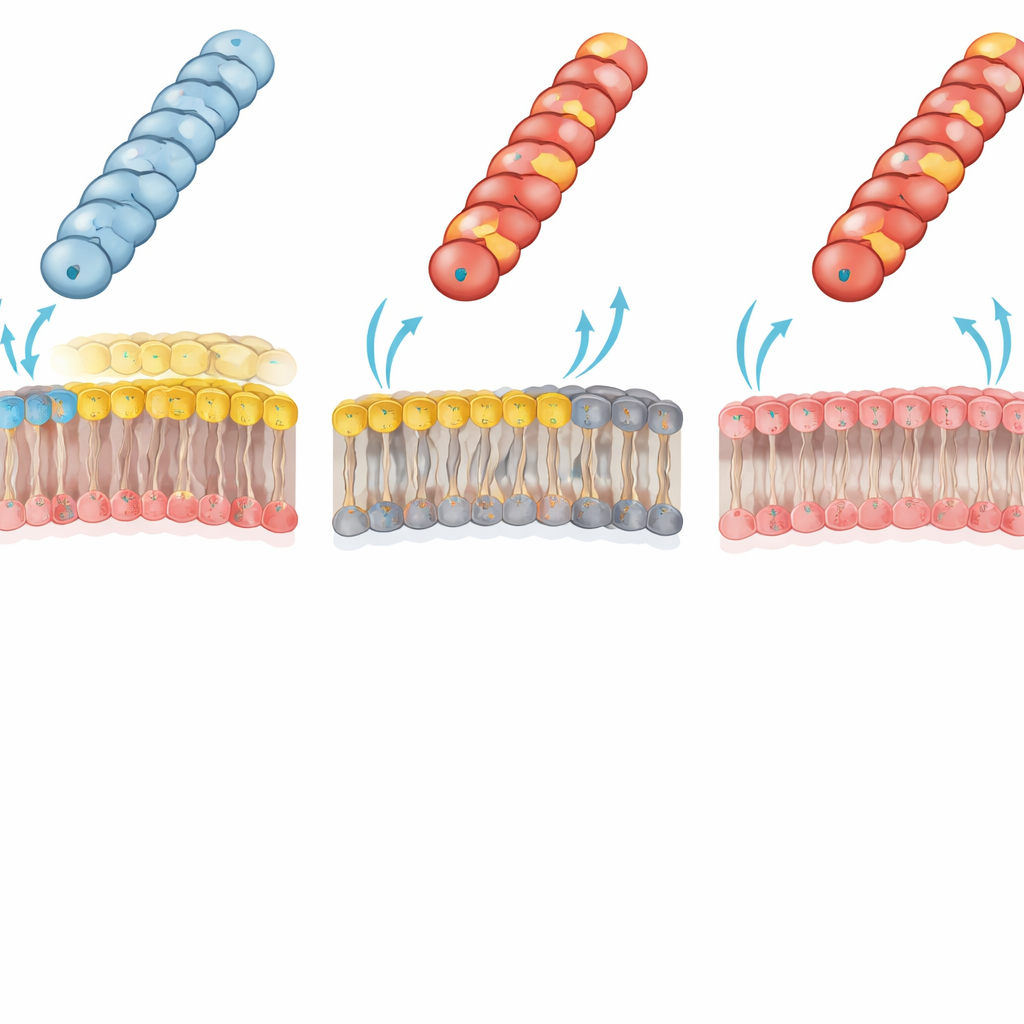
Lipidy błonowe decydują, kto może otrzymać DNA
Autorzy wyśledzili tę dramatyczną niepowodzenie do zderzenia elektrostatycznego między pilusem a zewnętrzną błoną biorcy. W typowych bakteriach Gram-ujemnych wewnętrzna warstwa zewnętrznej błony zawiera dominujący „zwitterjonowy” fosfolipid — fosfatydyloetanolaminę (PE), który niesie zarówno grupę dodatnią, jak i ujemną. Zespół użył specjalnie zmodyfikowanego szczepu E. coli pozbawionego PE; jego wewnętrzna warstwa zewnętrznej błony zbudowana była zamiast tego w całości z ujemnie naładowanych lipidów. U tego biorcy pozbawionego PE wcześniej niezdolne do transferu dodatnio naładowane pilusy (z Gly1Lys, Asp69Lys lub Asp69Arg) przenosiły plazmidy niemal tak efektywnie jak typ dziki. To odwrócenie potwierdza hipotezę, że niekorzystna interakcja ładunek–ładunek między dodatnio naładowaną powierzchnią pilusa a bogatą w PE błoną normalnie uniemożliwia końcówce pilusa przyjęcie odpowiedniej geometrii kontaktu potrzebnej do efektywnego transferu DNA.
Jak elektrostatyczne strojeni wpływa na rozprzestrzenianie się odporności na antybiotyki
Podsumowując, wyniki ujawniają wyraźny podział zadań. Mechanizm chemiczny przecinający i ponownie łączący łańcuch piliny, tworząc pierścień, jest dość elastyczny — wiele różnych reszt końcowych nadal można zszyć i zmontować w wyglądający normalnie pilus. Jednak udana koniugacja jest niezwykle wrażliwa na wielkość i szczególnie na ładunek tych odsłoniętych reszt, ponieważ kształtują one potencjał powierzchni pilusa, który musi odpowiadać lipidowemu środowisku błony biorcy. To elektrostatyczne „strojenie” pomaga wyjaśnić, dlaczego Gly1 i Asp69 są w przyrodzie tak surowo zachowane. Sugeruje też, że zmiany w składzie lipidów błonowych — wywołane stresem środowiskowym lub warunkami gospodarza — mogą modulować gotowość bakterii do wymiany plazmidów niosących geny odporności na antybiotyki. W efekcie obaj partnerzy w bakteryjnym „uścisku dłoni” współewoluują swoje powierzchnie, by wyważyć korzyści i ryzyka związane z dzieleniem się genami.
Cytowanie: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Słowa kluczowe: koniugacja bakteryjna, odporność na antybiotyki, struktura pilusa, lipidy błonowe, interakcje elektrostatyczne