Clear Sky Science · ja
Hピリンの環化とピルス生合成は寛容だが静電的撹乱はコンジュゲーション効率を損なう
なぜ小さな細菌のケーブルが重要なのか
細菌は常にDNAをやり取りしており、抗生物質耐性のような形質を共有することで無害な微生物が治療困難な脅威へと変わることがある。その主要な経路の一つが接合であり、供与細胞がピルスと呼ばれる長く細い表面のケーブルを伸ばして隣接する細胞と接続し、プラスミドDNAを受け渡す。今回の研究は一見些細に思えるが重大な問いを投げかける:ピルスの表面上の正確な原子配置や受容菌の外膜にある脂質が、DNA移行の成否をどう制御しているのか?
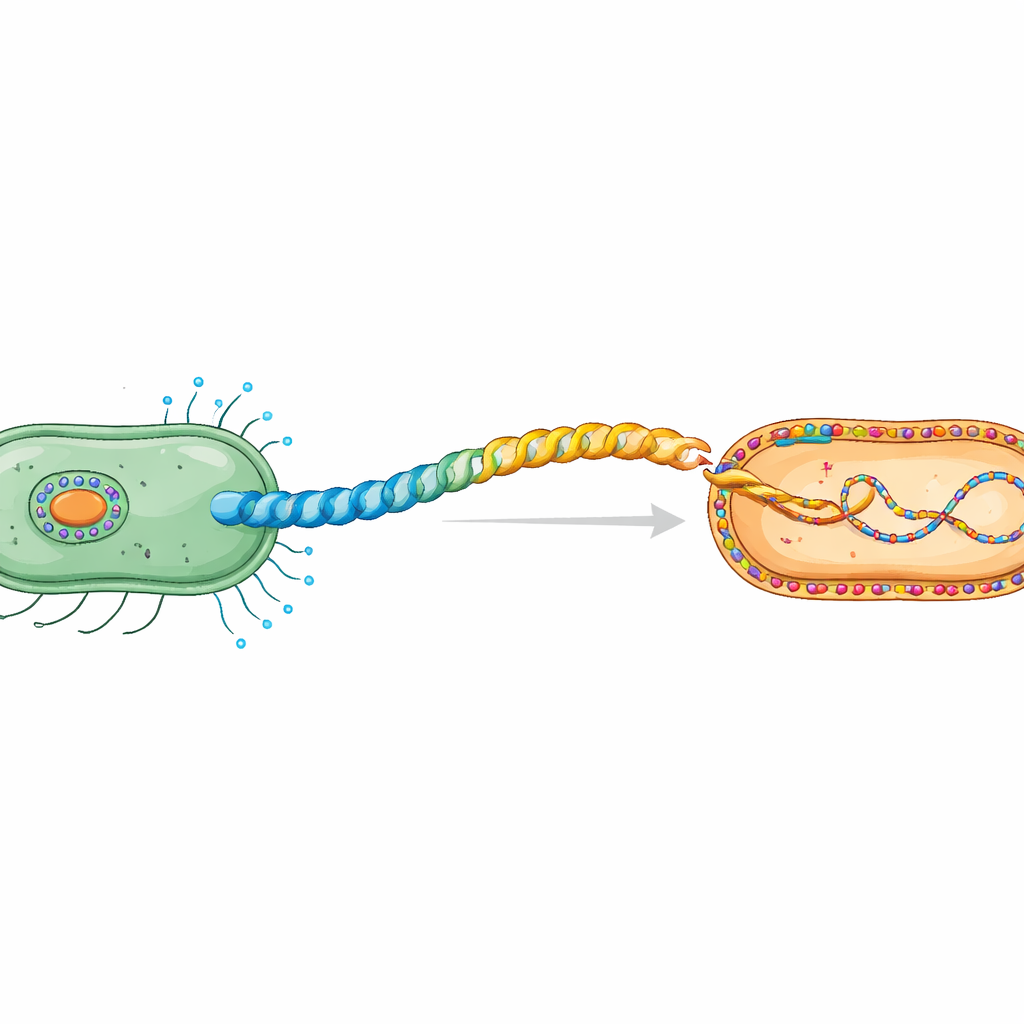
細菌間の秘密の握手
接合の際、プラスミドDNAは接触依存的なプロセスで供与細胞から受容細胞へ移動する。供与細胞はピリニン(pilin)という繰り返し単位からなる柔軟ならせん状の管状構造、ピルスを構築する。本研究は抗生物質耐性の拡散で知られるIncHI1プラスミドR27がコードするHピルスに着目している。以前のクライオ電子顕微鏡解析により、このピリニン(TrhA)は特異で、鎖端が開放されたままではなく、N末端(Gly1)とC末端(Asp69)が結合して“リング”状に結ばれていることが示された。この環化はDNAを移送できる機能的なピルスを形成するために不可欠である。
高度に保存されたタンパク質末端、意外に許容的な化学性
研究者らは大規模なプラスミドデータベースを解析し、関連プラスミド由来の147配列のTrhAを調べた。多くの位置に変異が見られる一方で、環を閉じる2残基—Gly1とAsp69—は完全に保存されており、強い進化的圧力が働いていることを示唆した。チームはこれらの2箇所を系統的に変異させ、複数の変異体ピリニンを作製した。高解像度クライオEMにより、Asp69をAsn、Ala、Gly、あるいはArgのようにかなり異なるアミノ酸に置換しても、TrhAは環化しピルスとして組み立てられ、野生型とほとんど区別のつかない構造を示すことが明らかになった。言い換えれば、環化とピルス形成の化学は意外なほど寛容だった。
ケーブルの電荷が接続を遮るとき
見た目は正常でも、これらの変異ピルスは多様なグラム陰性受容菌を用いた接合試験で非常に異なる挙動を示した。Asp69が中性のアミノ酸(Asn、Ala、Gly)に置換された場合、プラスミドはE. coliやKlebsiella pneumoniaeへの移行を依然として良好に行った。種によっては微妙な傾向が見られ、大きな側鎖は一般に小さなものよりわずかに高い移行効率を示した。全く異なる結果をもたらしたのは、Asp69やGly1がアルギニンやリシンのような正に帯電するアミノ酸に置換された場合である。これらの変化はピルス表面の電荷を負から強い正へと反転させた。変異ピルスは形成され続けたが、野生型ピルスと比べて正常な受容体への接合は最大で百万分の一まで低下した。
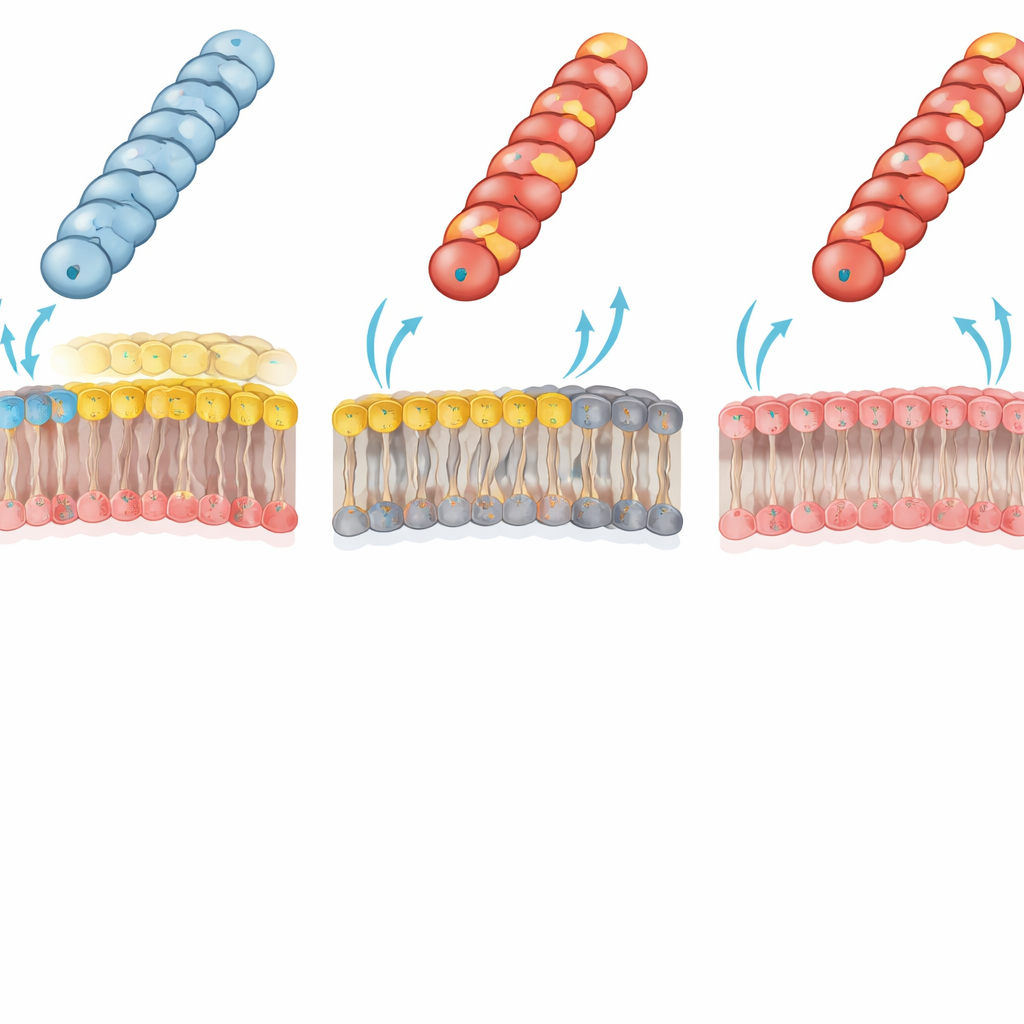
膜脂質が誰がDNAを受け取れるかを決める
著者らはこの劇的な失敗をピルスと受容細胞外膜の間の静電的な衝突に帰した。典型的なグラム陰性細菌では外膜の内側葉(inner leaflet)に主要な「双極性」リン脂質であるホスファチジルエタノールアミン(PE)が含まれ、正と負の両方の帯電基を持つ。チームはPEを欠くように設計した特殊なE. coli株を用い、その外膜内側葉は代わりに完全に負に帯電した脂質で構築されていた。このPE欠損受容体では、以前は機能不全だった正に帯電したピルス(Gly1Lys、Asp69Lys、Asp69Argなど)は野生型とほぼ同等の効率でプラスミドを移送できた。この逆転は、正に帯電したピルス表面とPEを多く含む膜との間の不利な電荷–電荷相互作用が通常、ピルス先端が効率的なDNA移行に必要な接触幾何をとるのを妨げるという考えを強く支持する。
静電的な微調整が抗生物質耐性の拡散をどう形作るか
総じて得られた結果は明確な分業を示している。ピリニン鎖を切断して再結合しリングを形成する化学機構はかなり柔軟であり、多くの異なる末端残基が結合されて外見上は正常なピルスに組み立てられ得る。しかし、成功する接合はこれら露出残基のサイズ、特に電荷に極めて敏感であり、それらが受容体膜の脂質環境と一致する必要があるピルス表面電位を形作るからである。この静電的な“チューニング”は、Gly1とAsp69が自然界でこれほど厳密に保存されている理由を説明する助けとなる。また、環境ストレスや宿主条件によって駆動される膜脂質組成の変化が、抗生物質耐性遺伝子を運ぶプラスミドの細菌間交換のしやすさを変動させ得ることを示唆する。実際、細菌の“握手”における両当事者は、遺伝子共有の利益とリスクのバランスを取るために表面を共進化させていると言える。
引用: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
キーワード: 細菌の接合, 抗生物質耐性, ピルス構造, 膜脂質, 静電相互作用