Clear Sky Science · it
La ciclizzazione della pilina H e la biogenesi del pili sono permissive ma le perturbazioni elettrostatiche compromettono l’efficienza della coniugazione
Perché contano i piccoli cavi batterici
I batteri scambiano costantemente DNA, condividendo tratti come la resistenza agli antibiotici che possono trasformare microbi innocui in minacce difficili da trattare. Una delle vie principali per questo scambio è la coniugazione, in cui un batterio donatore usa un lungo e sottile cavo superficiale chiamato pili per connettersi a un vicino e trasferire plasmidi. Questo studio pone una domanda sorprendentemente sottile ma dalle grandi implicazioni: come controllano gli esatti atomi sulla superficie del pili e i lipidi della membrana esterna del ricevente se il trasferimento di DNA avrà successo o meno?
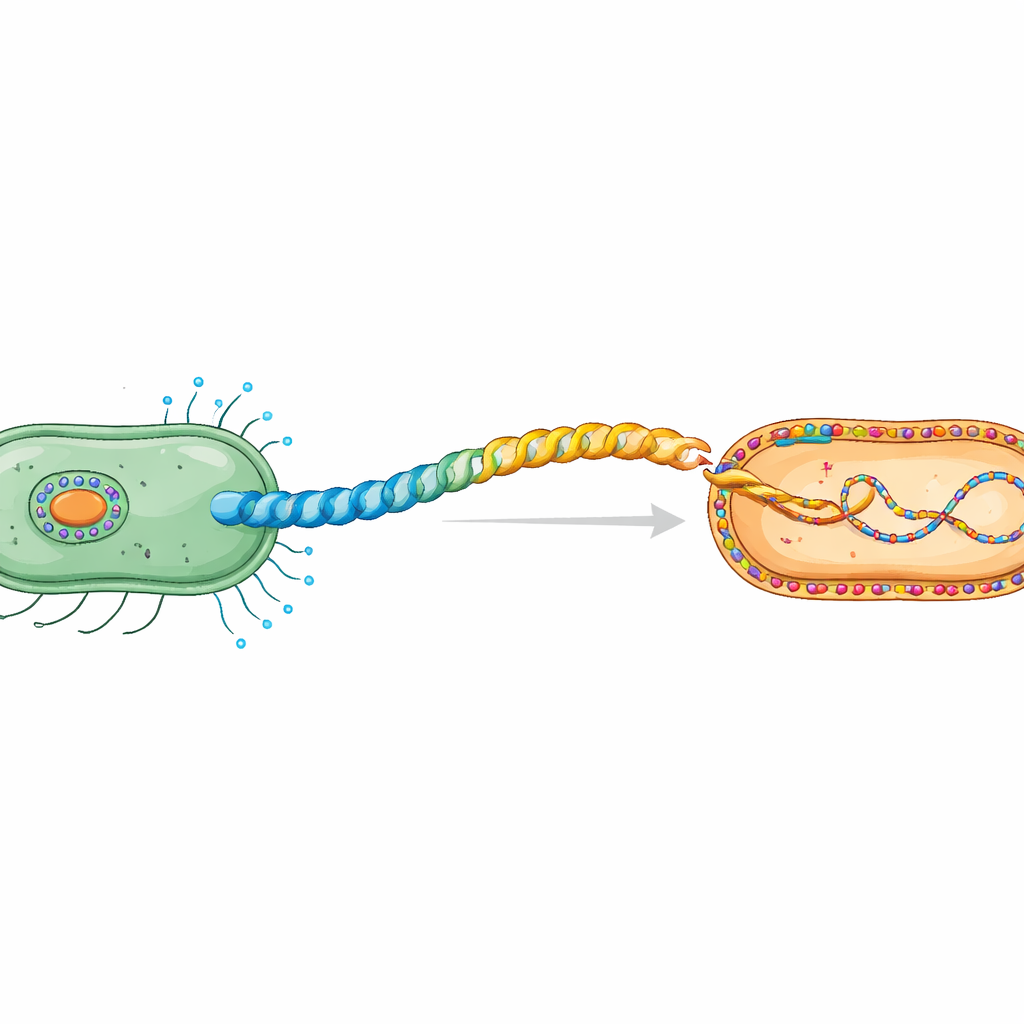
La stretta di mano segreta fra cellule batteriche
Durante la coniugazione, il DNA plasmidico passa da una cellula donatrice a una ricevente in un processo che richiede contatto. Le cellule donatrici costruiscono un pili speciale, un tubo elicoidale flessibile costituito da unità ripetute della proteina pilina. Il lavoro si concentra sull’H‑pilus codificato dal plasmide IncHI1 R27, una famiglia di plasmidi nota per la diffusione della resistenza agli antibiotici. Precedenti indagini con criomicroscopia elettronica avevano rivelato che la sua pilina, TrhA, è insolita: invece di avere una catena aperta, la proteina è “annodata in un anello” tramite l’unione dell’inizio (Gly1) e della fine (Asp69). Questa ciclizzazione è essenziale per formare un pili funzionale capace di trasferire DNA.
Punte proteiche altamente conservate, chimica sorprendentemente tollerante
Analizzando un ampio database di plasmidi, gli autori hanno esaminato 147 sequenze di TrhA provenienti da plasmidi correlati. Sebbene molte posizioni variassero, i due residui che chiudono l’anello—Gly1 e Asp69—erano assolutamente conservati, suggerendo una forte pressione evolutiva a mantenerli. Il gruppo ha quindi sostituito in modo sistematico queste due posizioni in laboratorio, creando diverse piline mutanti. La criomicroscopia elettronica ad alta risoluzione ha mostrato che persino aminoacidi molto diversi in Asp69 (come Asn, Ala, Gly o Arg) consentivano comunque a TrhA di ciclizzarsi e assemblarsi in pili strutturalmente quasi indistinguibili dal tipo selvatico. In altre parole, la chimica della formazione dell’anello e dell’assemblaggio del pili risultava sorprendentemente permissiva.
Quando la carica sul cavo blocca la connessione
Nonostante un aspetto normale, i pili mutanti si comportavano in modo molto diverso nei test di coniugazione con una gamma di riceventi Gram‑negativi. Quando Asp69 era sostituita da aminoacidi neutrali (Asn, Ala, Gly), i plasmidi venivano ancora trasferiti efficacemente in E. coli e Klebsiella pneumoniae. In alcune altre specie emersero tendenze sottili: catene laterali più grandi generalmente supportavano un’efficienza di trasferimento leggermente superiore rispetto a quelle più piccole. Un quadro molto diverso è apparso quando Asp69 o Gly1 furono sostituiti da aminoacidi carichi positivamente come arginina o lisina. Questi cambiamenti invertirono l’esterno del pili da carico negativo a fortemente positivo. Sebbene i pili mutanti si formassero ancora, la coniugazione verso riceventi normali calò fino a un milione di volte rispetto al pili di tipo selvatico.
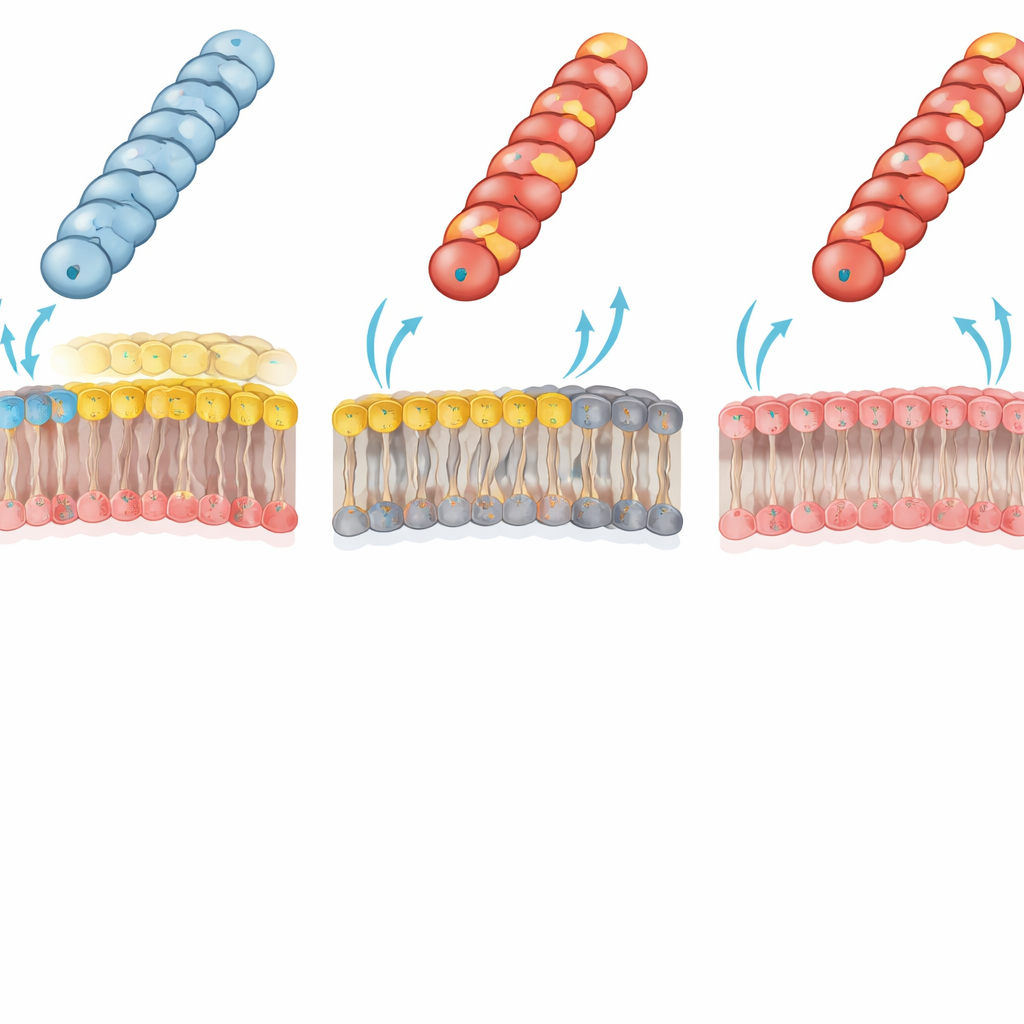
I lipidi di membrana decidono chi può ricevere DNA
Gli autori hanno ricondotto questo drastico fallimento a un conflitto elettrostatico tra il pili e la membrana esterna del ricevente. Nei batteri Gram‑negativi tipici, il foglietto interno della membrana esterna contiene un’importante fosfolipide “zwitterionico”, la fosfatidiletanolamina (PE), che porta sia un gruppo positivo sia uno negativo. Il team ha utilizzato un ceppo di E. coli appositamente ingegnerizzato privo di PE; il foglietto interno della sua membrana esterna è invece composto interamente da lipidi carichi negativamente. In questo ricevente carente di PE, i pili precedentemente compromessi e carichi positivamente (con Gly1Lys, Asp69Lys o Asp69Arg) trasferivano ora i plasmidi quasi con la stessa efficienza del tipo selvatico. Questa inversione supporta fortemente l’idea che un’interazione carica–carica sfavorevole tra una superficie del pili carica positivamente e la membrana ricca di PE normalmente impedisca alla punta del pili di adottare la geometria di contatto corretta per un efficiente trasferimento di DNA.
Come la sintonizzazione elettrostatica modella la diffusione della resistenza agli antibiotici
Nel complesso, i risultati rivelano una chiara divisione del lavoro. La macchina chimica che taglia e ricongiunge la catena della pilina per formare un anello è piuttosto flessibile—molti diversi residui terminali possono comunque essere cuciti insieme e assemblati in un pili dall’aspetto normale. Ma la coniugazione di successo è estremamente sensibile alle dimensioni e, soprattutto, alla carica di questi residui esposti, perché determinano il potenziale superficiale del pili che deve essere compatibile con l’ambiente lipidico della membrana del ricevente. Questa “sintonizzazione” elettrostatica aiuta a spiegare perché Gly1 e Asp69 sono così strettamente conservati in natura. Suggerisce anche che variazioni nella composizione lipidica della membrana—indotte da stress ambientali o condizioni dell’ospite—potrebbero modulare la facilità con cui i batteri scambiano plasmidi contenenti geni di resistenza agli antibiotici. In pratica, entrambi i partner nella “stretta di mano” batterica co‑evolvono le loro superfici per bilanciare benefici e rischi della condivisione genica.
Citazione: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Parole chiave: coniugazione batterica, resistenza agli antibiotici, struttura del pili, lipidi di membrana, interazioni elettrostatiche