Clear Sky Science · pt
A ciclização da pilina H e a biogênese do píleo são promíscuas, mas perturbações eletrostáticas prejudicam a eficiência da conjugação
Por que cabos bacterianos minúsculos importam
Bactérias trocam DNA constantemente, compartilhando características como resistência a antibióticos que podem transformar micróbios inofensivos em ameaças difíceis de tratar. Uma via principal para essa troca é a conjugação, em que uma bactéria doadora usa um cabo longo e fino na superfície, chamado píleo, para conectar-se a um vizinho e transferir DNA plasmidial. Este estudo faz uma pergunta surpreendentemente sutil, com grandes implicações: como os átomos exatos na superfície desse píleo, e os lipídios na membrana externa do receptor, controlam se a transferência de DNA terá sucesso ou falhará?
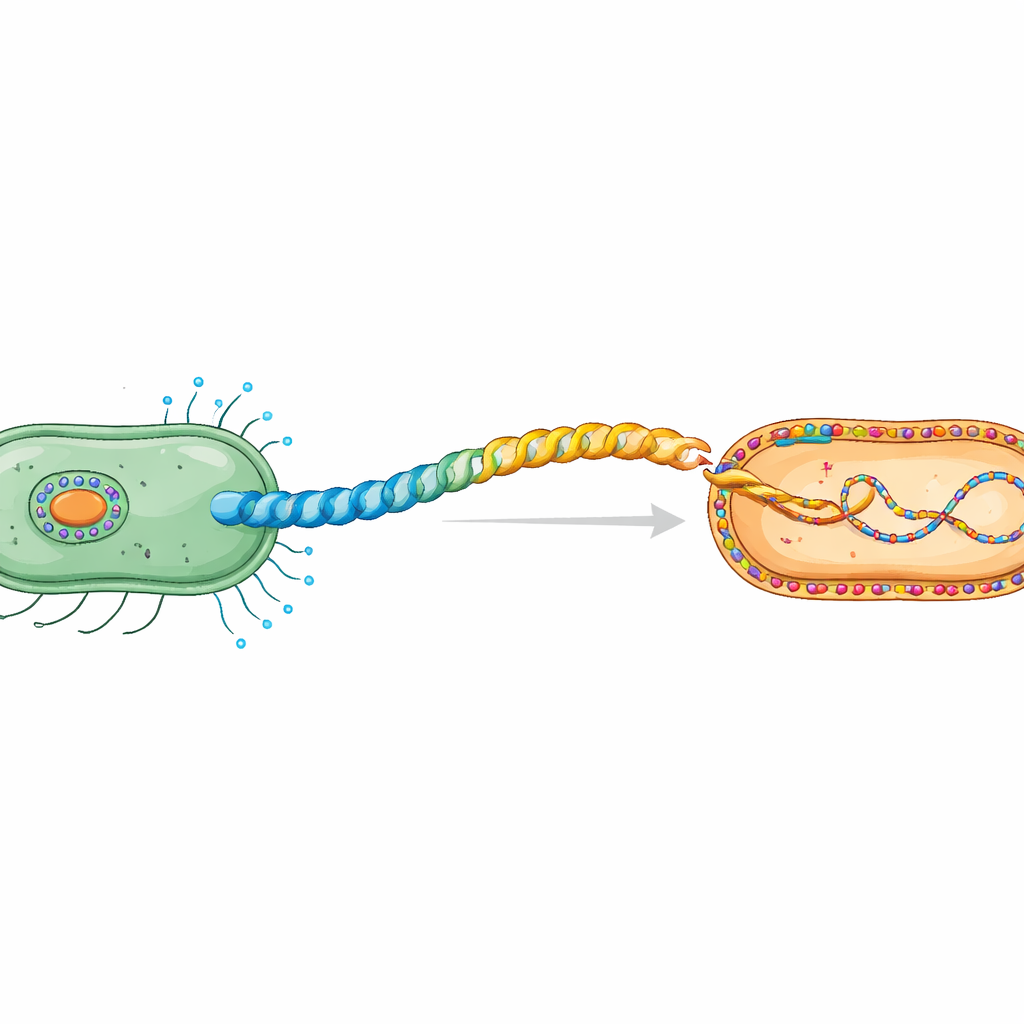
O aperto de mão secreto entre células bacterianas
Durante a conjugação, o DNA plasmidial viaja de uma célula doadora para uma receptora por um processo dependente de contato. Células doadoras constroem um píleo especial, um tubo helicoidal flexível feito de unidades repetidas da proteína pilina. O trabalho foca no píleo H codificado pelo plasmídeo IncHI1 R27, uma família de plasmídeos conhecida por disseminar resistência a antibióticos. Estudos anteriores por crio‑microscopia eletrônica revelaram que sua pilina, TrhA, é incomum: em vez de ter uma cadeia com pontas livres, a proteína é “amarrada em um anel” ao unir seu início (Gly1) e fim (Asp69). Essa ciclização é essencial para formar um píleo funcional capaz de transferir DNA.
Pontas proteicas altamente conservadas, química surpreendentemente tolerante
Minerando um grande banco de dados de plasmídeos, os autores examinaram 147 sequências de TrhA de plasmídeos relacionados. Embora muitas posições variassem, os dois resíduos que fecham o anel—Gly1 e Asp69—foram absolutamente conservados, sugerindo forte pressão evolutiva para mantê‑los. A equipe então alterou sistematicamente essas duas posições em laboratório, criando várias pilinas mutantes. Crio‑EM de alta resolução mostrou que mesmo aminoácidos bastante diferentes em Asp69 (como Asn, Ala, Gly ou Arg) ainda permitiam que TrhA ciclizar e se montasse em píleos estruturalmente quase indistinguíveis do tipo selvagem. Em outras palavras, a química da formação do anel e da montagem do píleo era surpreendentemente promíscua.
Quando a carga no cabo bloqueia a conexão
Apesar da aparência normal, os píleos mutantes comportaram‑se de modo muito diferente em testes de conjugação com uma gama de receptores Gram‑negativos. Quando Asp69 foi substituído por aminoácidos neutros (Asn, Ala, Gly), os plasmídeos ainda foram transferidos bem para E. coli e Klebsiella pneumoniae. Em algumas outras espécies surgiram tendências sutis: cadeias laterais maiores geralmente suportaram eficiência de transferência um pouco maior do que as menores. Um quadro muito diferente apareceu quando Asp69 ou Gly1 foram substituídos por aminoácidos positivamente carregados, como arginina ou lisina. Essas mudanças inverteram o exterior do píleo de negativamente carregado para fortemente positivo. Embora os píleos mutantes ainda se formassem, a conjugação em receptores normais caiu em até um milhão de vezes em comparação com o píleo do tipo selvagem.
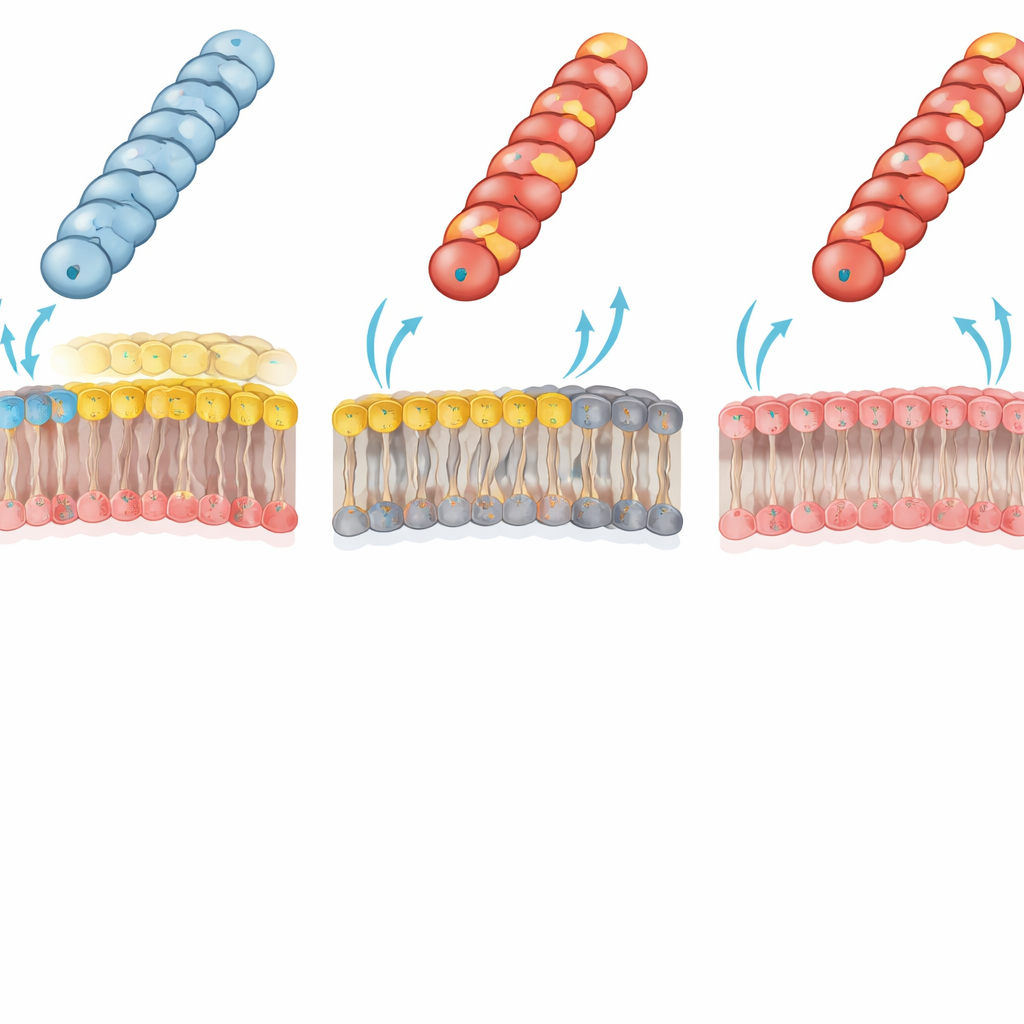
Os lipídios de membrana decidem quem pode receber DNA
Os autores atribuíram essa falha dramática a um choque eletrostático entre o píleo e a membrana externa do receptor. Em bactérias Gram‑negativas típicas, a monocamada interna da membrana externa contém um importante fosfolipídio “zwitteriônico”, a fosfatidiletanolamina (PE), que carrega tanto um grupo positivo quanto um negativo. A equipe usou uma cepa de E. coli especialmente engenheirada, sem PE; a monocamada interna de sua membrana externa é, em vez disso, composta inteiramente por lipídios carregados negativamente. Nesse receptor deficiente em PE, os píleos positivamente carregados que antes estavam inoperantes (com Gly1Lys, Asp69Lys ou Asp69Arg) agora transferiram plasmídeos quase tão eficientemente quanto o tipo selvagem. Essa reversão apoia fortemente a ideia de que uma interação carga–carga desfavorável entre uma superfície de píleo positivamente carregada e a membrana rica em PE normalmente impede que a ponta do píleo adote a geometria de contato correta para uma transferência eficiente de DNA.
Como o ajuste eletrostático fino molda a disseminação da resistência a antibióticos
Em conjunto, os resultados revelam uma divisão de funções clara. A maquinaria química que corta e junta a cadeia da pilina para formar um anel é bastante flexível—muitos resíduos terminais diferentes ainda podem ser unidos e montados em um píleo de aparência normal. Mas a conjugação bem‑sucedida é extremamente sensível ao tamanho e, especialmente, à carga desses resíduos expostos, porque eles moldam o potencial de superfície do píleo que deve combinar com o ambiente lipídico da membrana do receptor. Esse “ajuste” eletrostático ajuda a explicar por que Gly1 e Asp69 são tão estritamente conservados na natureza. Também sugere que mudanças na composição de lipídios da membrana—impulsionadas por estresse ambiental ou condições do hospedeiro—podem modular com que facilidade as bactérias trocam plasmídeos contendo genes de resistência a antibióticos. Em efeito, ambos os parceiros no “aperto de mão” bacteriano coevoluem suas superfícies para equilibrar os benefícios e riscos do compartilhamento de genes.
Citação: He, S., Ishimoto, N., Wong, J.L.C. et al. H pilin cyclisation and pilus biogenesis are promiscuous but electrostatic perturbations impair conjugation efficiency. Nat Commun 17, 2888 (2026). https://doi.org/10.1038/s41467-026-69599-3
Palavras-chave: conjugação bacteriana, resistência a antibióticos, estrutura do píleo, lipídios de membrana, interações eletrostáticas