Clear Sky Science · tr
PPP3CA/calcineurin’daki klinik missense varyantı E282K, aktif bölgeye alımı değiştirerek substrat defosforilasyonunu kaydırır
Beyin enziminin küçük bir değişikliği nasıl büyük sorunlara yol açar
Beyin hücrelerimiz sinyalleri sürekli olarak küçük kimyasal etiketler olan fosfatları ekleyip çıkararak açıp kapatır. Kalsinörin adı verilen anahtar bir enzim bu etiketlerin birçoğunu çıkarmaktan sorumludur ve geni PPP3CA’daki kalıtsal veya yeni ortaya çıkan mutasyonlar epilepsi ve gelişim geriliği ile karakterize şiddetli bir çocukluk hastalığıyla ilişkilendirilmiştir. Bu çalışma basit ama önemli bir soruyu sorar: kalsinörindeki tek bir yapı taşının değiştirilmesi beyin gelişimini nasıl bu kadar dramatik şekilde bozabilir?
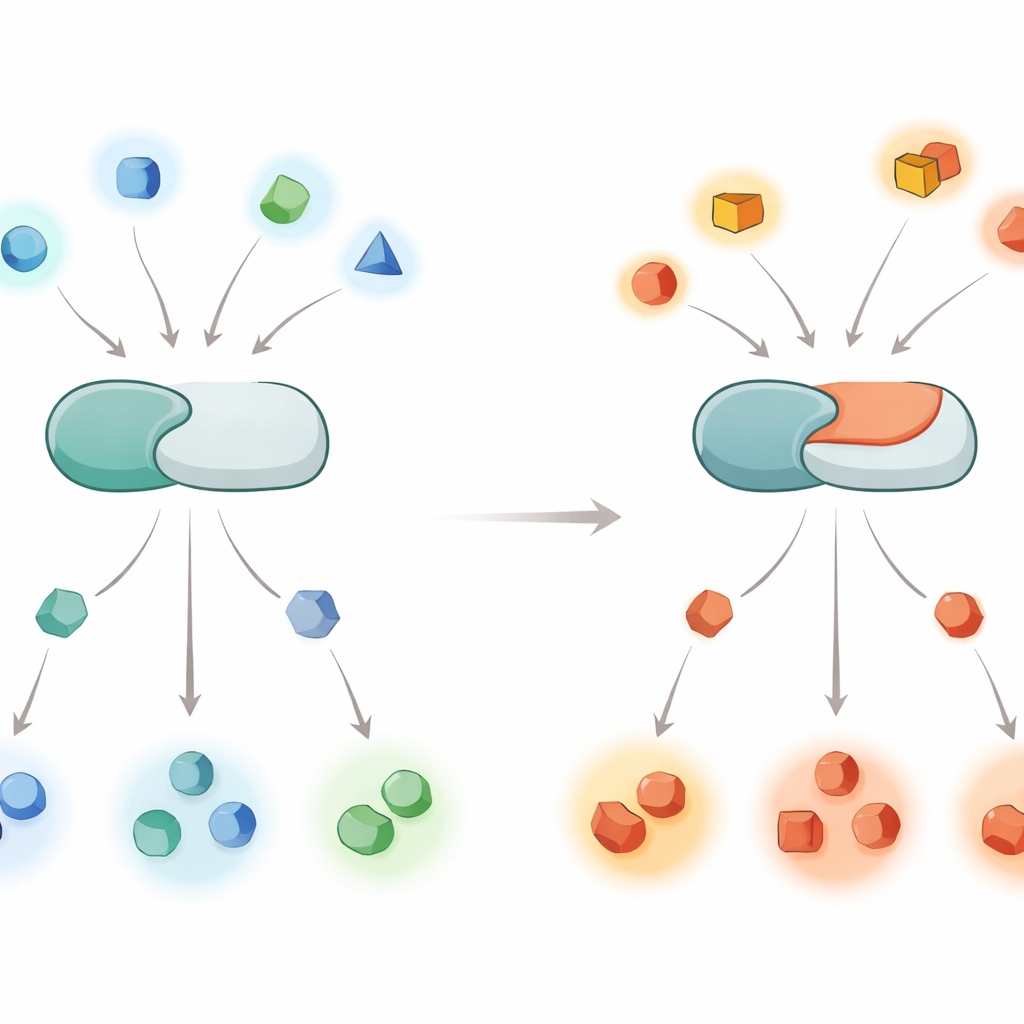
Hücreler kimyasal anahtarları nasıl kullanır
Hücre içindeki proteinler bir montaj hattındaki işçiler gibi davranır ve fosfat etiketleri bunları kontrol eden açma/kapama anahtarlarıdır. Kinazlar fosfat gruplarını takarken fosfatazlar onları çıkarır. Kalsinörin, kalsiyum sinyallerine yanıt veren bir fosfatazdır ve özellikle beyinde aktiftir; gelişimi, öğrenmeyi ve belleği kontrol etmeye yardımcı olur. Kalsinörin yüzlerce ila binlerce farklı protein hedefine dokunduğundan, hangi proteinlere etki ettiği konusundaki küçük hatalar bile birçok sinyal yolunda dalgalanmaya yol açabilir ve Alzheimer, Parkinson gibi hastalıklara veya PPP3CA ilişkili DEE91 olarak bilinen nadir gelişimsel duruma katkıda bulunabilir.
Çalışma bölgesinin yakınında gizli bir tutunma cebi
Araştırmacılar, kalsinörinin hedef proteinlerdeki spesifik noktaları nasıl tanıdığına odaklandı. Enzim çalıştırma bölgesinin hemen yanında önceden fark edilmemiş bir “alım/tutum cebi” olduğunu keşfettiler. Bazı kinazlar tarafından önceden modifiye edilen birçok hedef proteinin, fosfat etiketinden hemen önce pozitif yüklü bir amino asit olan arjinin taşıdığı görüldü. Yapısal biyoloji, bağlanma ölçümleri ve tüp içi reaksiyonları kullanarak ekip, bu arjininin E282 adlı kalsinörin kalıntısı çevresinde inşa edilmiş negatif yüklü bir cebe yerleştiğini; böylece etiketlenmiş bölgeyi enzimin fosfatı verimli şekilde çıkarabilmesi için çektiğini gösterdi.
E282K mutasyonunun gerçekten yaptığı şey
PPP3CA ilişkili DEE91’li çocuklarda, kalsinörinde en yaygın değişiklik E282’nin farklı bir amino asit olan lizine dönüşmesiyle oluşan E282K varyantıdır. İlginç bir şekilde kristal yapılar enzimin genel şeklinin neredeyse değişmeden kaldığını ve diğer tutunma bölgelerinin hâlâ işlev gördüğünü ortaya koydu. Kritik fark yerel kimyada yatar: bir zamanlar asidik ve açık olan E282 çevresindeki cep daha bazik hale gelir ve yeni bir iç tuz köprüsü ile kısmen tıkanır. Sonuç olarak, bu cebe arjinin yerleşmesine dayanan peptidler artık zayıf bağlanır ve çok daha düşük verimle defosforile edilir.
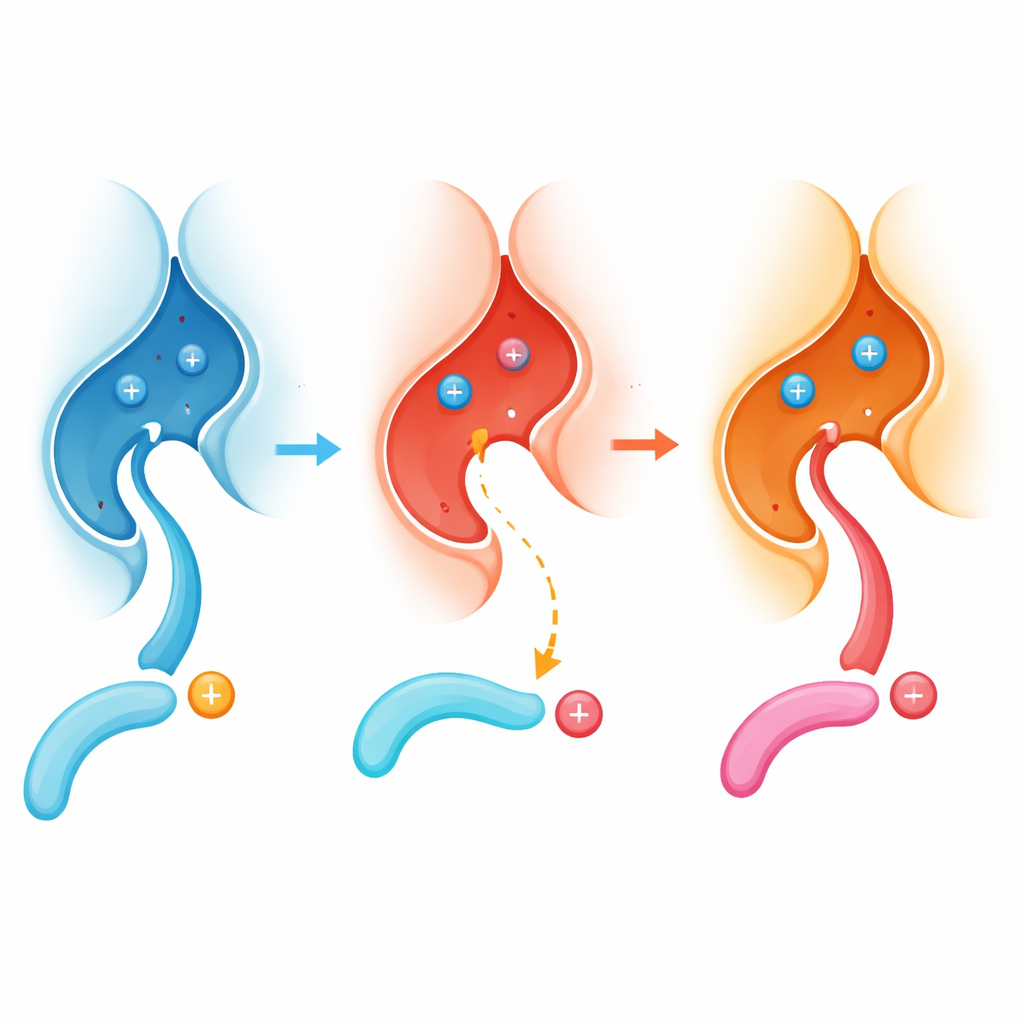
Kimlerin kapatıldığına dair küresel bir kayma
Bu etkinin ne kadar uzağa ulaştığını görmek için yazarlar insan hücrelerinden türetilen binlerce fosfopeptidi inceledi ve normal ile mutant kalsinörinin bunlar üzerinde zaman içinde nasıl davrandığını karşılaştırdı. Normal kalsinörin, fosfatın hemen öncesinde pozitif yüklü aminoasitlere (arjinin veya lizin gibi) sahip bölgelere güçlü şekilde öncelik veriyordu. Buna karşılık E282K versiyonu bu tercihin çoğunu kaybetmiş ve bunun yerine o pozisyonda negatif yüklü residülere sahip bölgeleri daha rahat işliyordu. Benzer desenler, ekibin iki enzim biçimini canlı hücre hatlarında (nöron benzeri bir hattı da dahil) ifade edip hangi protein bölgelerinin daha fazla veya daha az defosforile edildiğini kütle spektrometrisi ile katalogladığında da görüldü. Mutasyon, enzimi “bazik” bölgeleri seven bir durumdan “asidik” bölgeleri tercih eden bir duruma etkin biçimde yeniden ayarlıyor.
Bu neden DEE91’li çocuklar için önemlidir
Çalışma, E282K mutasyonunun kalsinörini basitçe zayıflatmadığını veya kapatmadığını gösteriyor. Bunun yerine, enzimin hangi protein anahtarlarını çevirebileceğini yeniden kablolar; hücre içindeki sinyal ağlarını kaydırır. Gelişen ve büyüyen beyin hücrelerinde, sinyallerin—normal arjinin açısından zengin hedeflerden uzaklaşıp farklı bölgelere yönelmesi—ince dengelenmiş programları bozması muhtemeldir; bu programlar nöronal büyüme, bağlantılanma ve elektriksel aktiviteyi kontrol eder. Bu spesifik alım cebini ve E282K’nin cebin yükünü ve erişimini nasıl değiştirdiğini belirleyerek çalışma hastalığı moleküler düzeyde anlamanın temelini atıyor ve mutasyon tersine çevrilemese bile doğru substrat seçimini geri getirmeye yönelik yeni tedavi arayışları için yol gösteriyor.
Atıf: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Anahtar kelimeler: kalsinörin, PPP3CA mutasyonu, protein fosforilasyonu, nörogelişimsel bozukluklar, enzim özgüllüğü