Clear Sky Science · ru
Клинический миссенс-вариант E282K в PPP3CA/кальциневрине смещает дефосфорилирование субстратов, изменяя привлечение к активному центру
Когда крошечная смена в мозговом ферменте вызывает большие проблемы
Наши нервные клетки постоянно включают и выключают сигналы, добавляя и убирая крошечные химические метки — фосфаты. Ключевой фермент кальциневрин отвечает за удаление многих таких меток, и наследственные или возникшие de novo мутации в его гене PPP3CA связаны с тяжелым детским заболеванием, сопровождающимся эпилепсией и задержкой развития. В этом исследовании ставится простой, но важный вопрос: как замена всего одного строительного блока в кальциневрине может так драматически нарушить развитие мозга?
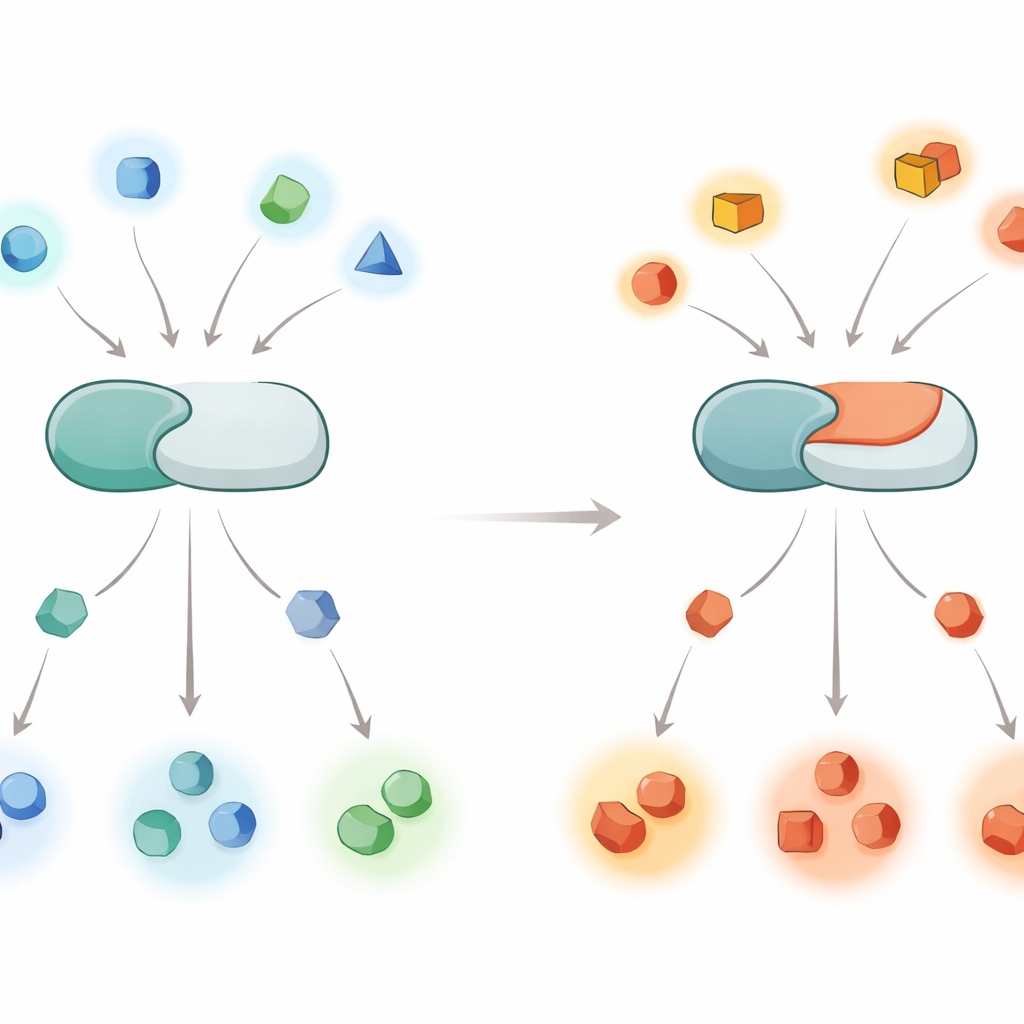
Как клетки используют химические выключатели
Белки в клетках работают как рабочие на конвейере, а фосфатные метки — это выключатели включения/выключения, которые ими управляют. Киназы добавляют фосфаты, фосфатазы их снимают. Кальциневрин — это фосфатаза, реагирующая на сигналы кальция и особенно активная в мозге, где он помогает регулировать развитие, обучение и память. Поскольку кальциневрин воздействует на сотни и даже тысячи разных белковых мишеней, даже небольшие ошибки в том, какие белки он обслуживает, могут отразиться на множестве сигнальных путей, способствуя таким заболеваниям, как болезнь Альцгеймера, болезнь Паркинсона и редкое развитиеое состояние, известное как DEE91, связанное с PPP3CA.
Скрытый «пристыковочный» карман рядом с рабочим центром
Исследователи сосредоточились на том, как кальциневрин распознает определенные участки на своих белковых мишенях. Они обнаружили ранее не распознанный «карман привлечения» прямо рядом с рабочим центром фермента. Многие белки-мишени, которые сначала модифицируются определенными киназами, имеют положительно заряженную аминокислоту — аргинин — непосредственно перед фосфатной меткой. С помощью структурной биологии, измерений сродства и реакций в пробирке команда показала, что этот аргинин встраивается в отрицательно заряженный карман, сформированный вокруг остатка кальциневрина E282, помогая подтянуть фосфорилированный участок в положение, удобное для эффективного удаления фосфата.
Что же делает мутация E282K
У детей с DEE91, связанным с PPP3CA, наиболее частая замена в кальциневрине меняет E282 на другую аминокислоту — лизин, создавая вариант E282K. Удивительно, но кристаллические структуры показали, что общая форма фермента остается почти неизменной и его другие сайты взаимодействия по-прежнему функционируют. Ключевое различие заключается в локальной химии: ранее кислый, открытый карман вокруг E282 становится более основным и частично блокируется новой внутренней ионной связью. В результате пептиды, которые зависят от того, что аргинин размещается в этом кармане, теперь слабо связываются и гораздо менее эффективно дефосфорилируются.
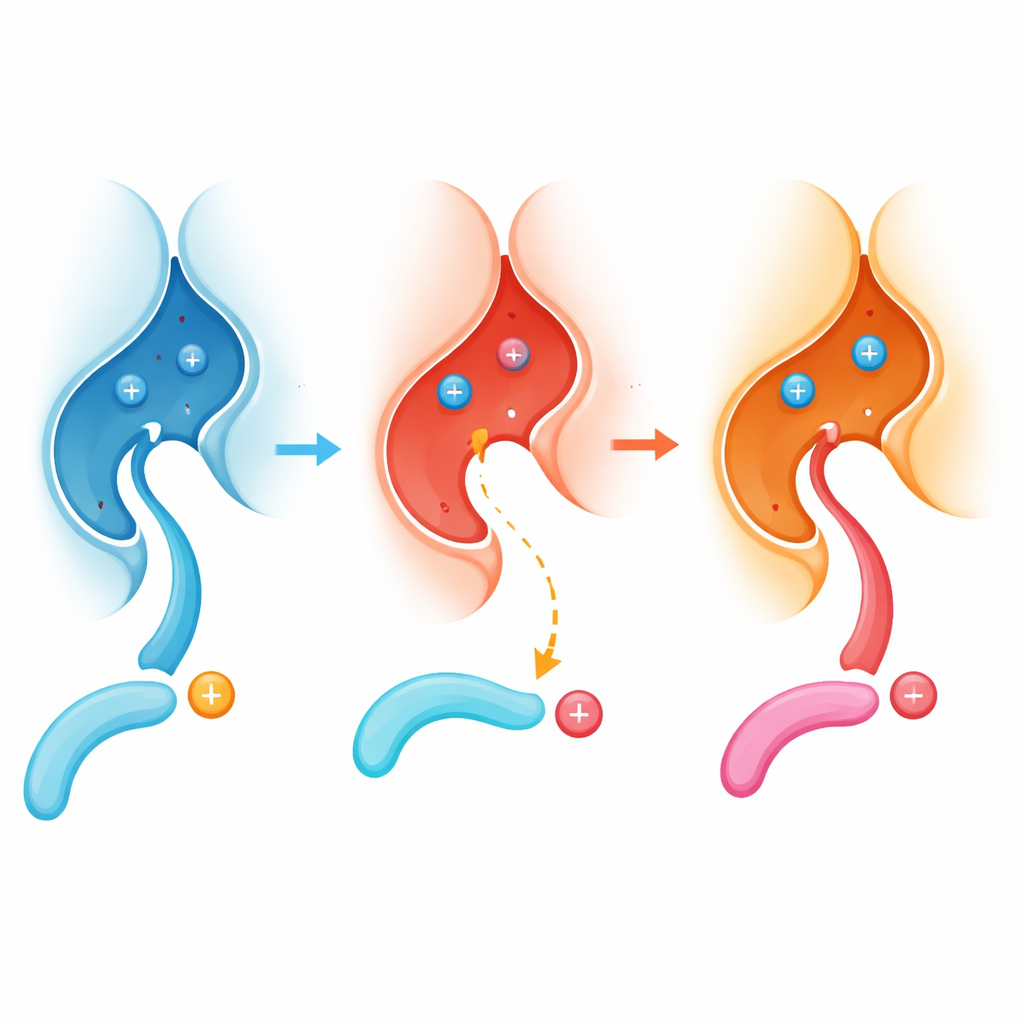
Глобальный сдвиг того, кто выключается
Чтобы понять масштаб эффекта, авторы проанализировали тысячи фосфопептидов, полученных из человеческих клеток, и сравнили, как нормальный и мутантный кальциневрин действуют на них со временем. Нормальный кальциневрин явно предпочитал сайты с положительно заряженными остатками (такими как аргинин или лизин) непосредственно перед фосфатом. В отличие от него, вариант E282K потерял большую часть этой предпочтительности и вместо этого охотнее обрабатывал сайты с отрицательно заряженными остатками в той позиции. Похожие закономерности наблюдались и при экспрессии двух форм фермента в живых клеточных линиях, включая нейроподобную линию, с последующим масс-спектрометрическим каталогизацией сайтов, которые становились более или менее дефосфорилированными. Мутация фактически перенастраивает фермент с «любви» к основным сайтам на предпочтение кислых.
Почему это важно для детей с DEE91
Работа показывает, что мутация E282K не просто ослабляет кальциневрин или выключает его. Скорее, она перестраивает набор белковых «выключателей», которые фермент может переворачивать, смещая сигнальные сети по всей клетке. В растущих и развивающихся нейронах такое широкое перенаправление сигналов — от их обычных аргинино-богатых мишеней к другим участкам — вероятно, нарушает тонко сбалансированные программы, контролирующие рост нейронов, их связность и электрическую активность. Указав на этот конкретный карман привлечения и объяснив, как E282K меняет его заряд и доступность, исследование закладывает молекулярную основу для понимания болезни и предлагает новые пути поиска терапий, которые могли бы восстановить правильный отбор субстратов, даже если саму мутацию обратить нельзя.
Цитирование: Shirakawa, K.T., Parikh, T., Machado, L.E. et al. The clinical missense variant E282K in PPP3CA/calcineurin shifts substrate dephosphorylation by altering active site recruitment. Nat Commun 17, 2837 (2026). https://doi.org/10.1038/s41467-026-69535-5
Ключевые слова: кальциневрин, мутация PPP3CA, фосфорилирование белков, нейроразвитные расстройства, специфичность фермента